Canlı görüntüleme "tespit" teknolojisi "gizli" hücrelerin saklanacak hiçbir yeri olmamasını sağlıyor
Çıplak farelerde tümör büyümesini gerçek zamanlı olarak kontrol etmek ister misiniz? Farelerde hücre kolonizasyonunun yerini bilmek ister misiniz? İlaç tedavisinin tümörler üzerindeki etkisini bilmek ister misiniz? canlıda? Hücreye bir izleyici takılarak bu sağlanabilir, böylece hücrelerin yeri ve sayısı her an kontrol edilebilir. Bu teknoloji in vivo görüntüleme "tespit" teknolojisidir. Peki in vivo görüntüleme teknolojisi nedir?
1. İn vivo görüntüleme teknolojisi nedir?
2. Lüsiferaz görüntülemenin özellikleri
3. Lüsiferaz görüntülemenin uygulama yönü
4. Deneysel örnek paylaşımı
5. SSS
6. Ürün bilgisi
7. Okuma ile ilgili
1. İn vivo görüntüleme teknolojisi nedir?
1999'da, ABD'deki Harvard Üniversitesi'nden Dr. Weissleder, moleküler görüntüleme kavramını, yani hücresel ve moleküler düzeylerde canlı organizmadaki biyolojik süreçler üzerinde nitel ve nicel araştırmalar yürütmek için görüntüleme yöntemlerini kullanmayı önerdi. Canlı organizmadaki görüntüleme, moleküler görüntülemeye dayanır. Bu görüntüleme sistemi sayesinde, tümör büyümesi ve metastaz, bulaşıcı hastalıkların gelişimi ve belirli genlerin ifadesi gibi biyolojik süreçler canlı hayvanlarda gözlemlenebilir.
Canlı hayvanların canlıda optik görüntülenmesi esas olarak iki teknolojiyi benimser: biyolüminesans ve floresans. Biyolüminesans, hücreleri veya DNA'yı işaretlemek için kullanılan lüsiferaz genidir, floresans teknolojisi ise yeşil floresan proteini ve kırmızı floresan proteini gibi floresan haberci genleri ve FITC, Cy5 ve Cy7 gibi floresans kullanır. Etiketleme için elementler ve kuantum noktaları (QD). Memeli biyolüminesansı genellikle ateş böceği lüsiferaz genini (554 nükleotidden oluşur, yaklaşık 50KD), yani lüsiferaz genini, lüsiferaz ifade etmek için beklenen gözlem hücresinin kromozomal DNA'sına entegre eder. Daha sonra lüsiferazı stabil bir şekilde ifade edebilen bir hücre hattı yetiştirilir ve hücreler bölündüğünde, farklılaştığında ve transfer olduğunda lüsiferaz da stabil bir şekilde ifade etmeye devam eder. Genler, hücreler ve canlı hayvanların hepsi lüsiferaz geni ile etiketlenebilir. Lüsiferaz, biyolüminesans üretmek için substratları katalize edebilen bir enzim türüdür. Farklı kaynaklardan gelen lüsiferazlar kendi özelliklerine sahiptir ve farklı renklerde ışık yaymak için substratları katalize edebilir. Bunlar arasında, ateş böceği lüsiferazının yüksek hassasiyeti ve 7~8 büyüklük mertebesinde geniş bir doğrusal aralığı vardır. En yaygın kullanılan memeli hücre haberci geni haline gelmiştir. Lüsiferaz haberci plazmidi hücrelere aktarıldı ve hücreleri inkübe etmek için substratı lüsiferin eklendi. ATP varlığında, O2ve magnezyum iyonları, lüsiferaz lüsiferin substratını oksitleyerek görünür ışık reaksiyonu üretebilir. "Tek seferlik 'izleyici' kurulumunu gerçekleştirin ve istediğiniz zaman izleyin ve tespit edin". Ateş böceği lüsiferazına ek olarak, bazen renilla lüsiferaz da kullanılır. İkisinin substratları farklıdır, birincisinin substratı D-lüsiferindir ve ikincisinin substratı koelenterazindir. İkisinin ışık yayan dalga boyları farklıdır, birincisinin yaydığı ışık dalga boyu aralığı 540-600 nm'dir ve ikincisinin yaydığı ışık dalga boyu aralığı 460-540 nm'dir. Birincisinin yaydığı ışığın dokulardan geçmesi daha kolaydır, ikincisi vücutta daha hızlı metabolize edilir ve özgüllüğü birincisi kadar iyi değildir. Bu nedenle, çoğu in vivo deneyde haberci gen olarak ateş böceği lüsiferazı kullanılmaz.
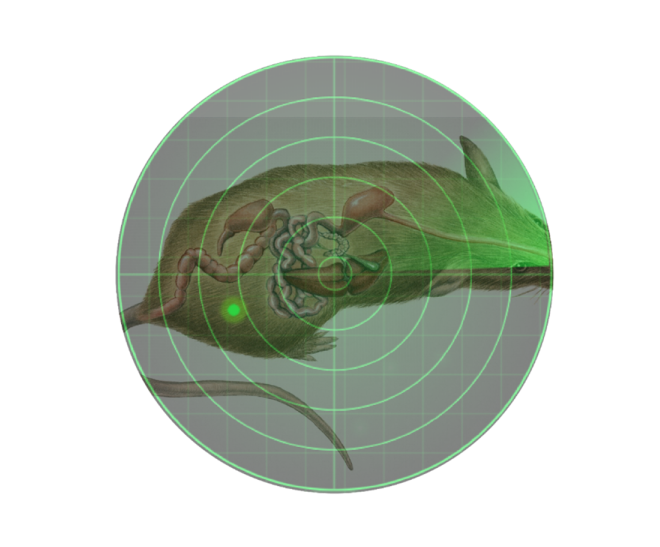
Şekil 1.Lüsiferaz etiketli hücrelerin lokalizasyonu
Biyolüminesansın optik prensibi: ışık memeli dokularında yayılırken dağılır ve emilir ve fotonlar hücre zarı ve sitoplazma ile karşılaştığında kırılır ve farklı hücre ve doku tipleri farklı foton emme özelliklerine sahiptir. Hemoglobin, vücuttaki görünür ışığın emiliminin ana nedenidir ve görünür ışığın mavi-yeşil bandının çoğunu emebilir. Ancak 600 nm'den büyük görünür ışığın kırmızı ışık bandında, hemoglobinin emilimi çok küçüktür. Bu nedenle, büyük miktarda ışık doku ve deriden geçerek kırmızımsı bölgede tespit edilebilir. Canlı hayvan biyolüminesan görüntüleme teknolojisi kullanılarak en az birkaç yüz deri altı hücresi tespit edilebilir. Ancak, faredeki ışık kaynağının derinliğine bağlı olarak görülebilen minimum hücre sayısı değişir. Genel olarak konuşursak, her 1 cm'lik artış için ışık yoğunluğu 10 kat azalır ve zayıflama kan açısından zengin dokular ve organlar için daha fazla, kemiklere bitişik dokular ve organlar için ise daha az olur. Aynı derinlikte tespit edilen ışık şiddetinin hücre sayısıyla anlamlı doğrusal bir ilişkisi vardır ve tespit edilen ışık şiddeti cihaz tarafından hücre sayısını yansıtacak şekilde ölçülebilir.
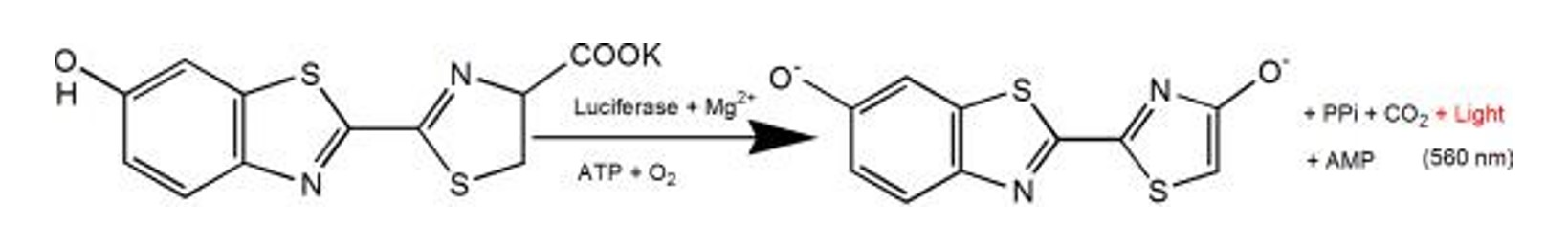
Şekil 2. Lüsiferaz ve lüsiferin potasyum tuzu reaksiyonunun lüminesans prensibi
Biyolüminesanstan farklı olarak, floresan teknolojisi etiketleme için floresan haberci genleri veya floresan boyaları (floresan kuantum noktaları gibi yeni nano etiketleme malzemeleri dahil) kullanır. Haberci genlerden, floresan proteinlerden veya boyalardan floresan kullanılarak canlı organizmada biyolojik bir ışık kaynağı yaratılabilir. Biyolüminesans, bir uyarım ışık kaynağı olmayan hayvanlarda otofloresanstır, floresan ise görüntüleme sistemi tarafından tespit edilebilmesi için harici bir uyarım ışık kaynağı tarafından uyarılma gerektirir. Floresan etiketler hayvanlar, hücreler, mikroorganizmalar, antikorlar, ilaçlar, nanomalzemeler vb. dahil olmak üzere yaygın olarak kullanılır.
2. Lüsiferaz görüntülemenin özellikleri
◎ radyasyon yok, organizmalar için neredeyse zararsız.
◎ Uyarıcı ışık kaynağı olmaksızın biyolüminesans.
◎ Yüksek hassasiyetle yüzlerce hücre tespit edilebilir.
◎ İyi penetrasyon kabiliyeti, 3-4 cm doku derinliğinde bile tespit edilebilir.
◎ yüksek sinyal-gürültü oranı, güçlü floresan sinyali ve iyi anti-parazit.
3. Lüsiferaz görüntülemenin uygulama yönü
3.1 Tümör büyümesi
Çıplak farelerde tümör oluşumu deneyinde, tümör büyümesi gerçek zamanlı olarak invazyon olmaksızın gözlendi ve ölçüm için tümörün soyulması gerekmedi.
3.2 Onkoloji ilaçları
Uygulamanın tümör büyümesi veya metastaz üzerindeki etkisi tespit edildi ve floresan substratı, ilaç deneyine müdahale etmeden 3 saat içinde ortadan kaldırılabildi.
3.3 Hücre lokalizasyonu
Hayvanlarda yabancı hücrelerin yerleşimi ve dağılımı tespit edildi.
3.4 Gen ifadesi düzenlemesi
İlaç tedavisi sırasında veya hastalığın seyri sırasında gen ekspresyonundaki değişiklikleri tespit etmek için hedef gen veya hedef genin promotörü, lüsiferaz geniyle birleştirildi.
3.5 Kök hücre araştırması
Kök hücrelerin nakli, hayatta kalması ve çoğalmasının izlenmesi; Kök hücrelerin dağılımının ve göçünün izlenmesi canlıda.
4. Deney örnek paylaşım

Şekil 3. canlıda CAR-MUC1'in terapötik etkisinin görüntülenmesi T/CAR-MUC1-IL22 HN4 hücrelerinin deri altına enjeksiyonuyla tümör oluşumunda T hücreleri fareler[1].
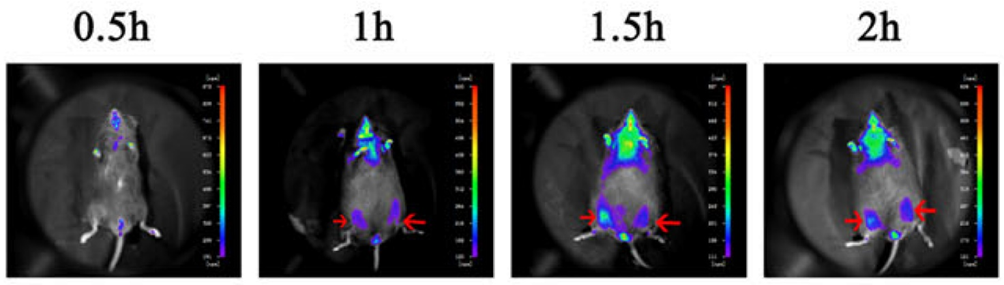
Şekil 4. HUC-MSC hücreleri fare iskelet kasına enjekte edildikten sonra, hücrelerin lokalizasyonu şu şekilde tespit edildi: canlıda görüntüleme (kırmızı okla işaretli)[2].
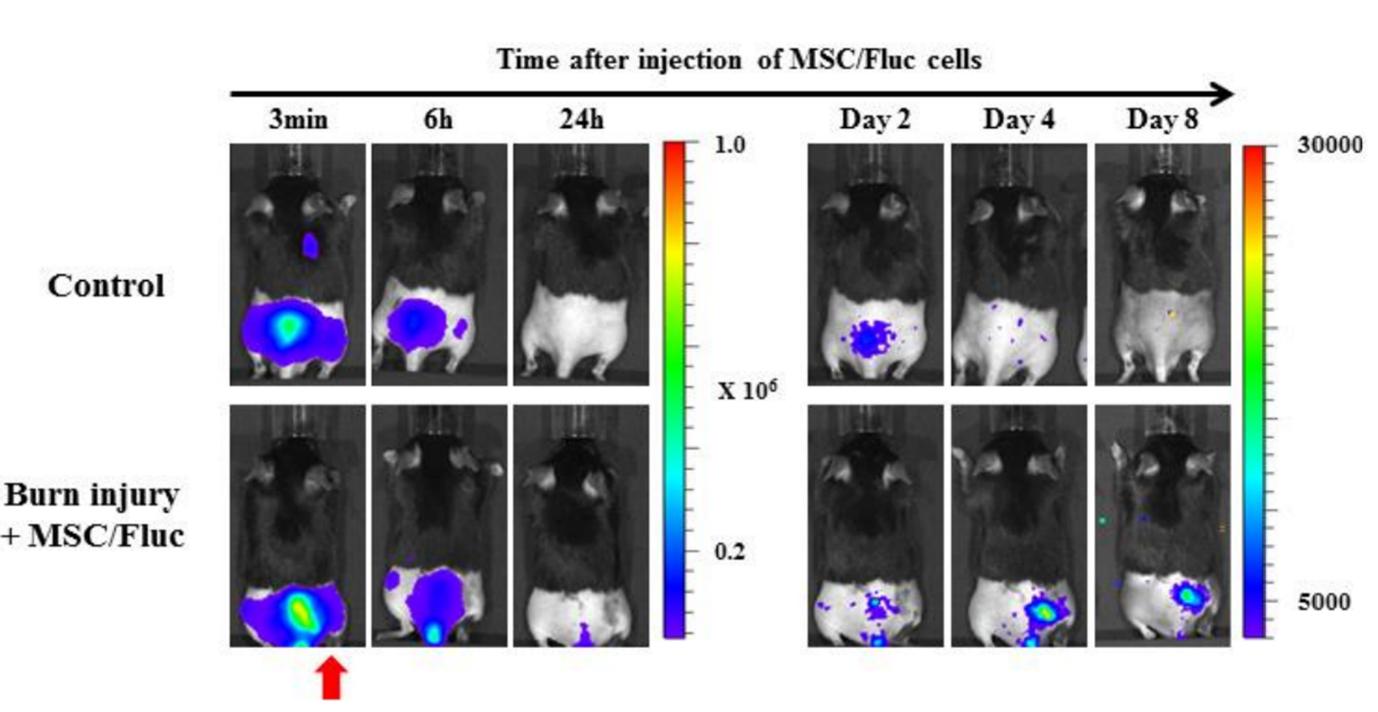
Şekil 5. Yeteneği canlıda mezenkimal kök hücrelerin (MSC) yanık bölgelerine göçünü tespit etmek için görüntüleme. Mezenkimal kök hücreler (MSC/FLuc) fare sırt yanık modeline intravenöz olarak enjekte edildi. Enjeksiyondan dört gün sonra, yanık yarasının yaralı bölgesinde biyolüminesans sinyalleri belirdi ve ardından kademeli olarak azaldı (kırmızı ok yanık bölgesini gösterir)[3].
5. SSS
S1: Biyolüminesans görüntüleme teknolojisinin geleneksel teknolojiye göre avantajları nelerdir?
Geleneksel teknolojiyle karşılaştırıldığında, bu teknoloji tümör metastazı, gen terapisi, epidemiyoloji, kök hücre izleme, lösemi ve diğer ilgili araştırmaların araştırılmasında geleneksel yöntemlerden daha hassastır. Ayrıca bir dizi transgenik hayvan hastalığı modeli aracılığıyla ilgili hastalıkların patogenezini ve ilaç taramasını hızlı ve sezgisel bir şekilde inceleyebilir.
S2: Kök hücreler lüsiferaz geni ile nasıl etiketlenir?
Yapısal olarak ifade edilen genler, transgenik fareler yapmak için etiketlenebilir ve kök hücreler etiketlenir. Hematopoietik kök hücreler farenin kemik iliğinden alınır ve başka bir farenin kemik iliğine nakledilir. Bu teknoloji, hematopoietik kök hücrelerin vücuttaki çoğalmasını, farklılaşmasını ve göçünü izlemek için kullanılabilir. Başka bir yöntem de kök hücreleri lentivirüs ile etiketlemektir.
S3: Floresan enjeksiyonundan sonra test yapmak ne kadar süre uygundur ve lüminesans ne kadar sürebilir?
Genellikle, floresan sinyali intraperitoneal enjeksiyondan sonra 10-15 dakika boyunca en güçlü stabil döneme ulaşır ve 20-30 dakika sonra azalmaya başlar. 3 saat sonra, floresan ortadan kalkar ve lüminesans tamamen kaybolur.
S4: Floresin farelere nasıl enjekte edilir? Enjeksiyon yöntemleri arasındaki fark nedir?
Fluorescein farelere intraperitoneal enjeksiyon veya kuyruk damarı enjeksiyonu ile enjekte edilebilir. Yaklaşık 1 dakikada farelerin tüm vücuduna yayılabilir. Çoğu durumda, florescein konsantrasyonu 150 mg/kg'dır. 20 g fareler için yaklaşık 3 mg florescein kullanılabilir. İntraperitoneal enjeksiyon için difüzyon yavaştır, ilk lüminesans yavaştır ve sürekli lüminesans süresi uzundur. Fluoresceinin kuyruk damarı enjeksiyonu için hızla yayılır ve hızla ışık yaymaya başlar, ancak lüminesans süresi kısadır.
6.Ürün bilgisi
Yeasen, üç ana biyolojik reaktifin araştırma, geliştirme, üretim ve satışıyla uğraşan bir biyoteknoloji şirketidir: moleküller, proteinler ve hücreler. Yeasen tarafından sağlanan ürünler aşağıdaki gibidir.
Tablo 1. Ürün bilgisi
| Ürün bilgisi | Ürün kodu | Özellikler |
| D-Lusiferin, Sodyum Tuzu | 40901ES01/02/03/08/10 | 0,1/0,5/1/5/10 gr |
| D-Lusiferin, Potasyum Tuzu | 40902ES01/02/03/08 | 0,1/0,5/1/5 gr |
| D-Lusiferin Firefly, Serbest Asit (Soruşturma) | 40903ES01/02/03 | 0,1/0,5/1 |
| Coelenterazine h (Soruşturma) | 40906ES02/03/08 | 0,5/1/5 mg |
| Kullanıma Hazır Coelenterazine h (Soruşturma) | 40907ES10 | 10 şişe |
| Çift Lüsiferaz Muhabir Gen Testi Kiti (Soruşturma) | 11402ES60/80 | 100/1000T |
| Luciferase Reporter Gen Analiz Kiti (Soruşturma) | 11401ES60/76/80 | 100/500/1000T |
| VDR (D Vitamini Reseptörü) Lüsiferaz Muhabir Plazmidi (Soruşturma) | 11502ES03 | 1μg |
| STAT1 Lüsiferaz Muhabir Plazmidi (Soruşturma) | 11504ES03 | 1μg |
7. Okuma ile ilgili
Yeni nesil lüsiferaz muhabir gen tespit sistemi——Daha kolay, daha hassas, daha kesin
