In vivo billeddannelses-"detektions"-teknologi gør, at "undercover"-celler ingen steder kan gemme sig
Vil du kontrollere tumorvækst i nøgne mus i realtid? Vil du vide placeringen af cellekolonisering i mus? Vil du vide effekten af lægemiddelbehandling på tumorer in vivo? Disse kan opnås ved at installere en tracker på cellen, så du til enhver tid kan kontrollere placeringen og antallet af celler. Denne teknologi er in vivo billeddannende "detektions" teknologi. Så hvad er in vivo billedteknologi?
1. Hvad er in vivo billedteknologi?
2. Karakteristika ved luciferase-billeddannelse
3. Anvendelsesretning af luciferase-billeddannelse
4. Eksperimentel eksempeldeling
5. FAQ
6. Produktinformation
7. Vedrørende læsning
1. Hvad er in vivo billedteknologi?
Allerede i 1999 foreslog Dr. Weissleder fra Harvard University i USA konceptet molekylær billeddannelse, det vil sige at bruge billeddannelsesmetoder til at udføre kvalitativ og kvantitativ forskning i biologiske processer in vivo på cellulært og molekylært niveau. In vivo billeddannelse er baseret på molekylær billeddannelse. Gennem dette billeddannelsessystem kan biologiske processer såsom tumorvækst og metastaser, udvikling af infektionssygdomme og ekspression af specifikke gener observeres i levende dyr.
In vivo anvender optisk billeddannelse af levende dyr hovedsageligt to teknologier: bioluminescens og fluorescens. Bioluminescens er luciferasegenet til at markere celler eller DNA, mens fluorescensteknologi bruger fluorescerende reportergener såsom grønt fluorescerende protein og rødt fluorescerende protein og fluorescens såsom FITC, Cy5 og Cy7. Elementer og kvanteprikker (QD) til mærkning. Pattedyrs bioluminescens integrerer generelt ildflueluciferasegenet (sammensat af 554 nukleotider, ca. 50KD), det vil sige luciferasegenet, i kromosomalt DNA af den forventede observationscelle for at udtrykke luciferase. Dyrk derefter en cellelinje, der stabilt kan udtrykke luciferase, og når cellerne deler sig, differentierer og overføres, vil luciferasen også fortsætte med at udtrykke stabilt. Gener, celler og levende dyr kan alle mærkes med luciferasegenet. Luciferase er en slags enzym, der kan katalysere substrater til at producere bioluminescens. Luciferaser fra forskellige kilder har deres egenskaber og kan katalysere substrater til at udsende forskellige farver af lys. Blandt dem har ildflueluciferase høj følsomhed og et bredt lineært område på 7 ~ 8 størrelsesordener. Det er blevet det mest almindeligt anvendte pattedyrscelle-reportergen. Luciferase-reporterplasmidet blev overført til cellerne, og dets substrat luciferin blev tilsat for at inkubere cellerne. I nærværelse af ATP, O2og magnesiumioner, kunne luciferase oxidere luciferinsubstratet for at frembringe en synlig lysreaktion. Realiser "engangs 'tracker' installation, og spor og detekter til enhver tid". Ud over ildflue-luciferase bruges nogle gange renilla-luciferase. Substraterne af de to er forskellige, substratet af førstnævnte er D-luciferin, og substratet af sidstnævnte er coelenterazin. De lysemitterende bølgelængder af de to er forskellige, området for lysbølgelængden udsendt af førstnævnte er 540-600 nm, og området for lysbølgelængden udsendt af sidstnævnte er 460-540 nm. Det lys, der udsendes af førstnævnte, er lettere at passere gennem væv, mens sidstnævnte metaboliseres hurtigere i kroppen, og dets specificitet er ikke så god som førstnævnte. Derfor er det ikke de fleste in vivo-eksperimenter, der bruger ildflue-luciferase som et reportergen.
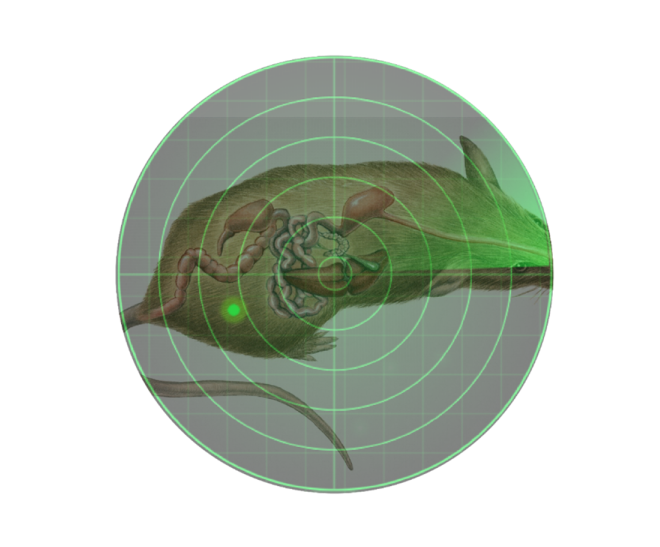
Figur 1.Lokalisering af luciferase-mærkede celler
Det optiske princip for bioluminescens: lys vil blive spredt og absorberet, når det formerer sig i pattedyrsvæv, og fotoner vil blive brudt, når de møder cellemembran og cytoplasma, og forskellige typer celler og væv har forskellige egenskaber ved at absorbere fotoner. Hæmoglobin er hovedårsagen til absorptionen af synligt lys i kroppen og kan absorbere det meste af det blågrønne bånd af synligt lys. Men i det røde lysbånd af synligt lys større end 600nm er absorptionen af hæmoglobin meget lille. Derfor kan en stor mængde lys passere gennem væv og hud for at blive opdaget i det rødlige område. Mindst et par hundrede subkutane celler kan påvises ved hjælp af levende animalsk bioluminescerende billeddannelsesteknologi. Men afhængigt af dybden af lyskilden i musen varierer det mindste antal celler, der kan ses. Generelt for hver stigning på 1 cm dæmpes lysstyrken 10 gange, og dæmpningen er mere for væv og organer rige på blod og mindre dæmpning for væv og organer, der støder op til knogler. I tilfælde af samme dybde har den detekterede lysintensitet et signifikant lineært forhold til antallet af celler, og den detekterede lysintensitet kan kvantificeres af instrumentet for at afspejle antallet af celler.
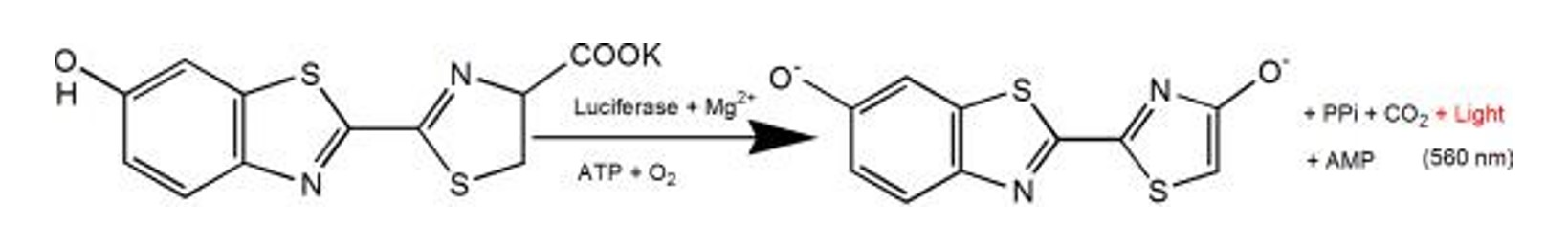
Figur 2. Det selvlysende princip for luciferase og luciferinkaliumsaltreaktion
Forskellig fra bioluminescens bruger fluorescensteknologi fluorescerende reportergener eller fluorescerende farvestoffer (herunder nye nanomærkningsmaterialer såsom fluorescerende kvanteprikker) til mærkning. Ved at bruge fluorescens fra reportergener, fluorescerende proteiner eller farvestoffer kan der skabes en biologisk lyskilde in vivo. Bioluminescens er autofluorescens hos dyr uden en excitationslyskilde, mens fluorescens kræver excitation af en ekstern excitationslyskilde, før den kan detekteres af billeddannelsessystemet. Fluorescerende etiketter er meget udbredt, herunder dyr, celler, mikroorganismer, antistoffer, lægemidler, nanomaterialer osv.
2. Karakteristika ved luciferase-billeddannelse
◎ ingen stråling, næsten uskadelig for organismer.
◎ bioluminescens uden excitationslyskilde.
◎ høj følsomhed, hundredvis af celler kan detekteres.
◎ god gennemtrængelighed, 3-4 cm vævsdybde kan stadig detekteres.
◎ højt signal-til-støj-forhold, stærkt fluorescenssignal og god anti-interferens.
3. Anvendelsesretning af luciferase-billeddannelse
3.1 Tumorvækst
I tumorgenese-eksperimentet i nøgne mus blev tumorvæksten observeret i realtid uden invasion, og der var ikke behov for at strippe tumoren til måling.
3.2 Onkologiske lægemidler
Indgivelsens indflydelse på tumorvækst eller metastase blev detekteret, og fluoresceinsubstratet kunne elimineres inden for 3 timer uden interferens med lægemiddelforsøget.
3.3 Cellelokalisering
Lokaliseringen og fordelingen af fremmede celler i dyr blev påvist.
3.4 Regulering af genekspression
Målgenet eller promotoren af målgenet blev fusioneret med luciferasegenet for at detektere genekspressionsændringer under lægemiddelbehandling eller sygdomsforløbet.
3.5 Stamcelleforskning
Overvågning af transplantation, overlevelse og spredning af stamceller; Sporing af stamcellers fordeling og migration in vivo.
4. Eksperiment eksempel deling

Figur 3. in vivo billeddiagnostisk påvisning af den terapeutiske effekt af CAR-MUC1 T/CAR-MUC1-IL22 T-celler på tumordannelse ved subkutan injektion af HN4-celler i mus[1].
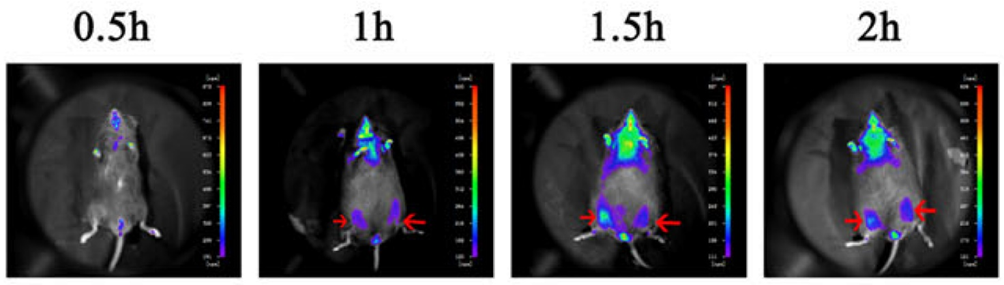
Figur 4. Efter at HUC-MSCs-celler var blevet injiceret i musens skeletmuskulatur, blev lokaliseringen af celler detekteret vha. in vivo billedbehandling (markeret med rød pil)[2].
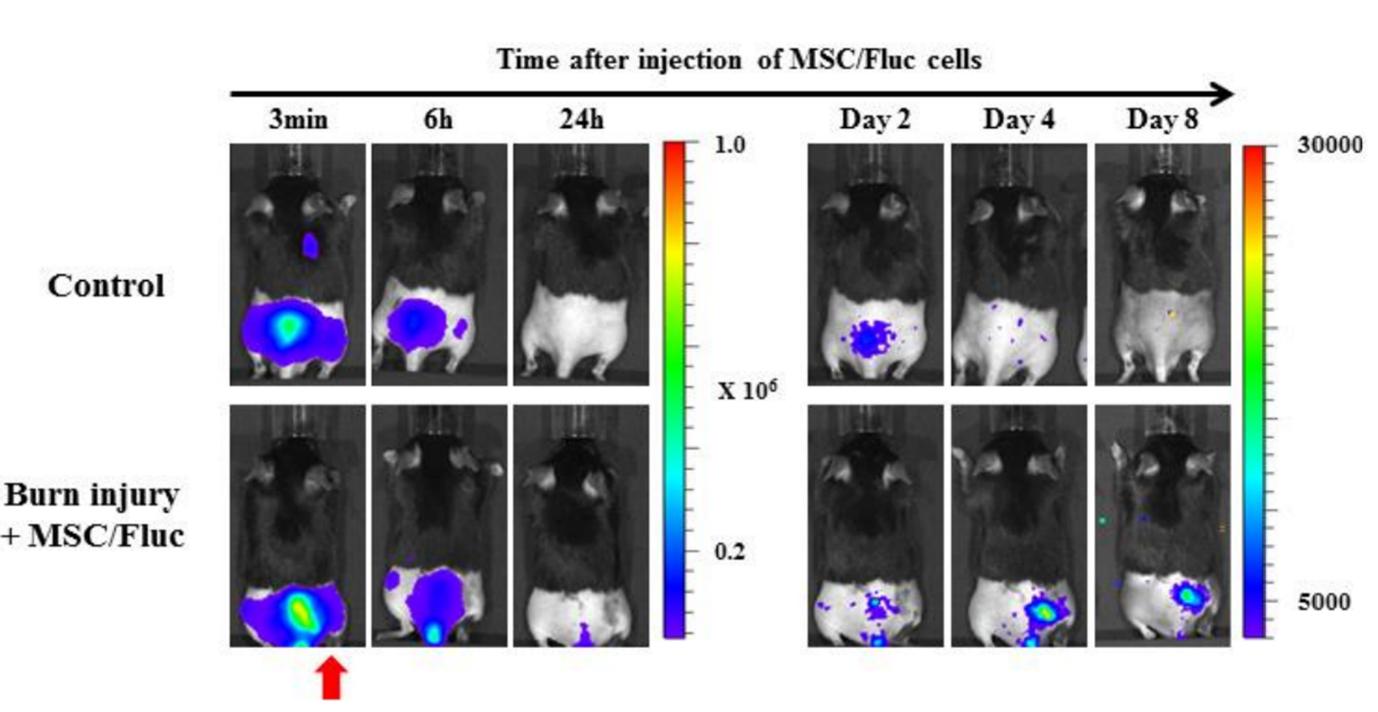
Figur 5. Evnen til in vivo billeddannelse for at detektere migrationen af mesenkymale stamceller (MSC) til forbrændingssteder. Mesenkymale stamceller (MSC/FLuc) blev injiceret intravenøst i museback burn-modellen. Fire dage efter injektionen optrådte bioluminescenssignaler på det skadede sted af forbrændingssåret og faldt derefter gradvist (den røde pil angiver forbrændingsstedet)[3].
5. FAQ
Q1: Sammenlignet med traditionel teknologi, hvad er fordelene ved bioluminescensbilledteknologi?
Sammenlignet med traditionel teknologi er denne teknologi mere følsom end de traditionelle metoder til forskning i tumormetastaser, genterapi, epidemiologi, stamcellesporing, leukæmi og anden relateret forskning. Det kan også hurtigt og intuitivt studere patogenesen og lægemiddelscreeningen af relaterede sygdomme gennem en række transgene dyresygdomsmodeller.
Q2: Hvordan mærker man stamceller med luciferasegenet?
De konstitutivt udtrykte gener kan mærkes til at lave transgene mus, og stamcellerne mærkes. De hæmatopoietiske stamceller tages fra musens knoglemarv og transplanteres ind i en anden muss knoglemarv. Denne teknologi kan bruges til at spore spredning, differentiering og migration af hæmatopoietiske stamceller i kroppen. En anden metode er at mærke stamceller med lentivirus.
Q3: Hvor længe er det passende at teste efter fluorescein-injektion, og hvor længe kan luminescensen vare?
Generelt når fluorescenssignalet den stærkeste stabile periode efter intraperitoneal injektion i 10-15 minutter og begynder at henfalde efter 20-30 minutter. Efter 3 timer er fluoresceinet elimineret, og luminescensen forsvinder fuldstændigt.
Q4: Hvordan injicerer man fluorescein i mus? Hvad er forskellen mellem injektionsmetoder?
Fluorescein kan injiceres i mus ved intraperitoneal injektion eller haleveneinjektion. Det kan spredes til hele musekroppen på cirka 1 min. I de fleste tilfælde er koncentrationen af fluorescein 150 mg/kg. Til 20 g mus kan der anvendes ca. 3 mg fluorescein. For intraperitoneal injektion er diffusionen langsom, den indledende luminescens er langsom, og den kontinuerlige luminescenstid er lang. Til haleveneinjektion af fluorescein diffunderer det hurtigt og begynder at udsende lys hurtigt, men varigheden af luminescens er kort.
6.Produktinformation
Yeasen er en bioteknologisk virksomhed, der beskæftiger sig med forskning, udvikling, produktion og salg af tre store biologiske reagenser: molekyler, proteiner og celler. Produkterne leveret af Yeasen er som følger.
Tabel 1. Produktinformation
| Produktinformation | Produktkode | Specifikationer |
| D-Luciferin, natriumsalt | 40901ES01/02/03/08/10 | 0,1/0,5/1/5/10 g |
| D-Luciferin, Kaliumsalt | 40902ES01/02/03/08 | 0,1/0,5/1/5 g |
| D-Luciferin Firefly, fri syre (Spørge) | 40903ES01/02/03 | 0,1/0,5/1 |
| Coelenterazin h (Spørge) | 40906ES02/03/08 | 0,5/1/5 mg |
| Klar til brug Coelenterazine h (Spørge) | 40907ES10 | 10 hætteglas |
| Dual Luciferase Reporter Gene Assay Kit (Spørge) | 11402ES60/80 | 100/1000T |
| Luciferase Reporter Gene Assay Kit (Spørge) | 11401ES60/76/80 | 100/500/1000T |
| VDR (Vitamin D Receptor) Luciferase Reporter Plasmid (Spørge) | 11502ES03 | 1 μg |
| STAT1 Luciferase Reporter Plasmid (Spørge) | 11504ES03 | 1 μg |
7. Vedrørende læsning
En ny generation af luciferase-reporter-gendetektionssystem - lettere, mere følsomt, mere præcist
