説明
Hieff NGS™ OnePot Pro DNAライブラリ準備キットV4は、イルミナで使用するために設計された次世代の酵素ライブラリ準備キットです。 および MGI ハイスループット シーケンシング プラットフォームで使用できます。従来のライブラリ作成方法と比較して、このキットは高品質の断片化酵素を使用しているため、面倒な超音波処理が不要です。断片化モジュールと末端修復モジュールが 1 つのステップに統合されているため、ライブラリ作成の時間とコストが大幅に削減されます。このキットは、植物や動物のゲノム、微生物のゲノムなど、さまざまなサンプル タイプに適しており、サンプル入力範囲は 1 ng から 1 μg です。酵素による断片化により、異なる種間での断片サイズが均一になり、種間の変動が最小限に抑えられます。さらに、このキットは Illumina またはMGI Illumina または MGI ハイスループット プラットフォームでのシーケンス用のアダプターとプライマー。
仕様
|
カタログ番号 |
12972ES08 / 12972ES24 / 12972ES96 |
|
サイズ |
8 24時間 96 円 T |
コンポーネント
|
コンポーネント番号 |
名前 |
12972 ES08 |
12972 ES24 |
12972 ES96 |
|
12972 -A |
80 μL |
240 μL |
960 μL |
|
|
12972 -B |
スメアラーゼ™酵素4.0 |
80 μL |
240 μL |
960 μL |
|
12972 -C |
ライゲーションエンハンサー4.0 |
240μL |
720μL |
3 ×960 μL |
|
12972 -D |
ラピッドDNA リガーゼ4.0 |
80 μL |
240 μL |
2 × 480μL |
|
12972 -E |
2×Ultima HF 増幅ミックス |
200μL |
600μL |
3×8 00μL |
ストレージ
この製品は-25〜-15℃で1年間保管してください。 年。
注記
1. 操作について
1.安全のため、白衣と使い捨て手袋を着用して作業してください。
2. 成分を室温で解凍します。解凍後、ボルテックスでよく混ぜ、チューブを軽く回転させて、後で使用するために氷上に置いておきます。
3.各ステップの反応溶液を調製する際は、ピペットを使用してよく混ぜるか、軽く振ることをお勧めします。激しく振るとライブラリ出力が低下する可能性があります。
4.交差汚染を避けるために、フィルター付きのピペットチップを使用することを強くお勧めします。異なるサンプルを処理するときは、必ずピペットチップを交換してください。
5. 不適切な操作はエアロゾル汚染を引き起こし、結果の精度に影響を与える可能性が非常に高いです。PCR反応混合領域とPCR産物精製アッセイ領域を物理的に分離することが推奨されます。ライブラリ構築用の専用ピペットなどの機器を装備しています。0.5 %次亜塩素酸ナトリウムまたは10%漂白剤で表面を拭いて、各エリアの定期的な清掃を実行します。
6. この製品は研究目的にのみご使用ください。
2. DNAの断片化1.このキットは 100 pg ~ 1,000 ng の入力 DNA に対応しています。A260/A280 = 1.8 ~ 2.0 の高品質入力 DNA を使用することを強くお勧めします。
2.入力 DNA に金属キレート剤などの高濃度の塩が導入されると、その後の実験に影響が出る可能性があります。断片化のために DNA サンプルをddH 2 Oで溶出することをお勧めします。
3.標準 DNA サンプルの断片化時間については、表6を参照してください。このキットは断片化バイアスが低く、幅広い GC 組成の DNA サンプルに対して均一な GC カバレッジを提供します。実験要件に基づいて断片化時間を調整してください。
4.正確な断片化のために、反応を氷上で準備してください。
3. アダプターライゲーション
1. 実験要件に応じて、Illumina または MGI ロング アダプター (バーコード アダプター) キットとショート アダプター キットを選択できます。
2. 高品質の市販のアダプターを選択することをお勧めします。自作のアダプターを選択する場合は、NGSプライマー合成の経験がある会社に委託し、厳格な汚染管理の必要性に留意してください。また、クロスコンタミネーションを防ぐために、クリーンベンチでDNAアニーリング溶液を調製し、毎回1種類のアダプターのみを操作することをお勧めします。
3. アダプターは氷の上または 4°C で解凍してください。室温で操作する場合は、アダプターの変性を防ぐために、実験室の温度が 25°C を超えないようにしてください。
4.アダプターの品質と濃度は、ライゲーション効率とライブラリ収量に直接影響します。アダプターの濃度が高すぎるとアダプター二量体の形成が促進され、アダプターが低すぎるとライゲーション速度とライブラリ収量が低下します。アダプターを使用する場合は、入力 DNA 量に応じて TE バッファーで希釈します。表 2 -3に、このキットを使用したさまざまな入力 DNA 量に対する推奨アダプター希釈方法を示します。
表1 異なる入力DNAに対するイルミナの推奨アダプター量
|
入力DNA |
アダプター希釈(アダプター容量:総容量) |
集中 |
|
1 ng |
30倍( 1:30 ) |
0.5 μM |
|
10 ng |
7.5倍(1: 7.5 ) |
2 μM |
|
100 ng |
3つ折り(1: 3 ) |
5 μM |
|
1000 ng |
1.5倍(1: 1.5 ) |
10 μM |
表2 異なる入力DNAに対する推奨MGIアダプター量
|
入力DNA |
アダプター希釈(アダプター容量:総容量) |
集中 |
|
1 ng |
20倍( 1:20 ) |
0.5 μM |
|
10 ng |
5折り(1 : 5 ) |
2 μM |
|
100 ng |
2つ折り(1: 2 ) |
5 μM |
|
1000 ng |
希釈されていない |
10 μM |
4.ビーズベースのDNAクリーンアップとサイズ選択
1. DNA 断片サイズの選択ステップは、アダプター連結後またはライブラリ増幅後に実行できます。
2.入力 DNA 量が 50 ng を超える場合は、アダプター連結直後にサイズ選択を実行することをお勧めします。それ以外の場合は、増幅後にサイズ選択を実行してください。
3.ライゲーションエンハンサーには高濃度の PEG が含まれており、正確なサイズ選択に重大な影響を及ぼす可能性があります。したがって、アダプターライゲーションの直後にサイズ選択を実行する場合は、サイズ選択の前にビーズクリーンアップステップを追加することを強くお勧めします。サイズ選択ステップは、エンド修復/dA テーリングの前、またはライブラリ増幅後に実行する場合は直接実行できます。
4.磁気ビーズは使用前に室温で平衡化する必要があります。そうしないと、収量が減少し、サイズ選択効果に影響が出ます。
5.磁気ビーズは使用前にボルテックスまたはピペッティングでよく混ぜてください。
6.上清を移すときにビーズを吸引しないでください。微量のビーズでも次の反応に影響を与える可能性があります。
7. 80% エタノールは新しく調製する必要があります。そうでないと回収効率に影響します。
8.正確なサイズ選択を行うには、100 μL 以上の容量から始めることをお勧めします。容量がそれより少ない場合は、超純水で容量を 100 μL まで増やすことをお勧めします。
9.磁気ビーズは、生成物を溶出する前に室温で乾燥させる必要があります。乾燥が不十分だと、残留エタノールが後続の反応に影響を与えやすくなります。乾燥が過剰だと、磁気ビーズが割れて精製収率が低下します。通常、室温で 3 ~ 5 分間乾燥させると、ビーズが完全に乾燥します。
10.必要に応じて、 0.1× TEバッファーで溶出した精製またはサイズ選択されたDNAサンプルは、 4°Cで1〜2週間、または-20°Cで1か月間保存できます。
5. ライブラリの拡張
1.ライブラリ増幅を実行するかどうかは、DNA入力量、アダプターの種類、シーケンスデータアプリケーションなどによって異なります。部分アダプターを使用する場合は、増幅ステップが必要です。全長アダプターを使用する場合、入力DNAが<200 ngの場合は増幅を実行することをお勧めします。それ以外の場合は、増幅は必要ありません。
2. 増幅サイクル数は厳密に制御する必要があります。増幅が不十分だとライブラリ収量が低下する可能性があり、増幅が多すぎるとバイアス、エラー、重複読み取り、キメラ産物の増加につながる可能性があります。表 3 1 μg のライブラリ収量を目標とした推奨サイクル数をリストします。
表3 1,000 ngのライブラリー収量を生成するための推奨サイクル数
|
入力DNA |
1μgのライブラリ収量を生成するために必要なサイクル数 |
|
1000 ng |
2 - 4 |
|
500 ng |
2 - 4 |
|
250 ng |
4 - 6 |
|
100 ng |
5 - 7 |
|
50 ng |
7 - 9 |
|
1 ng |
12 - 14 |
注記:
1.表3は、約200bpの高品質Input DNAテストを使用したループパラメータの数を示しています。FFPE DNAの品質は大きく異なり、DNAの品質が悪い場合やライブラリの長さが長い場合は、十分なライブラリを得るためにサイクル数を適切に増やす必要があります。
2.ライブラリ構築プロセス中にサイズ選択が必要な場合は、ライブラリ増幅のサイクル数を高くすることをお勧めします。それ以外の場合は、サイクル数を低くすることをお勧めします。
3.不完全なアダプターを使用する場合は、完全なアダプターを形成するために少なくとも 2 サイクルを増幅する必要があります。
6. ライブラリ品質分析
1. 構築されたライブラリの品質は、通常、濃度とサイズ分布を測定することによって分析されます。
2. ライブラリの濃度は、Qubit や PicoGreen などの蛍光ベースの方法や qPCR によって測定できます。
3. NanoDrop などの吸光度ベースの定量化方法の使用は推奨されません。
4. ライブラリの定量化には qPCR 法を使用することをお勧めします。Qubit や PicoGreen などの蛍光ベースの方法では、不完全な dsDNA 構造 (アダプターのない挿入物、または片方の端のみがアダプターで連結された挿入物) を完全なライブラリと区別できません。qPCR 法では、両端がアダプターで連結された完全なライブラリ (シーケンス可能なライブラリ) のみを増幅して測定するため、ローディングのより正確な測定が可能になります。
5. ライブラリのサイズ分布は、Agilent Bioanalyzer またはキャピラリー電気泳動やマイクロ流体の原理に基づくその他のデバイスを使用して分析できます。
7. その他の資料
1. DNA精製磁気ビーズ:Hieff NGS TM DNA選択ビーズ(Yeasen Cat#12601)またはAMPure® XP ビーズ (A63880) または同等の製品。
2. アダプター: Illumina 用完全アダプター: Yeasen Cat#13519-13520 ; 384 デュアル CDI プライマー: Yeasen Cat#12412~Cat#12413 ; 384 ユニークデュアルインデックス (UDI) プライマー: Yeasen Cat#1 2327 ~Cat#1 3330 ; UMI UDI アダプター: Yeasen Cat#13370~Cat#13371 ; MGI 用完全アダプター: Yeasen Cat#13360-13362。DNA プライマーミックス: Cat# 12190 またはカタログ番号12191。
3.ライブラリ品質分析: Agilent 2100 Bioanalyzer DNA 1000 Chip/High Sensitivity Chip または同等の製品、ライブラリ定量試薬。
4.その他の材料:無水エタノール、滅菌超純水、低保持ピペットチップ、PCRチューブ、磁気スタンド、サーマルサイクラーなど。
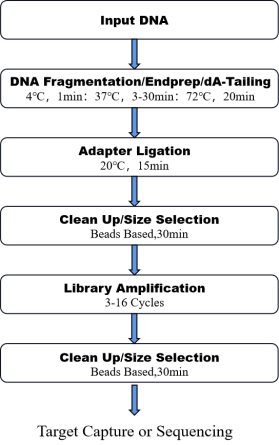
8.ワークフロー
図1. OnePot Pro DNAライブラリ準備キットのワークフロー
支払いとセキュリティ
お支払い情報は安全に処理されます。 クレジットカードの詳細を保存したり、クレジットカード情報にアクセスすることはありません
問い合わせ
あなたも好きかもしれません
よくある質問
この製品は研究目的のみに使用され、人間や動物の治療や診断に使用することを意図したものではありません。製品とコンテンツは、
特定のアプリケーションでは、追加のサードパーティの知的財産権が必要になる場合があります。