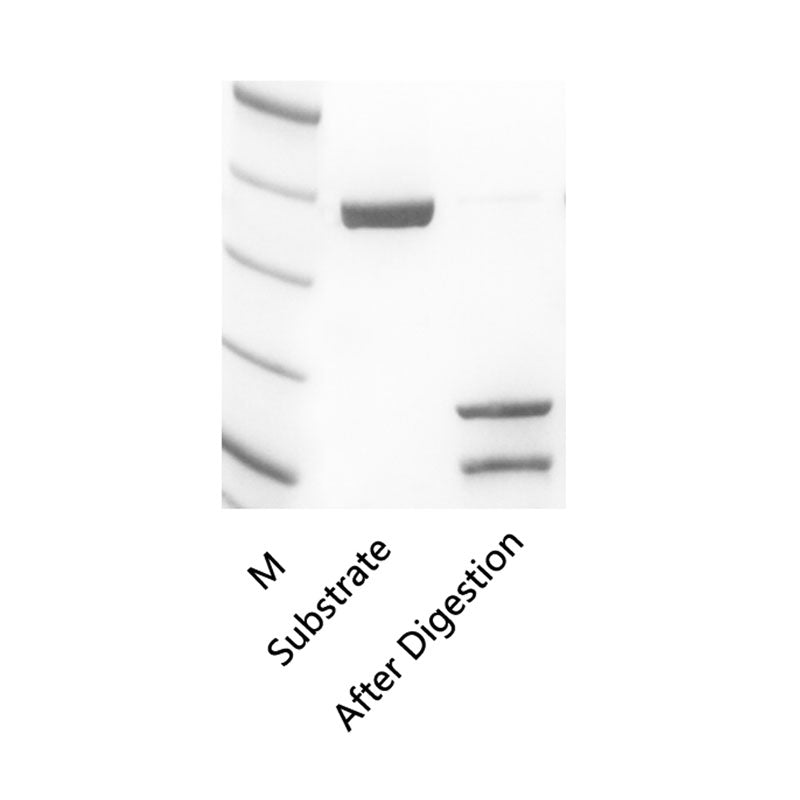
Beschrijving
Recombinant Enterokinase (rEK) is een zeer zuiver fragment van de recombinante bovine enterokinase light chain. De aminozuursequentie is identiek aan die van de bovine enterokinase light chain, met enzymatische splitsingsplaatsen die net zo specifiek zijn als die in natuurlijk geëxtraheerde enterokinase, met knipplaatsen op Asp-Asp-Asp-Asp-Lys. Dit maakt het mogelijk om het fusie-eiwit te verwijderen dat zich aan de N-terminus van het eiwit bevindt, waardoor onnodige fusietags worden geëlimineerd. Bovendien vertoont rEK een hogere splitsingsactiviteit vergeleken met het natuurlijke enzym.
De recombinante enterokinase is een zeer zuivere, zeer actieve en zeer specifieke runderenterokinase die wordt geproduceerd door recombinante expressie in Escherichia coli. Zonder andere proteasen kan het effectief fusie-eiwitten splitsen over een breed pH-bereik (4,5-9,5) en een breed temperatuurbereik. Het behoudt gedeeltelijke activiteit, zelfs in de aanwezigheid van verschillende detergenten en denaturerende middelen. Dit product is labelvrij en vanwege de extreem hoge enzymatische splitsingsactiviteit zijn er minimale hoeveelheden nodig voor splitsingsreacties, waardoor er geen interferentie is met downstream-eiwittoepassingen, waardoor verwijdering onnodig is.
Functie
Specificiteit: Het enzym vertoont specificiteit voor een bepaalde aminozuursequentie en knipt de aminozuren af aan de carboxylterminale plaats die vier asparaginezuren bevat, gevolgd door lysine (DDDDK).
Diervrij: Geproduceerd via recombinante methoden, waardoor er geen besmetting is van exogene virussen. Het productieproces omvat geen dierlijke materialen.
Kwaliteitsstabiliteit: Door batchproductie zijn consistente, stabiele batches gegarandeerd, zonder kwaliteitsverschillen tussen verschillende batches.
Hoge zuiverheid: Vrij van andere proteasen, waardoor niet-specifieke splitsing mogelijk is.
Naleving van regelgeving: Productiefaciliteiten en -omgevingen voldoen aan de relevante wettelijke vereisten. Het productieproces voldoet aan de GMP-richtlijnen.
Uitgebreide kwaliteitsdocumentatie: Kan relevante wettelijke ondersteunende documenten leveren volgens de vereisten van de klant.
Specificatie
| Bron | Uitgedrukt in E. coli. |
| Moleculair gewicht | 25,85 kDa |
| Verschijning | Heldere, kleurloze vloeistof. |
| Concentratie | ≥5 U/uL |
| Activiteit Definitie | Eén eenheid activiteit wordt gedefinieerd als de hoeveelheid enzym die nodig is om 95% van 500 μg van een 30KD fusie-eiwit dat enterokinase-splitsingsplaatsen bevat, onder de volgende omstandigheden: 25°C, 12-16 uur, in een buffersysteem bestaande uit 25 mM Tris-HCl, pH 8,0. |
| Endotoxine | <1 EU/μg |
| zorgverlener | ≤0,01% |
| Label | Nee |
| Opslagbuffer | 50 mM Tris-HCl, pH8.0,250 mM NaCl,2 mM CaCl2,50% Glycerol |
De hoeveelheid recombinant eiwit dat per eenheid Enterokinase (EK) wordt gekliefd
| Leveranciers | | Thermisch 1 Eenheden/μL | NEB 16 U/μL |
| Activiteit | 500 μg/U | 20 μg/U | 25 μg/U |
Opslag
Bewaren bij -25 tot -15°C voor 1 jaar.
Documenten:
Veiligheidsinformatieblad
Handleidingen
Betaling en beveiliging
Uw betalingsinformatie wordt veilig verwerkt. We slaan geen creditcardgegevens op en hebben geen toegang tot uw creditcardinformatie.
Navraag
Misschien vind je het ook leuk
FAQ
Het product is alleen bedoeld voor onderzoeksdoeleinden en is niet bedoeld voor therapeutisch of diagnostisch gebruik bij mensen of dieren. Producten en inhoud worden beschermd door patenten, handelsmerken en auteursrechten die eigendom zijn van
Voor bepaalde toepassingen zijn mogelijk aanvullende intellectuele eigendomsrechten van derden vereist.