Матрица базальной мембраны Ceturegel™ — ваш первый выбор
С развитием терапии стволовыми клетками и разработкой лекарств на основе органоидов, базальная мембранная матрица играет ключевую роль в качестве питательного вещества и носителя для культур стволовых клеток и органоидов, 3D-клеточных культур и других приложений, включая ангиогенез, эксперименты по онкогенезу in vivo и т. д. Экстракты базальной мембраны Ceturegel™ извлекаются из опухолей мышей Engelbreth-Holm-Swarm (EHS), богатых белками внеклеточного матрикса, включая ламинин, коллаген типа IV, нестин и т. д. IGF, FGF и другие факторы роста. При комнатной температуре базальная мембранная матрица Ceturegel™ полимеризуется, образуя биологически активную трехмерную матрицу. Она может имитировать структуру, состав, физические свойства и функции базальной мембраны клетки in vivo, что полезно для культивирования и дифференциации клеток in vitro и является хорошей альтернативой матригелю.
1. Что такое базальная мембранная матрица Ceturegel™?
2. Какова роль базальной мембранной матрицы Ceturegel™?
3. Каковы характеристики матрицы базальной мембраны Ceturegel™?
4. Популярное применение матрицы базальной мембраны Ceturegel™
5. Часто задаваемые вопросы
6. Руководство по выбору базальной мембранной матрицы Ceturegel™ от Yeasen
1. Что такое базальная мембранная матрица Ceturegel™?
Матрикс, прилегающий к эндотелиальным клеткам, эпителиальным клеткам, мышечным и нейрональным клеткам, образует непрерывный, слоистый внеклеточный матрикс, называемый базальной мембраной. Базальная мембрана дегенерирует и регенерирует в процессе развития и заживления ран. Она не только поддерживает клетки и клеточные слои, но и играет важную роль в формировании тканей, влияя на адгезию, миграцию, пролиферацию и дифференциацию клеток, которые являются функциями базальной мембраны. Поэтому можно сказать, что базальная мембрана является основным барьером для инвазии метастатических опухолевых клеток.
Рисунок 1. Матрица базальной мембраны Ceturegel™
Базальная мембранная матрица Ceturegel™, разработанная и произведенная YEASEN, не содержит LDEV (вирус, усиливающий лактатдегидрогеназу) и имеет сверхнизкое содержание эндотоксина. И после обнаружения микоплазмы, чтобы гарантировать отсутствие заражения микоплазмой, включая различные типы, такие как базовая концентрация, высокая концентрация и низкий фактор роста.
2. Какова роль базальной мембранной матрицы Ceturegel™?
Базальная мембранная матрица Ceturegel™ может использоваться для приготовления базальных мембранных матриц различных требований. Она может использоваться для исследований клеточной сигнализации, таких как изучение роли факторов роста в формировании почечных канальцев стволовыми клетками почек мышей, исследование экспрессии генов эпителиальных стволовых клеток молочной железы мышей и эксперимент Transwell по инвазивности опухолей. В то же время ее можно использовать для изучения морфологии клеток, биохимической функции, миграции, инфекции и экспрессии генов. Базальная мембранная матрица Ceturegel™ может эффективно помогать прикреплению и дифференцировке эпителиальных клеток и других типов клеток, включая нервные клетки, стволовые клетки, эпителиальные клетки млекопитающих, клетки меланомы, сосудистые эндотелиальные клетки, клетки щитовидной железы и клетки волосяных фолликулов. В то же время базальная мембранная матрица Ceturegel™ также влияет на уровень экспрессии белка эпителиальных клеток молочной железы мышей и поддерживает регенерацию периферических нервов.

Рисунок 2.Основные направления применения базальной мембранной матрицы Ceturegel™
Миграция и инвазия клеток в деталях: Миграция клеток, также известная как ползание клеток, движение или перемещение, относится к перемещению клеток после того, как они получают сигнал миграции или чувствуют градиент определенных веществ. Миграция клеток представляет собой чередующийся процесс расширения псевдоподий в головке клетки, установления новых спаек и втягивания хвоста тела клетки. Миграция клеток является одной из основных функций нормальных клеток, а также физиологическим процессом нормального роста и развития организма. Как повсеместная форма перемещения живых клеток, она может участвовать в различных коллективных физиологических и патологических процессах. Таких как эмбриональное развитие, ангиогенез, заживление ран, иммунный ответ, воспалительный ответ, атеросклероз, метастазы рака и т. д. Тогда как инвазия клеток относится к способности клеток мигрировать из одной области в другую через внеклеточный матрикс. Инвазия клеток представляет собой ответ нормальных клеток и раковых клеток на химические и механические стимулы. Инвазия клеток часто происходит в процессах заживления ран, ангиогенеза, воспаления, метастазирования опухолевых клеток и аномальной инфильтрации тканей.
3. Каковы характеристики матрицы базальной мембраны Ceturegel™?
Высокая безопасность: нет LDEV (вирус повышения лактатдегидрогеназы)
Концентрация разнообразия: диапазон концентраций составляет от 8 до 20 мг/мл
Хорошая стабильность партии: строгий процесс контроля качества продукции для обеспечения стабильной производительности между партиями
Низкий уровень эндотоксинов: содержание эндотоксинов <8 ЕЭ/мл
Обнаружение загрязнения: остатков микоплазмы, бактерий и грибков не обнаружено
Высокая производительность единичной партии: выход одной партии превышает уровень 50 л
Совместимость: Совместим с любым типом среды для культивирования клеток
4. Популярное применение матрицы базальной мембраны Ceturegel™
4.1 Анализ миграции и инвазии
Экспериментальным методом определения способности клеток к миграции и инвазии является эксперимент Transwell, а Transwell также называется экспериментом по перфорации. Сначала в камеру добавляется клеточная суспензия, поскольку камера имеет плотные поры. Затем камеры помещаются в 24-луночный планшет, в который добавляется полная среда. Клетки деформируются и проходят через отверстия в камере наружу из более богатой питательными веществами камеры, где они прилипают к внешней стороне. Окрашивая и подсчитывая клетки снаружи камеры, можно судить о способности клеток к миграции и инвазии. Принцип Transwell заключается в том, чтобы поместить маленькую камеру в культуральный планшет, маленькая камера называется верхней камерой, а культуральный планшет называется нижней камерой. Верхний и нижний слои культуральной жидкости разделяются поликарбонатной мембраной, верхний слой культуральной жидкости добавляется в верхнюю камеру, а нижний слой культуральной жидкости добавляется в нижнюю камеру. Клетки находятся в верхней камере, и состав нижней среды будет влиять на клетки в верхней камере из-за проницаемости мембраны. Кроме того, было исследовано влияние компонентов нижней среды на рост и движение клеток.
Конкретные операции с базальной мембранной матрицей Ceturegel™ в анализах миграции и инвазии: Разбавленная базальная мембранная матрица Ceturegel™ была добавлена в верхнюю камеру Transwell, а клетки были высеяны и инкубированы при температуре 37°C, 5% CO2.2 инкубатор на 24 часа, фиксированный в 4% параформальдегиде и окрашенный 0,1% раствором кристаллического фиолетового. Клетки наблюдались и подсчитывались под инвертированным фазово-контрастным микроскопом.
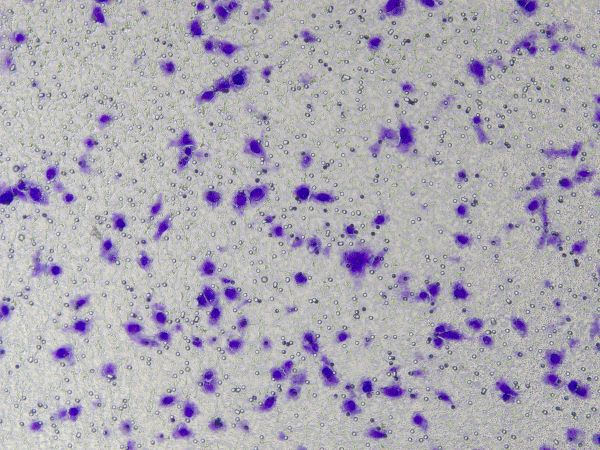
Рисунок 3. Результаты окрашивания кристаллическим фиолетовым после инвазии клеток.
4.2 Ангиогенез
1) За день до эксперимента достаньте Цетурегель™. Достаньте Матригель из морозильника и поместите его на ночь в холодильник при температуре 4°C для размораживания, предварительно охладив использованные расходные материалы.
2) Всегда храните Ceturegel™ Matrigel в холодильнике перед экспериментом. Откройте стерильную упаковку ангиогенных слайдов и извлеките слайды.
3) Добавьте 10 мкл Ceturegel™ Matrigel в каждую лунку. Обратите внимание, что кончик пипетки должен быть перпендикулярен верхней части внутреннего отверстия при добавлении Ceturegel™ Matrigel, чтобы предотвратить вытекание Matrigel через верхнее отверстие и оставление остатков клея.
4) Сначала накройте предметное стекло, подготовьте чашку Петри диаметром 10 см и положите туда бумажные полотенца, смоченные водой, чтобы получилась влажная коробка.
5) Положите слайды в чашку Петри и накройте чашку Петри. Поставьте ее в CO2.2 инкубатор, дайте постоять около 30 минут, дождитесь коагуляции геля и одновременно приготовьте клеточную суспензию.
6) Подготовьте переваренные клетки в клеточную суспензию плотностью 2*105 клеток/мл и тщательно перемешать.
7) Удалите предметное стекло, содержащее кровеносный сосуд, затвердевший в гель. Добавьте 50 мкл клеточной суспензии в каждую лунку, следя за тем, чтобы кончик пипетки находился вертикально над верхней лункой и не касался геля в нижней лунке.
8) Добавьте среду для культивирования клеток, закройте крышку и дайте постоять. Через некоторое время все клетки опустятся на поверхность Матригеля.
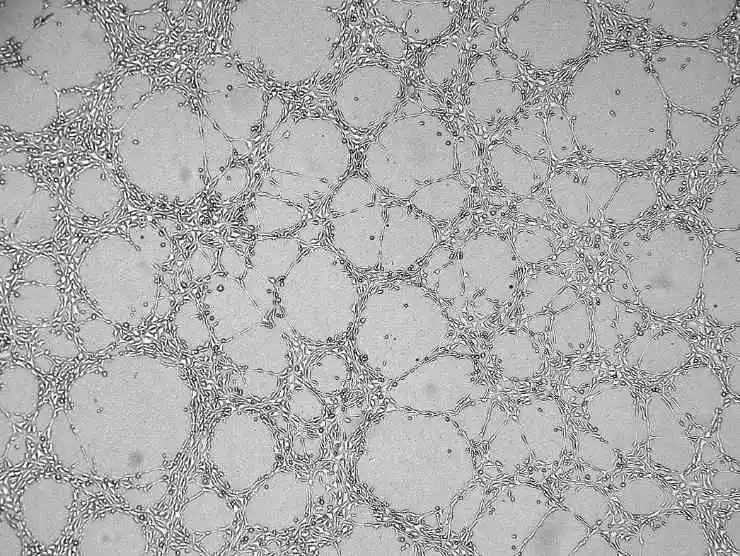
Рисунок 4. График результатов ангиогенеза
Иммунофлуоресцентное окрашивание
1) Осторожно удалите среду из лунок, не касаясь клея или клеточной сети. Разведите кальцеин в среде без сыворотки до конечной концентрации 6–8 мкг/мл. Добавьте раствор для окрашивания клеток, чтобы полностью покрыть клетки, и инкубируйте при комнатной температуре в течение 30–40 минут в темноте.
2) Промыть три раза PBS. Обратите внимание, что PBS следует добавлять в верхние лунки медленно, чтобы не повредить клетки. Наблюдение за флуоресценцией с использованием длины волны Ex=485 нм, Em=529 нм
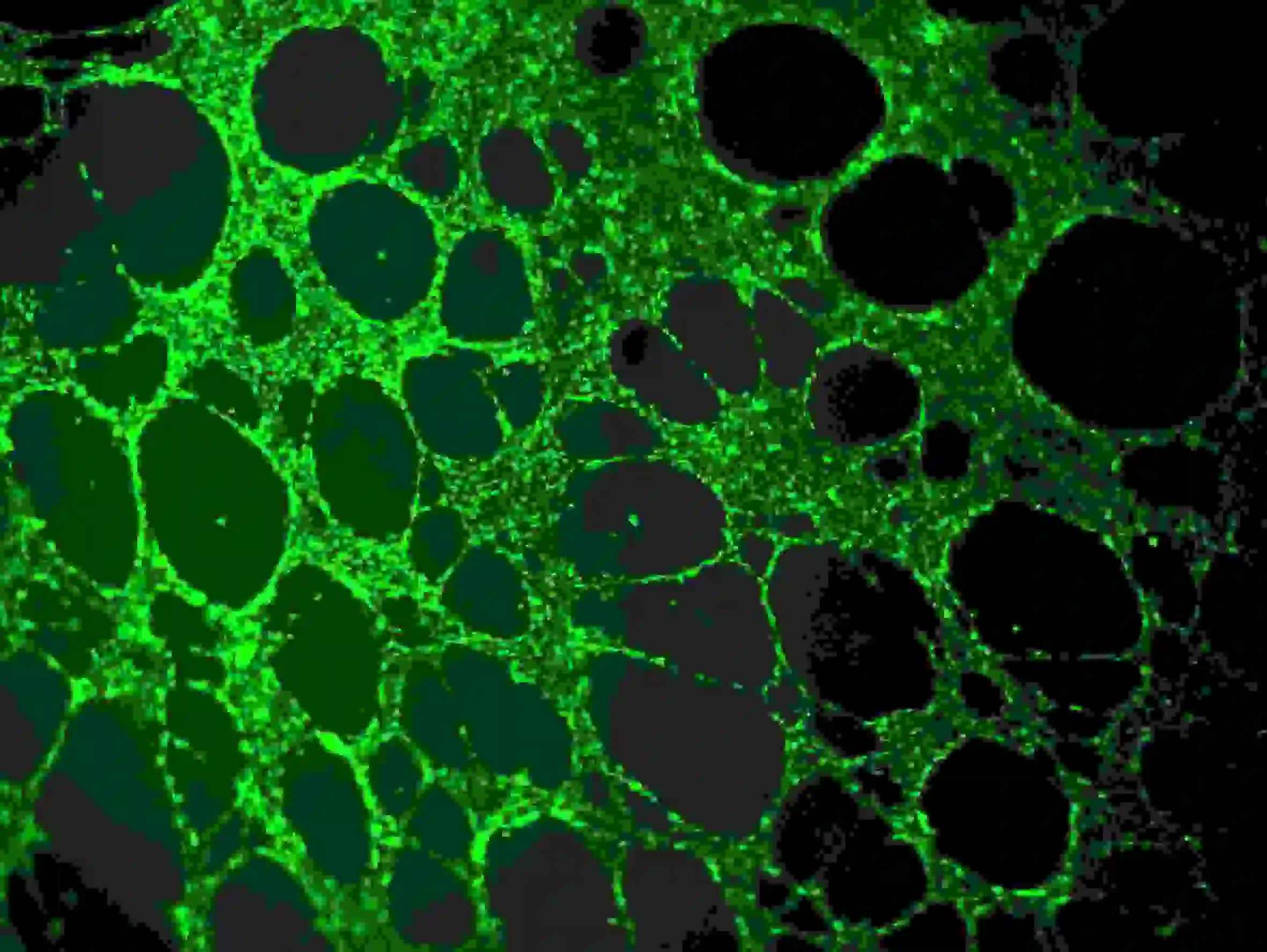
Рисунок 5. Иммунофлуоресцентное окрашивание кровеносных сосудов.
4.3 3D-культура клеток
В отличие от традиционной клеточной культуры, 3D-культура клеток воспроизводит среду клеток in vivo. Даже простые сфероидные модели могут компенсировать недостатки монослойных культур. Эти структуры могут образовывать градиенты кислорода, питательных веществ, метаболитов и растворимых сигналов, которые, в свою очередь, формируют разнообразные популяции клеток. Технология 3D-культуры клеток может лучше имитировать естественную среду, в которой клетки живут в организмах, делая взаимодействия между клетками и биохимические и физиологические реакции более реалистичными. В 3D-среде реакции клеток на эндогенные и экзогенные стимулы более близки к их реакциям in vivo.
Конкретная работа базальной мембранной матрицы Ceturegel™ в 3D-культуре клеток выглядит следующим образом: осторожно смешайте базальную мембранную матрицу Ceturegel™ с отрегулированной концентрацией суспензии отдельных клеток HepG2 в соотношении 1:1 и добавьте 50 мкл смешанной выше суспензии отдельных клеток в предварительно охлажденный 24-луночный планшет с помощью предварительно охлажденного наконечника пипетки для формирования дугообразных клеточных капель, которые культивировали в инкубаторе при температуре 37 °C и 5 % CO2, наблюдая и фотографируя каждый день.
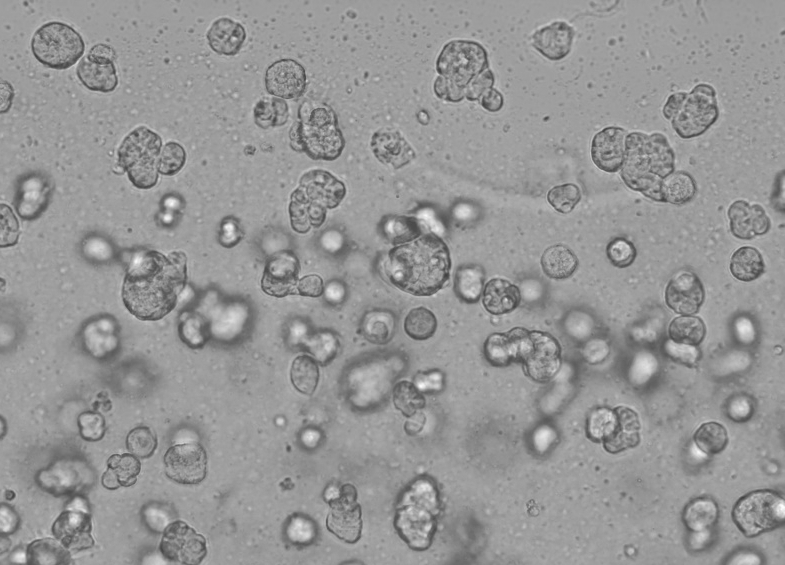
Рисунок 6. Результаты 3D-культивирования клеток
Таблица 1. Матрица базальной мембраны Ceturegel™ 3D Cell Culture. Ссылка на использование:
| Тип культуральной пластины (чашки) | Площадь клеточной культуры (см2) | Измерение расхода (концентрация ≥ 3 мг/мл)* |
|---|---|---|
| 6-луночный планшет | 9.6 | 200 мкл/см2 |
| 12-луночный планшет | 4.5 | 180 мкл/см2 |
| 24-луночный планшет | 2.0 | 180 мкл/см2 |
| 96-луночный планшет | 0,32 | 160 мкл/см2 |
| 35мм блюдо | 11.78 | 200 мкл/см2 |
| 100мм блюдо | 58.95 | 200 мкл/см2 |
Примечание: разные партии базальной мембранной матрицы Ceturegel™ имеют определенную разницу в концентрации, рекомендуемая дозировка приведена только для справки.
4.4 Эксперимент по формированию опухолей in vivo
Взяв в качестве примера эксперимент по подкожному опухолеобразованию клеток HepG2 у голых мышей, матрица базальной мембраны Ceturegel™ и клеточная суспензия были использованы для разведения 1:1, и самки мышей BALB/c-nu в возрасте 4-5 недель были инокулированы подкожно. Экспериментальный процесс выглядит следующим образом:
♦ Подготовьте клетки HepG2 с логарифмическим ростом и плотностью клеток около 80–90 % и замените свежую среду накануне сбора клеток.
♦ Клетки перевариваются трипсином. Когда клетки становятся круглыми и не покидают чашку для культивирования, трипсин удаляют, добавляют среду без сыворотки для приготовления клеточной суспензии, центрифугируют и очищают один раз, и конечная концентрация составляет 5 × 107 клеток/мл.
♦ Разбавьте клеточную суспензию и базальную мембранную матрицу Ceturegel™ в соотношении 1:1 при температуре 4 ℃, чтобы получить конечную концентрацию 5 × 107 клеток/мл.
♦ Возьмите фиксированную голую мышь левой рукой и сделайте ей подкожную инъекцию в правое плечо голой мыши. Во время инокуляции игла вводится подкожно немного глубже, примерно на 1 см, чтобы уменьшить перелив клеточной суспензии из ушка иглы после инъекции.
Объем инокуляции составляет 200 мкл. (Этот процесс следует завершить в течение получаса, насколько это возможно. По пути клеточную суспензию следует поместить на лед, чтобы замедлить апоптоз клеток и предотвратить явление геля).
♦ Поместите голых мышей обратно в клетку для продолжения кормления, и опухоль можно будет наблюдать в течение примерно от 1 недели до 1 месяца.Согласно экспериментальному плану, голых мышей следует умертвить, когда объем опухоли достигнет требуемого уровня, и сделать фотографии.
Примечание: Контрольная группа представляет собой суспензию культуральной среды и клеток, а конечная плотность такая же, как и у тестовой группы с матричным клеем.
4.5 Культура органоидов
Органоиды — это трехмерные многоклеточные крошечные ткани, дифференцированные от стволовых клеток. Некоторые свойства органов могут быть воспроизведены. Органоиды многоклеточные и демонстрируют высокую степень самосборки, и поэтому лучше способны демонстрировать сложные клеточные реакции и взаимодействия in vivo, чем традиционные двумерные культуры. Стволовые клетки и/или клетки-предшественники органов из нормальной или больной ткани можно смешивать с базальной мембранной матрицей Ceturegel™ или коллагеном. Образуют почки, щитовидную железу, печень, мозг, легкие, кишечник, простату и другие микроорганизмы. Например, для исследователей, проводящих генетические скрининги, субстраты базальной мембранной матрицы Ceturegel™ могут использоваться в качестве биочернил для обеспечения точной локализации и внедрения живых клеток/органоидов в трехмерную биопечать.
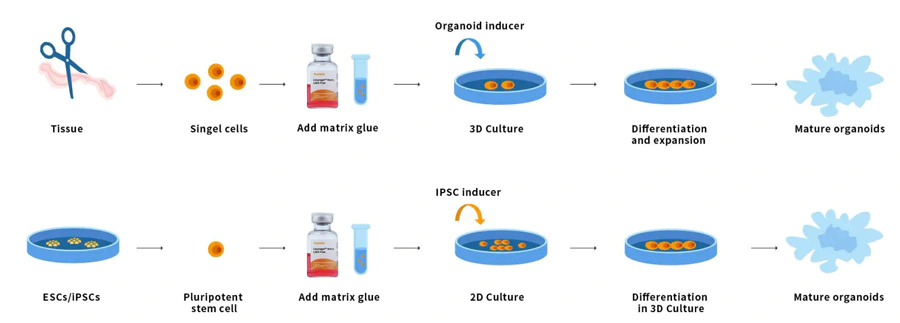
Рисунок 7. Процесс работы органоида
Строение органоида тонкого кишечника мыши
Подготовка образца: Мышей умерщвляли, перерезая им шеи, и поверхность опрыскивали спиртом для стерилизации. Вырезайте кишечную ткань на расстоянии 3~15 см от желудочного конца в стерильной среде, осторожно удаляйте брыжейку и жир снаружи кишечного тракта пинцетом и помещайте ее в раствор DPBS, содержащий 1% двойных антител, предварительно охлажденный до 4 ℃.
Очистка образца: промойте кишечный тракт шприцем 2–3 раза, хирургическими ножницами осторожно разрежьте кишечный тракт так, чтобы кишечная полость была обращена вверх, и хирургическим лезвием осторожно соскоблите кишечные ворсинки с поверхности кишечной полости. После того, как кишечные ворсинки будут соскоблены (будет видна прозрачная ткань), поместите кишечную ткань в новую культуральную чашку, содержащую DPBS, на 2–3 раза.
Первичная обработка образцов: нарежьте промытую тонкую кишечную ткань на небольшие кусочки шириной 2 мм, а затем перенесите их в новую центрифужную пробирку объемом 50 мл. Аккуратно промойте их 3-5 раз с помощью DPBS, чтобы удалить клетки кишечных ворсинок и плавающую жировую ткань.
Образец переваривания: добавьте 10–15 мл предварительно охлажденного DPBS, содержащего 3–5 мМ ЭДТА, к очищенным фрагментам тонкого кишечника для переваривания, инкубируйте при температуре 4 ℃ в течение примерно 30 минут и осторожно встряхивайте центрифужную пробирку каждые 10 минут в течение этого периода.
После переваривания слейте супернатант раствора ЭДТА и осторожно промойте ткани новым буферным раствором DPBS 2–3 раза, чтобы удалить оставшуюся ЭДТА.
Добавьте 10-15 мл предварительно охлажденного DPBS, содержащего 0,1% BSA, в фрагменты тонкой кишечной ткани, продуйте и повторно суспендируйте фрагменты ткани несколько раз, чтобы отделить углубление от базального слоя, затем возьмите немного суспензии для микроскопического исследования. Когда будет видно большое количество структур, похожих на углубления, прекратите продувание и используйте 70% для продутой суспензии ткани μM Filter screen для фильтрации и сбора суспензии ткани, проходящей через фильтр-сетку.
Повторите шаги 5–6 дважды и центрифугируйте при 1500 об/мин и температуре 4 ℃ в течение 3 минут.
Формирование смеси: Ceturegel™ Matrix Glue Heavy Suspension Recession Fabric Precipitation, каждые 10 мкл Matrix Glue Suspension содержат 200~600 Recessions. После ресуспендирования смесь помещают на лед и обрабатывают как можно скорее, чтобы избежать образования геля Matrix Glue.
Примечание: степень разбавления матричного клея ≥ 50% для обеспечения стабильности структуры матричного клея Ceturegel™ в процессе культивирования.
Поместите смешанную суспензию в центр дна 24-луночного планшета, по 30–50 мкл на лунку слева и справа, чтобы избежать контакта суспензии с боковой стенкой пластины с отверстием.
Поместите культивируемый культуральный планшет в инкубатор с постоянной температурой углекислого газа 37 ℃ и инкубируйте в течение примерно 30 минут, пока матричный гель не затвердеет.
Подождите, пока Ceturegel™ полностью затвердеет. После того, как матричный клей полностью затвердеет, медленно добавьте вдоль стенки подготовленную среду для культивирования органов кишечника, по 800 мкл на лунку.
Поместите 24-луночный планшет в инкубатор с углекислым газом при температуре 37 ℃ для культивирования. Заменяйте свежую среду каждые 3 дня и следите за статусом роста органов, подобных органам. Как правило, органы, подобные тонкому кишечнику, у мышей формируются в течение 5-7 дней.
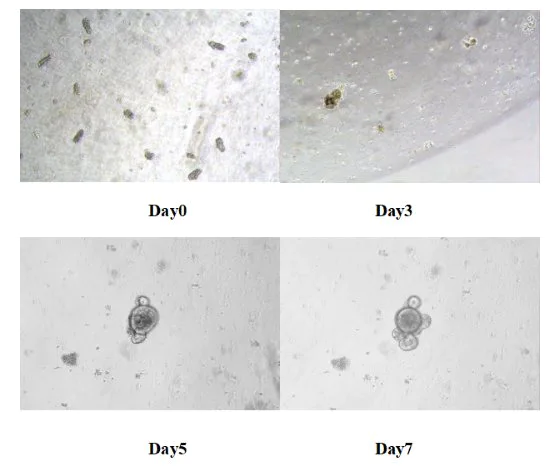
Рисунок 8. Результаты культивирования in vitro органов, подобных тонкому кишечнику мышей.
5. Часто задаваемые вопросы
1. В чем причина разницы в цвете (от светло-желтого до темно-красного) полученного субстрата?
Для базальной мембранной матрицы Ceturegel™, содержащей феноловый красный, это в основном вызвано взаимодействием фенолового красного и бикарбоната с CO2, но разница в цвете уменьшится после уравновешивания с 5% CO2. После замораживания и оттаивания осторожно встряхните флакон, чтобы равномерно распределить матрицу базальной мембраны Ceturegel™.
2. На какие моменты следует обратить внимание при эксплуатации базальной мембранной матрицы Ceturegel™?
Все операции следует выполнять в стерильной среде, а для обеспечения гомогенизации матрицы базальной мембраны Ceturegel™ следует использовать предварительно охлажденную пипетку.
3. Как заморозить и хранить матрицу базальной мембраны Ceturegel™ для использования?
Замороженную и размороженную матрицу Ceturegel™ Matrix LDEV-Free Ceturegel™ можно распределить по нескольким небольшим пробиркам. Все распределения должны быть в предварительно охлажденных криопробирках, которые следует быстро заморозить и хранить, чтобы избежать многократного замораживания и размораживания. Все задействованные предметы следует предварительно охладить перед использованием. Используйте предварительно охлажденные пипетки, наконечники и небольшие пробирки для работы с матрицей Ceturegel™ base membrane.
6. Руководство по выбору базальной мембранной матрицы Ceturegel™ от Yeasen
Различные типы базальной мембранной матрицы Ceturegel™ имеют различные области применения. Стандартные концентрации базальной мембранной матрицы Ceturegel™ могут использоваться для полярных клеточных культур, таких как эпителиальные клетки. Она может способствовать дифференциации различных клеток и использоваться для экспериментов по миграции и инвазии опухолевых клеток. Высокие концентрации базальной мембранной матрицы Ceturegel™ широко используются in vivo и могут использоваться для экспериментов по формированию канальцев. Основная функция низкого фактора роста (СКФ) заключается в устранении помех факторов роста в эксперименте, и она подходит для исследований с высокими требованиями к подготовке базальной мембраны. Базальная мембранная матрица Ceturegel™ без фенолового красного может устранить помехи индикатора фенолового красного и подходит для экспериментов по развитию цвета, таких как колориметрия и обнаружение флуоресценции. Базальная мембранная матрица Ceturegel™ для культуры эмбриональных стволовых клеток человека специально используется для культуры эмбриональных стволовых клеток человека, индуцированной плюрипотентной культуры стволовых клеток без питателя. Yeasen предоставляет множество типов базальной мембранной матрицы Ceturegel™, вы можете выбрать их на основе своих экспериментов.
Таблица 2. Руководство по выбору матрицы Ceturegel™
| Тип продукта | Номер кат. | Название продукта | Матригель Кат. № | Направление применения |
| Базовая концентрация (8-12 мг/мл) | 40183ES | 356234/ 354234 | Адаптирован для экспериментов по культивированию, инвазии и миграции в 2D и 3D, а также может использоваться для экспериментов по канцерогенезу in vivo. | |
| 40184ES | 356237 | В основном используется для обнаружения цвета, например, в экспериментах по обнаружению флуоресценции и т. д. | ||
| Снижение фактора роста
| 40185ES | 354230 | В основном для исключения влияния факторов роста на эксперимент. Применяется для смежных исследований факторов роста, сигнальных путей и т. д. | |
| 40186ES | 356231 | |||
| Высокая концентрация (≥18мг/мл) | 40187ES | 354248 | В основном используется в таких экспериментах, как ангиогенез, эмболизация гелем и формирование опухолей in vivo (для ангиогенеза рекомендуется, чтобы конечная концентрация базальной мембранной матрицы Ceturegel™ составляла ≥10 мг/мл) | |
| 40189ES | Ceturegel™Matrix Высокая концентрация, СКФ, без LDEV | 354263 | ||
| 40188ES | Ceturegel™Matrix Высокая концентрация, без фенольного красного, без LDEV | 354262 | ||
| Для стволовых клеток | 40190ES | Ceturegel™Matrix, сертифицированный для эмбриональных стволовых клеток человека, без LDEV | 354277 | В основном используется для культивирования стволовых клеток, таких как эмбриональные стволовые клетки человека (hESC), плюрипотентные ... стволовые клетки (iPSC) и т. д. |
| Органоид-специфический | 40191ES | Матрица Ceturegel™ для культивирования органоидов, без фенолового красного, без LDEV | 356255 | Матрица базальной мембраны Ceturegel™ для органоидной культуры |
