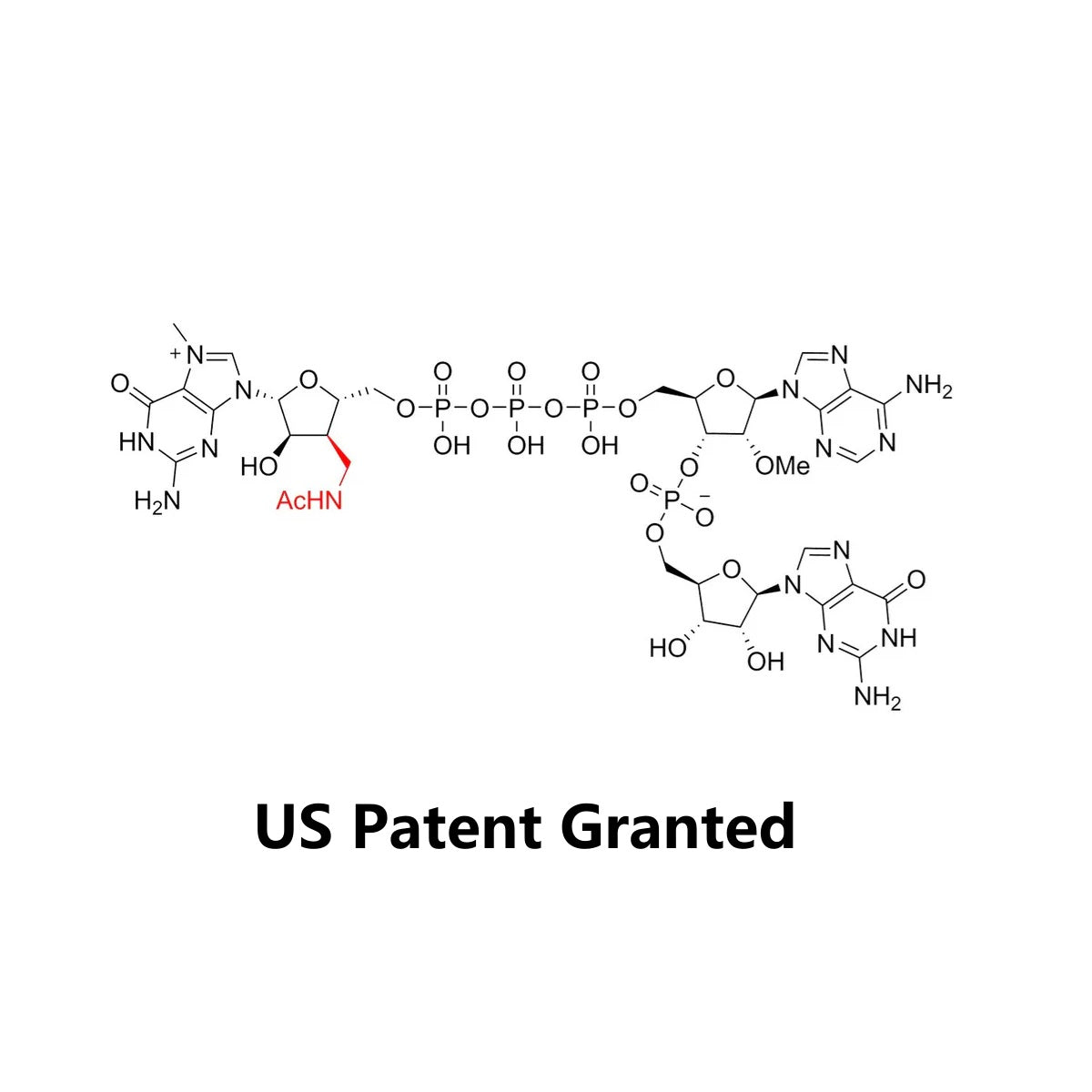
Description
Cap AG (3'Acm) est un analogue de cap avec la structure de m7(3'AcmG)(5')ppp(5')(2'0MeA)pG, sa formule moléculaire est C35H48N16O24P4 et le poids moléculaire est 1200,75Le produit est utilisé pour la transcription avec la séquence initiale de 5'AG3', et la structure naturelle cap1 est produite par le capping de transcription Cap1. Par rapport au Cap0 produit par la méthode de capping traditionnelle, la structure cap1 produite par CapAG (3'Acm) permet à l'ARNm d'avoir une activité et une efficacité de traduction plus élevées in vivo.
Fonctionnalité
Comparé aux produits existants comme CleanCap, ce produit est un 3'Acm Analogue de capuchon d'ARNm modifié. Sa structure à double liaison améliore la stabilité moléculaire, ce qui le rend résistant à la reconnaissance et à l'hydrolyse par les nucléases. Avec le 3'Acm, il stabilise efficacement la structure de la coiffe 5', améliorant la capacité de liaison de l'ARNm avec le facteur d'initiation eucaryote (eIF4E) et améliorant ainsi l'efficacité de la traduction de l'ARNm. De plus, ce type d'analogue de coiffe présente des données prometteuses en termes de rendement de transcription in vitro et d'efficacité de coiffage.
Composants
| N° de chat. | Nom | Taille |
| 10684 | LZCap AG (3'Acm) (100 mM) | 100 μL |
| 1 ml |
Détails du produit
| Formule moléculaire | C35H48N16O24P4 (Acide libre) |
| Poids moléculaire | 1200,75 (acide libre) |
| Concentration | 100± 3 mM |
| Pureté | HPLC ≥ 95 % |
Chiffre

Figure 1. L'analogue de LZCap a montré une affinité plus forte pour les facteurs d'initiation de la traduction eIF4E, permettant une initiation plus efficace de la traduction de l'ARNm. Plus la valeur Kd est faible, plus l'affinité de l'analogue de la coiffe pour la protéine de liaison à la coiffe eIF4E est forte.
Figure 2. L'expression in vivo de l'ARNm coiffé de LZCap AG est beaucoup plus élevée que celle de l'analogue de la coiffe 3'OMe.

Figure 3. Les ARNm coiffés de LZCap sont plus résistants à l'enzyme de décapsulage. Plus la valeur de la CI50 est élevée, plus la capacité de l'analogue de la coiffe à résister au clivage par l'enzyme de décapsulage est forte
Figure 4. ARNm coiffé de LZCap réduit l'ARN stimulé par un seul ARN niveau de transcription du facteur immunitaire dans la cellule THP-1.
Profil de sécurité générale
| Résultat et Conclusion | |
| Cytotoxicité Test | Non cytotoxicité était observé avec le modifié nucléoside dans multiple cellule lignes |
| Polymérase Inhibition Étude | Le modifié nucléoside est ni l'un ni l'autre un inhibiteur ni un substrat de humain ARN et ADN polymérases et est donc pas intégré dans le génome |
| Amès Test* | Non génotoxicité était observé dans le Amès test |
Stockage
Ce produit peut être stocké à -25~-15 ℃ pendant deux ans.
Précautions
- Pour votre sécurité et votre santé, veuillez porter un équipement de protection individuelle (EPI), tel que des blouses de laboratoire et des gants jetables, lorsque vous utilisez ce produit.
- À usage de recherche uniquement.
Questions et réponses
1. Comment concevez-vous le LZCap ?
Les enzymes ont une reconnaissance relativement « spécifique » des substrats. Par conséquent, lors de la conception d'une nouvelle structure de coiffe, d'une part, nous avons besoin de nouvelles modifications structurelles à des fins de brevet, mais d'autre part, nous nous efforçons de maintenir autant que possible la similitude avec les structures naturelles/connues. La structure naturelle a un ribose 3' OH, qui peut être modifié (par exemple, méthylation). Sur la base de cette considération, nous avons choisi d'ajouter un carbone en position 3' pour la nouveauté du brevet, suivi d'un NH pour imiter la liaison hydrogène de OH, puis d'un groupe acétyle pour réduire la basicité de NH et améliorer sa capacité de liaison hydrogène. LzCap est meilleur que le méthylatecasquette naturelle ed, probablement en raison d'une augmentation des liaisons hydrogène. Comparé aux groupes méthyle et méthoxy, le groupe amino acétyl peut également augmenter les interactions de van der Waals entre le substrat (cap) et le facteur initiateur (enzyme).
2. Le groupe amino acétyl est-il stable ?
Le groupe amino acétyl est déjà suffisamment stable. Il est beaucoup plus stable que la position 7-méthylée et la liaison phosphodiester, qui sont les parties les moins stables de la coiffe.
Publication
- Les vaccins à ARNm polyvalents mpox suscitent des réponses immunitaires robustes et confèrent une protection puissante contre le virus de la vaccine, 2024, Cell Reports 43,114269
- Étude préliminaire de l'efficacité et de la durée d'un agoniste GLP-1R à base d'ARNm chez les singes diabétiques.2024, Diabète, 73
Limité Utiliser Déclaration de licenceent
Veuillez nous contacter pour plus de détails sur la licence LZCap.
Paiement et sécurité
Vos informations de paiement sont traitées en toute sécurité. Nous ne stockons pas les détails de la carte de crédit ni accès aux informations de votre carte de crédit.
Enquête
Vous pouvez aussi aimer
FAQ
Le produit est destiné à des fins de recherche uniquement et n'est pas destiné à un usage thérapeutique ou diagnostique chez l'homme ou l'animal. Les produits et le contenu sont protégés par des brevets, des marques déposées et des droits d'auteur appartenant à Yeasen Biotechnology. Les symboles de marque indiquent le pays d'origine, pas nécessairement l'enregistrement dans toutes les régions.
Certaines applications peuvent nécessiter des droits de propriété intellectuelle tiers supplémentaires.
Yeasen se consacre à la science éthique, estimant que nos recherches doivent répondre à des questions cruciales tout en garantissant la sécurité et les normes éthiques.