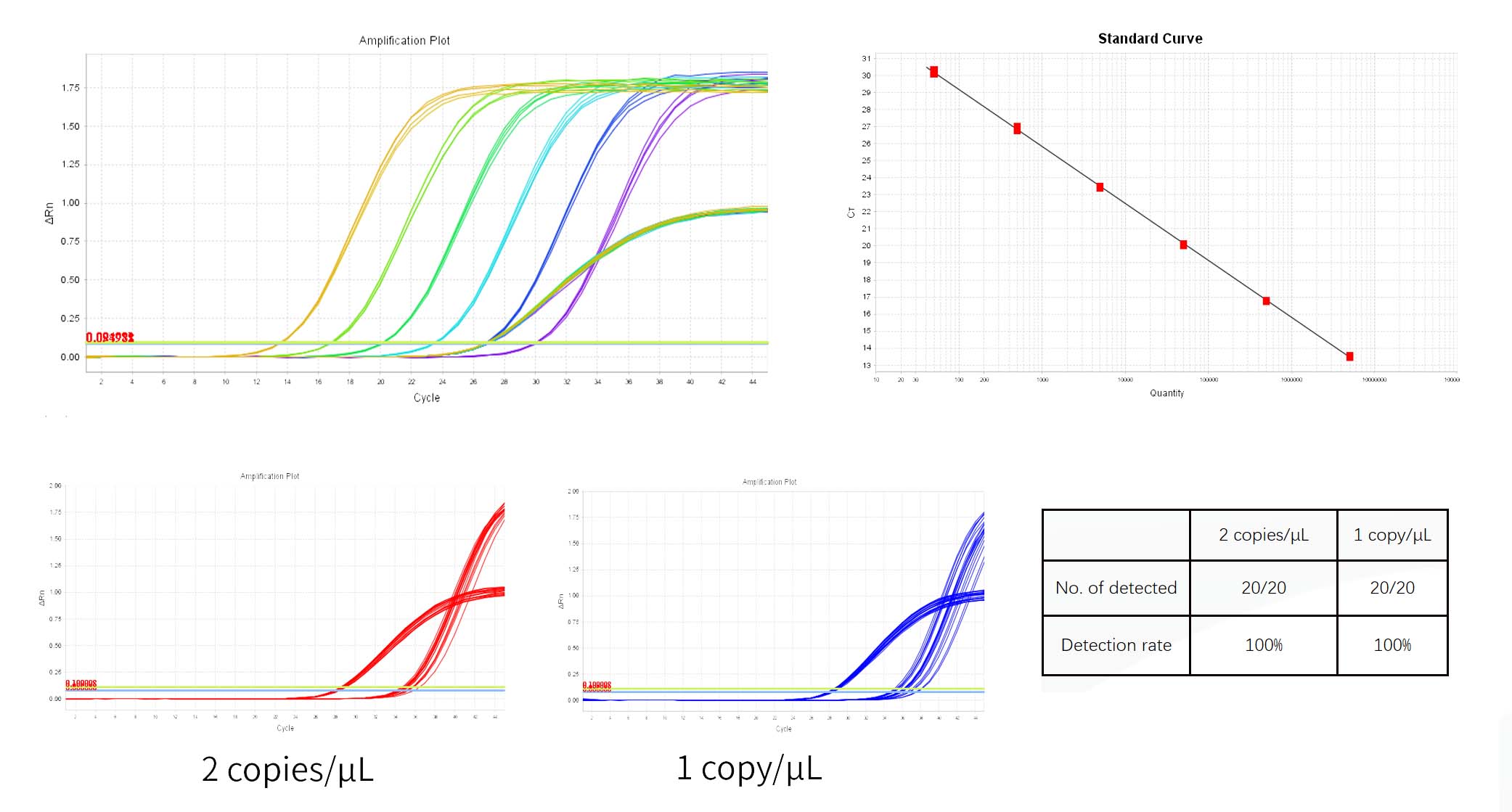
描述
使用複製型慢病毒 (RCL) 檢測試劑盒 定量檢測複製慢病毒 可能發生在 與慢病毒相關的多種細胞產品 矢量的潛在風險。
該試劑盒設計了特定的引子 慢病毒包膜蛋白的VSV-G基因序列。 它採用taqman 螢光探針和聚合酶鍊式反應(PCR)方法,其檢測極限為1拷貝/μL級, 可以特異性、快速地檢測 具有複製能力的慢病毒風險。該套件需要 一起使用 殘留 DNA 樣本製備試劑盒(Cat# 18461ES)。
成分
| 零件編號 | 姓名 | 41311ES50 | 41311ES60 |
| 41311-A | RCL qPCR 混合物 | 0.75 毫升 | 1.5 毫升 |
| 41311-B | RCL 引子和探針混合物 | 200 微升 | 400 微升 |
| 41311-C | DNA稀釋 緩衝 | 2×1.8毫升 | 4×1.8毫升 |
| 41311-D | RCL DNA對照(5×10E8 份/μL) | 二十五 微升 | 50 微升 |
| 41311-E | 我知道了* | 50 微升 | 100 微升 |
* 我知道了: 內部的 控制。
貯存
本產品應儲存於-25~-15℃ 2 人份 年。
41311-A 和 41311-B 均應避光保存。
適用的 樂器 模型
包括但不限於: Bio-Rad:CFX96 光學模組;熱電科技: ABI 7500; ABI Quant Studio 5; ABI 步驟 OnePlus。
指示
- 克隆的DNA 標準 稀釋 和 標準 曲線 準備
使用試劑盒中提供的 DNA 稀釋緩衝液對 RCL DNA 對照進行梯度稀釋* 以及稀釋 濃度為5×10E7 拷貝/μL,5×10E6 拷貝/μL,5×10E5 拷貝/μL,5×10E4 拷貝/μL,5×10E3 拷貝/μL,5×10E2 拷貝/μL, 5×10E1 份/μL。
請參閱下面的詳細說明:
1) 在冰上解凍 RCL DNA 對照和 DNA 稀釋緩衝液。 完全解凍後, 輕輕旋渦 混合,然後 低速離心 10 秒鐘。
2) 取出七隻乾淨的 1.5 mL 管,標示為 Std0、Std1、Std2、Std3、Std4、Std5、Std6。
3) 添加 90 μL DNA 稀釋緩衝液和 10 將 μL RCL DNA 對照加入標示 Std0 的 1.5 mL 微量離心管中, 即 稀釋至 5×10E7 份/μL。混合並 然後離心 10 秒鐘。分裝稀釋的DNA標準品,即可 短期儲存(不超過3個月)於-25~-15℃** .請避免反覆凍融。
4) 添加 90 μL DNA 稀釋緩衝液倒入其他管中*** ,然後按照以下步驟操作 連續稀釋**** 。
| 管子 | 稀釋比例 | 標準濃度 |
| 標準1 | 10 μL Std0 + 90 μL DNA 稀釋液 緩衝 | 5×10E6 份/微升 |
| 標準2 | 10 μL 標準品 1 + 90 μL DNA 稀釋 緩衝 | 5×10E5 份/微升 |
| 標準3 | 10 μL 標準2 + 90 μL DNA 稀釋 緩衝 | 5×10E4 份/微升 |
| 標準4 | 10 μL Std3 + 90 μL DNA 稀釋液 緩衝 | 5×10E3 份/微升 |
| 標準5 | 10 μL 標準4 + 90 μL DNA 稀釋 緩衝 | 5×10E2 份/微升 |
| 標準6 | 10 μL 標準5 + 90 μL DNA 稀釋 緩衝 | 5×10E1 份/微升 |
表1 標準梯度稀釋
*三 複製 井 是 必需的 為了 每個 濃度 偵測 範圍 是 5×10E1 拷貝/μL~5×10E6 份/微升 和 這 範圍 能 是 如果需要的話可以擴充。
** 到 減少 這 數位 的 重複 凍融 和 避免 污染,它 是 受到推崇的 到 店鋪 這 脫氧核糖核酸 控制 在 等分試樣 在 -25~-15℃ 為了 這 第一的 時間。
*** 一次 解凍, 脫氧核糖核酸 稀釋 緩衝 可以 是 儲存 在 2-8℃ 為了 7 天,如果 不是 用過的 為了 一個 長的 請給時間 店鋪 在 -25~-15℃ 。
**** 製作 當然 這 範本 是 完全地 混合,輕輕地 搖 這 混合物 為了 15 秒 到 1 分鐘 為了 每個 坡度 稀釋。
- 萃取回收 控制 (環境責任委員會) 準備
根據需要設定 ERC 中 RCL DNA 的濃度(ERC 樣品以 5×10E4 將 RCL DNA 複製為 舉例來說),如下:
1) 新增 100 μL 測試樣品放入乾淨的 1.5 mL 管中,然後加入 10 微升 5×10E3 拷貝/μL RCL DNA 標準 (Std4) 和 混合均勻,標記為ERC。
2) 將ERC樣本的DNA萃取與測試樣本一起進行,製備純化的ERC樣本。
- 陰性對照 解決方案 (國家癌症中心) 準備
實驗中設定陰性對照,具體操作步驟如下:
1) 新增 100 μL 樣本基質(或 DNA 稀釋緩衝液)倒入乾淨的 1.5 mL 管中,然後標記為 NCS。
2) 進行 NCS 的 DNA 萃取 樣品與測試樣品一起製備純化的NCS 樣本。
- 無模板 控制 (NTC) 準備
實驗中設置無模板對照,具體操作步驟如下:
1)NTC無需樣品預處理,可在qPCR檢測殘留DNA的階段進行配置 內容。
2)每管或每孔中NTC樣品20 μL 混合液(即 15 μL RCL qPCR 混合物 + 4 微升 雷諾公司 引子和探針 混合 + 1 μL IC)+ 10 μL DNA稀釋緩衝液。建議配置三個重複孔。
- 聚合酶連鎖反應 反應 系統
| 成分 | 容量(μL) |
| RCL qPCR 混合物* | 15 |
| RCL 引子和探針混合物 | 4 |
| 我知道了 | 1 |
| DNA模板 | 10 |
| 全部的 體積** | 三十 |
表2 反應體系
* 計算 這 全部的 聚合酶連鎖反應 反應 體積 經過 這 數位 的 反應:qPCR 混合 =( 數位 的 反應+2) × (15+4+1) μL(含 這 損失 兩個反應孔)。建議實驗中每個樣品重複三次以上。
** 後 封蓋 這 管子 或者 密封 這 板、離心機 這 反應 管子 或者 盤子 在 低的 速度 為了 10秒。後 充足的 搖晃 和 混合 為了 5秒,重複 離心機 到 收集 這 液體 從 這 蓋 或者 牆 到 這 底部。避免 氣泡 期間 手術。
請參閱下表以了解建議的板材設定:
|
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 |
| 一個 | 負溫度係數 (NTC) |
| TS 1 | TS 1 | TS 1 |
| 標準 1 | 標準 1 | 標準 1 |
|
|
|
| 乙 | 負溫度係數 (NTC) |
| TS 2 | TS 2 | TS 2 |
| 標準 2 | 標準 2 | 標準 2 |
|
|
|
| 碳 | 負溫度係數 (NTC) |
| TS 3 | TS 3 | TS 3 |
| 標準 3 | 標準 3 | 標準 3 |
|
|
|
| 德 |
|
|
|
|
|
| 標準 4 | 標準 4 | 標準 4 |
|
|
|
| 埃 | 國家電腦系統公司 |
| 緊急應變委員會 1 | 緊急應變委員會 1 | 緊急應變委員會 1 |
| 標準 5 | 標準 5 | 標準 5 |
|
|
|
| 弗 | 國家電腦系統公司 |
| ERC 2 | ERC 2 | ERC 2 |
| 標準 6 | 標準 6 | 標準 6 |
|
|
|
| 格 | 國家電腦系統公司 |
| ERC 3 | ERC 3 | ERC 3 |
|
|
|
|
|
|
|
| 赫 |
|
|
|
|
|
|
|
|
|
|
|
|
表3 計算機開機 參考 木板
板佈局包括:6 個 Std(6 個標準濃度的標準曲線)、1 個 NTC(無模板對照)、1 NCS(陰性對照溶液)、3TS(測試樣本)、3ERC(萃取回收對照)。三個重複孔 每個樣本。
- 設定指南 為了 一個 聚合酶連鎖反應 樂器
以下說明僅適用於 熱 ABI 7500 qPCR 儀器(軟體 版本2.0)。如果 你使用 不同的儀器,請參閱適用的儀器指南以了解設定指南。
1)產生新實驗,選擇絕對定量模板或 用戶定義。
2) 創建1個檢測探針,命名為“RCL-DNA”,選擇報告螢光團為“FAM”,淬滅螢光團為 “沒有任何”;建立 1 個檢測探針,命名為“IC”,選擇報告螢光團為“CY5”,然後淬滅 螢光團為「無」。 參考螢光為ROX」(參考螢光可以基於 儀器型號等,選擇 無論 您需要添加它)。
3)在 ‘Samples’窗格,依序加入所有samples的資訊。然後選擇孔,選擇目標, 樣品。放 RCL DNA標準的任務作為標準,並分配 值 5000000, 500000, 在 Quantity 欄中分別輸入 50000、5000、500、50(每孔 DNA 濃度單位為拷貝數/μL),並將 分別為孔 Std 1、Std 2、Std 3、Std 4、Std 5 和 Std 6。設定 NTC 作為 NTC 的任務。將 NCS、TS 和 ERC 設定為 未知,並根據上面的板塊佈局相應命名。 然後點擊下一步。
4)設定擴增程序:設定反應體積為30 μL。
| 循環步驟 | 溫度(℃) | 時間 | 週期 |
| 消化系統受污染 | 37℃ | 5 分分鐘 | 1 |
| 初始變性 | 95℃ | 5 分分鐘 | 1 |
| 變性 | 95℃ | 15 秒 |
四十五 |
| 退火/延伸(螢光收集) | 60℃ | 30 秒 |
表4 擴增程序
- 分析 定量PCR 結果
1)系統 將自動給出閾值 擴增圖面板 分析。給定的閾值 系統有時過於接近基線,導致差異很大 重複孔之間的 Ct。 您可以手動調整 將閾值調整到適當位置並點擊 分析。然後你可以初步檢查 多組分圖中擴增曲線是否正常。
2)結果 分析選項卡,查看標準曲線圖。 驗證 R2、效率、斜率和 Y 截距。對於常態標準曲線,R²>0.99,90%≤Eff%≤110%,-3.6≤Slope≤-3.1。
3)在 '看法 好表'窗格中 分析,每個樣品的濃度以數量表示, 單位 為拷貝數/μL,單位可在檢測報告中換算。
4)參數設定 結果分析需要基於具體的模型和軟體 版本 並且通常可以由儀器自動解釋。
5) 根據測試結果計算加標回收率 樣本 TS 待測量和樣品加標 回收率 ERC 需要尖刺 介於50%~150%之間。
回收率 (%) = {Sample spiked assay (eg.copies/μL) - Sample assay (eg.copies/μL)} x 洗脫體積 (μL) / 理論 DNA添加量值(例如拷貝數) x 100%。
6)CT 的價值 陰性對照 NCS 應該大於平均值 最低濃度 Ct 這 標準。
7) 免模板控制NTC 應為未確定或 Ct 值≥38。
筆記
- 本產品僅供研究使用。
- 為了您的安全,請穿著實驗服和戴上一次性手套進行操作。
3.使用前請仔細閱讀本手冊 該試劑和實驗應標準化,包括 樣品處理、反應體系製備和 樣品添加。
4.使用前確保各組分充分渦旋並以低速離心。
付款和安全
您的付款信息已安全處理。我們無法存儲信用卡詳細信息,也無法訪問您的信用卡信息。
詢問
你也可能喜歡
常問問題
本產品僅用於研究目的,不用於人類或動物的治療或診斷用途。產品和內容受以下公司的專利、商標和版權保護:
某些應用程式可能需要額外的第三方智慧財產權。