O kit de reagentes HCP comercial da

Conceito e necessidade de detecção de HCP
Produtos biológicos são tipicamente produzidos usando tecnologia recombinante em células hospedeiras (como bactérias, leveduras, células de mamíferos, insetos ou plantas), incluindo anticorpos monoclonais, proteínas recombinantes e vacinas. Os processos de fabricação e purificação desses produtos inevitavelmente introduzem proteínas de células hospedeiras (HCPs) como impurezas, que incluem proteínas estruturais das células hospedeiras e fatores de crescimento secretados pelas células hospedeiras, formando uma mistura complexa com várias propriedades físico-químicas e imunológicas. Apesar do uso de técnicas avançadas de purificação, algumas proteínas de células hospedeiras ainda podem permanecer como impurezas relacionadas ao processo em produtos farmacêuticos intermediários.
Essas impurezas têm potencial imunogenicidade e podem aumentar a resposta imunogênica de produtos biofarmacêuticos, afetando sua estabilidade e eficácia, apresentando riscos à segurança humana. Portanto, estratégias de monitoramento apropriadas para a remoção de HCPs precisam ser estabelecidas, e o conteúdo de HCPs no produto final precisa ser controlado para atender aos requisitos de qualidade do medicamento.
Requisitos regulamentares para profissionais de saúde
O conteúdo residual de HCPs em produtos biológicos é geralmente considerado um atributo crítico de qualidade (CQA) do produto, um índice de avaliação importante para monitoramento de robustez do processo e um índice de controle de qualidade essencial do produto. Autoridades regulatórias em vários países têm disposições sobre HCPs, exigindo análise e purificação de biofármacos para reduzir HCPs de proteína de célula hospedeira a níveis aceitáveis. O nível de aceitação de HCPs será avaliado com base em circunstâncias específicas e depende de vários fatores, incluindo dose, frequência de dosagem, tipo de medicamento e gravidade da doença.
A Farmacopeia Chinesa (edição de 2020) estipula: Para células CHO, o HCP residual precisa ser <0,05% (equivalente a menos de 500 ppm); para E. coli, o HCP residual precisa ser <0,01%.
O capítulo <1132> da Farmacopeia dos Estados Unidos USP especifica: Um método altamente sensível deve ser usado para detectar HCPs em medicamentos, e o conteúdo deve estar abaixo do limite de detecção (geralmente menos de 100 ppm, ou seja, o conteúdo de HCP em 1 mg de proteína total deve ser menor que 100 ng, ou <0,01%).
A Farmacopeia Europeia EP 2.6.34 especifica: Em produtos biológicos, o conteúdo de HCPs deve ser inferior a 0,1%.
As diretrizes da Conferência Internacional sobre Harmonização de Requisitos Técnicos para Registro de Produtos Farmacêuticos para Uso Humano (ICH): ICH Q6B afirma que métodos sensíveis e validados devem ser adotados para monitorar HCPs residuais, com a quantidade residual normalmente necessária sendo inferior a 100 ppm.
Pode-se ver que as agências reguladoras têm requisitos altamente consistentes para HCPs. O desenvolvimento do processo de produtos biológicos deve passar pela detecção de HCP, demonstrar que o processo de purificação pode reduzir HCPs a níveis seguros, e os limites recomendados para conteúdo residual no produto final estão abaixo de 0,01% tanto na China quanto nos Estados Unidos.
Métodos de detecção de HCP
O Enzyme-Linked Immunosorbent Assay (ELISA) é atualmente o método mais comumente usado para detecção de HCP. Os métodos de detecção de resíduos de proteína hospedeira mencionados nos Capítulos 3412/3413/3414 da edição de 2020 da Farmacopeia Chinesa são todos métodos ELISA.
O capítulo <1132> da Farmacopeia dos Estados Unidos USP também menciona que métodos como eletroforese, ELISA e LC-MS/MS podem ser usados para detectar conteúdo de HCP, e ELISA é recomendado como o método preferido para detecção de HCP devido à sua facilidade de operação, velocidade, alta sensibilidade e alto rendimento.
ELISA:
Propósito: Detecta a quantidade total de proteínas em HCPs, pode ser usado para desenvolvimento de produtos e controle de processos e atualmente é um método comum para detecção de HCPs.
Vantagens: Alta sensibilidade e especificidade; Alto rendimento e capacidade de automação; Quantitativo; Operação fácil e rápida.
Desvantagens: Requer anticorpos específicos; Não é possível identificar e avaliar especificamente HCPs individuais; O desenvolvimento do método é complexo, exigindo preparação especial de antígenos; Muitos fatores de influência para o método, a cobertura de HCP precisa ser avaliada; Não é possível identificar espécies.

Western Blotting:
Propósito: Usado para triagem consistente de grandes números de amostras e detecção de proteínas desconhecidas que reagem com anticorpos anti-HCP. Adequado para detectar HCPs e fornecer informações aproximadas sobre o peso molecular relativo de HCPs.
Vantagens: Especificidade; Os resultados são visualmente intuitivos: visualiza diferenças no tamanho da proteína e nos níveis de expressão; Pode detectar e quantificar HCPs específicos.
Desvantagens: Semiquantitativo; Limitado a proteínas específicas: só pode detectar HCPs ligados a anticorpos; Não é sensível o suficiente para misturas complexas de proteínas; A desnaturação de SDS de proteínas pode levar à perda de epítopos conformacionais; A sensibilidade depende da qualidade dos anticorpos policlonais.
Eletroforese em gel bidimensional (2-DE):

Propósito: Comumente usado para desenvolvimento e caracterização de processos upstream ou downstream, ele pode distinguir diferentes HCPs em um único gel.
Vantagens: Não há necessidade de Western blotting, evitando problemas de transferência; Pode separar vestígios de impurezas de HCP do produto; Fornece informações aproximadas sobre peso molecular relativo e ponto isoelétrico.
Desvantagens: O excesso de proteína pode mascarar manchas de HCP; A distribuição de HCPs na amostra pode ser observada, mas não pode ser quantificada.

Análise de espectrometria de massa:
Propósito: Identifica HCPs individuais, fornecendo informações precisas de identificação e quantificação de proteínas de células hospedeiras.
Vantagens: Alta resolução e precisão; Identifica e monitora HCPs individuais; Fornece espectros abrangentes de HCPs; Pode cobrir uma ampla gama de proteínas; Pode identificar espécies de HCP.
Desvantagens: Altos requisitos técnicos e de equipamento; Operação complexa; Alto custo; Baixo rendimento do método; Pré-tratamento complexo da amostra; Possíveis efeitos de matriz; Requer capacidades especializadas de análise de dados.
ELISA é o método recomendado para detectar HCPs residuais em produtos biológicos por farmacopeias em vários países, capaz de determinar a quantidade total de HCPs. No entanto, ele tem limitações na identificação dos tipos e abundâncias de HCPs e precisa ser suplementado com outros métodos. Cada método de detecção tem suas vantagens e desvantagens e, em aplicações práticas, a seleção pode ser feita com base em propósitos experimentais, características da amostra, precisão e conveniência operacional, entre outros fatores, combinados com o uso de diferentes métodos para obter resultados mais abrangentes e precisos.
Além disso, a Farmacopeia dos Estados Unidos USP <1132> e a Farmacopeia Europeia EP 2.6.34. ENSAIOS DE PROTEÍNA DE CÉLULAS HOSPEDEIRAS indicam que diferentes reagentes ELISA devem ser usados para detecção de HCP em diferentes estágios do desenvolvimento do produto, categorizando os métodos de detecção de HCP em reagentes comerciais, métodos específicos de produto/processo e métodos de plataforma.
A USP <1132> menciona que, na ausência de métodos de plataforma, reagentes comerciais podem ser usados em ensaios clínicos pré-clínicos, de Fase I e de Fase II; em ensaios clínicos de Fase III/validação de processo e produto pós-comercialização, devido a limitações como cobertura insuficiente de anticorpos de reagentes comerciais gerais de detecção de HCP, deve-se considerar fatores como tipo de célula e especificidade do processo, usando métodos de plataforma ou métodos específicos de produto/processo para desenvolvimento de processo upstream.
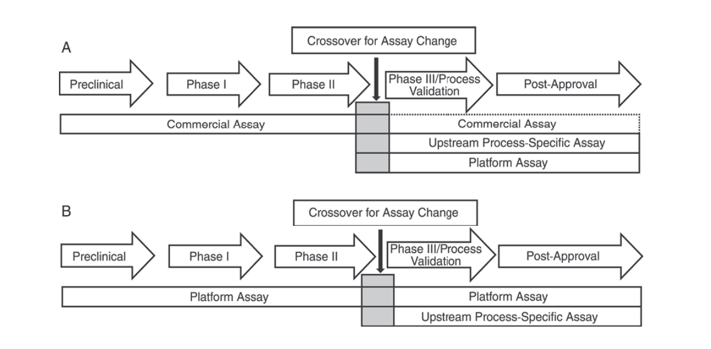
Figura 1. No USP <1132>, diferentes estágios de desenvolvimento do produto são sugeridos para usar métodos específicos para detectar HCPs.
| Método | Kit de reagentes comerciais | Detecção específica de produto/processo Kit | Detecção de plataforma Kit |
| Disponibilidade | Prontamente disponível
| Requer preparação de antígenos, incluindo clonagem de linhas de células hospedeiras
| Requer preparação de antígenos usando linhas celulares de vetores nus ou vazios
|
| Desenvolvimento | Requer preparação mínima | O desenvolvimento da detecção, incluindo a caracterização do antígeno, a imunização e a confirmação, normalmente leva pelo menos 6 meses | O desenvolvimento da detecção, incluindo a caracterização do antígeno, a imunização e a confirmação, normalmente leva pelo menos 9 meses |
| Diversidade | Limitado aos sistemas de expressão mais comuns | Vários tipos de sistemas de expressão podem ser usados | Vários tipos de sistemas de expressão podem ser usados |
| Especificidade | A especificidade pode ser baixa, com potenciais HCPs não detectados
| A especificidade é geralmente aumentada, com cobertura de anticorpos visando padrões HCP específicos | Em comparação com os métodos de detecção comerciais, a especificidade é melhorada, a compreensão do desempenho da detecção é aprimorada e a cobertura dos tipos de HCP também é aumentada |
| Custo | Os preços iniciais são relativamente baratos, mas os custos de desenvolvimento aumentarão rapidamente para todo o processo de purificação a jusante | Os custos iniciais são mais altos, mas o ponto de equilíbrio normalmente está no valor de 100 conjuntos de kits de reagentes | Devido à sua aplicabilidade a múltiplos produtos, apresenta vantagens de custo significativas |
| Dependência | Dependendo de um fornecedor específico, os reagentes e esquemas de controle ficam em um estado de "caixa preta". | Possui controle abrangente sobre todos os reagentes e tampões, podendo ser ajustado a qualquer momento | Tem propriedade e controle completos sobre todos os reagentes, reduzindo riscos na cadeia de suprimentos e na comparabilidade de lotes |
| Requisitos regulamentares | Não é adequado para suporte de marketing pedidos de autorização | Aplicável para dar suporte a todo o processo, desde o desenvolvimento inicial até a comercialização de produtos licenciados | Aplicável para apoiar o desenvolvimento inicial até a autorização de comercialização |
Tabela 1.Comparação de diferentes tipos de kits de reagentes HCP
Serviço de desenvolvimento de ensaios HCP personalizados da Yeasen Biotech
Dada a importância da detecção de HCP,
Linha do tempo de personalização
O serviço de personalização para kits de detecção de proteínas residuais de células hospedeiras normalmente leva de 6 a 10 meses.
Preparação de antígeno-anticorpo: determinar antígenos de HCP, estabelecer padrões de referência para HCP, elaborar vias e estratégias imunológicas, preparar anticorpos para HCP, etc., normalmente leva de 4 a 6 meses.
Desenvolvimento do kit de ensaio: otimização de anticorpos, análise de cobertura, validação do método do kit de ensaio, etc., normalmente leva de 2 a 4 meses.
Yeasen Serviço de verificação de cobertura de anticorpos Biotech HCP
Sabe-se que ELISA é o padrão ouro para detectar HCP residual na indústria, mas a precisão desse método depende da cobertura de anticorpos multiclonais para HCP. A Farmacopeia dos Estados Unidos e a Farmacopeia Europeia mencionam imunopurificação e 2D-WB como métodos recomendados para caracterizar anticorpos ELISA de HCP e sua cobertura.
Cobertura de anticorpos HCP Verificação Serviço
O 2D-WB primeiro separa as proteínas com base no tamanho e na carga usando eletroforese em gel bidimensional e, em seguida, transfere essas proteínas para uma membrana para incubação com anticorpos HCP para detecção de impressão proteica.
Nós possui um conjunto completo de instrumentação 2D-WB e ampla experiência laboratorial para fornecer serviços de verificação de cobertura de anticorpos para amostras de HCP de células hospedeiras, como CHO, E. coli, HEK293, etc.
Produto relacionado:
| Produto | Nº de catálogo. | Tamanho |
| 36712ES | 48T/96T | |
| 36713ES | 48T/96T | |
| Kit CHO HCP ELISA (CHO-K1) | 36714ES | 48T/96T |
| Kit E.coli HCP ELISA (Plasmídeo) | 36721ES | 48T/96T |
