ऑर्गेनोइड्स पर गहन शोध के साथ, बढ़ती संख्या में व्यक्ति इसमें शामिल हो रहे हैं। यह लेख ऑर्गेनोइड्स [1-5] के बारे में कुछ सामान्य ज्ञान बिंदुओं को संक्षेप में प्रस्तुत करता है, जिससे सभी के लिए मददगार होने की उम्मीद है।
प्रश्न: क्या ऑर्गेनोइड्स एक ही प्रकार की कोशिका या बहुकोशिकीय ऊतकों से बने होते हैं?
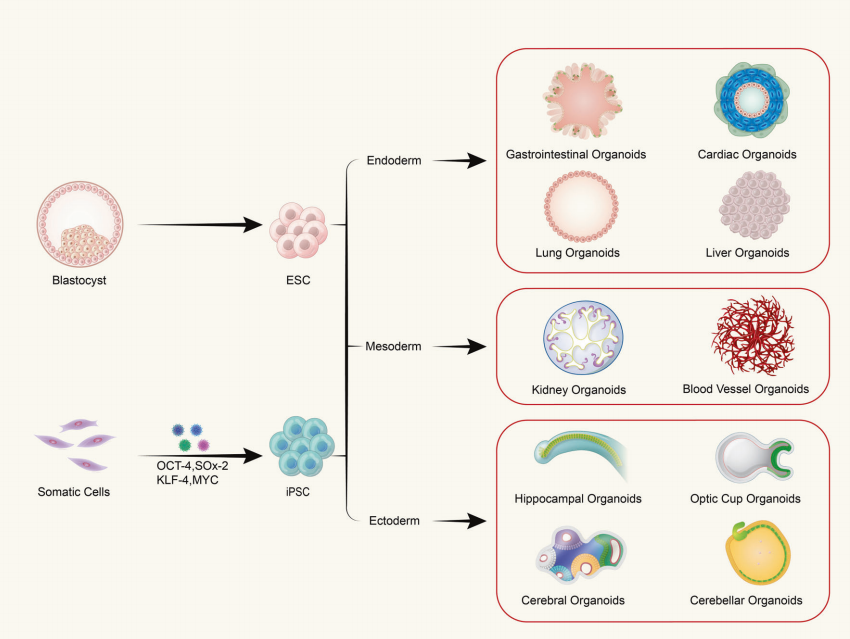
ऑर्गेनॉइड वयस्क स्टेम कोशिकाओं या प्लुरिपोटेंट स्टेम कोशिकाओं की इन विट्रो त्रि-आयामी (3D) खेती से बनते हैं, जिसके परिणामस्वरूप एक निश्चित स्थानिक संगठन के साथ ऊतक जैसी संरचनाएं बनती हैं। ऑर्गेनॉइड एकल कोशिकाओं से बनी संरचनाएं नहीं हैं; बल्कि, वे स्टेम सेल गुणों वाली आरंभिक कोशिकाओं के विभाजन और विभेदन को प्रेरित करके बनते हैं, जो फिर एक निश्चित स्थानिक संरचना, आकारिकी और कार्यक्षमता वाले ऊतकों में स्वयं-संयोजित होते हैं जो विवो में संबंधित अंगों के समान होते हैं।
प्रश्न: ऑर्गेनोइड्स के संवर्धन के स्रोत क्या हैं?
(1) प्लुरिपोटेंट स्टेम सेल से प्राप्त ऑर्गेनोइड्स में वयस्क स्टेम सेल (एएससी), प्लुरिपोटेंट स्टेम सेल (पीएससी) और प्रेरित प्लुरिपोटेंट स्टेम सेल (आईपीएससी) शामिल हैं। (2) ऊतक-निष्कर्षित कोशिकाओं से प्राप्त ऑर्गेनोइड्स आमतौर पर ट्यूमर ऊतकों में पाए जाते हैं।
प्रश्न: क्या ताजे ऊतक की अनुपस्थिति में जमे हुए ऊतक का उपयोग 3D संवर्धन के लिए किया जा सकता है?
हां, लेकिन हिमीकृत ऊतक के आकार के लिए उच्च आवश्यकताएं हैं, और प्राथमिक हिमीकृत ऊतक और कोशिकाओं की व्यवहार्यता काफी कम हो जाएगी, जिससे बाद की खेती में सफलता दर बहुत कम हो जाएगी।
प्रश्न: ऑर्गेनोइड्स को कैसे जमाया और पुनर्जीवित किया जाता है?
ऑर्गेनोइड्स को फ्रीज करने का सबसे अच्छा समय मार्ग 2-5 पर है, जब ऑर्गेनोइड्स की गतिविधि और विभेदन क्षमता अपने सबसे अच्छे स्तर पर होती है। ऑर्गेनोइड्स का पुनर्जीवन सेल पुनर्जीवन के लिए इस्तेमाल की जाने वाली विधियों का पालन कर सकता है।
प्रश्न: क्या संवर्धित ऑर्गेनोइड्स के आकार को नियंत्रित करना आवश्यक है, और यदि वे बहुत बड़े हैं तो क्या यह लाभदायक है?
हां, आकार को नियंत्रित करना आवश्यक है, अधिमानतः 500μm के भीतर, क्योंकि ऑर्गेनोइड्स में आंतरिक संवहनी और गैस-तरल परिसंचरण प्रणालियों की कमी होती है। जब ऑर्गेनोइड्स का आकार बड़ा होता है, तो केंद्र के पास की कोशिकाएं बाहरी वातावरण के साथ ऑक्सीजन और पोषक तत्वों का आदान-प्रदान करने के लिए संघर्ष करती हैं। इसलिए, संरचना जितनी बड़ी होगी, मृत कोशिकाओं की संख्या उतनी ही अधिक होगी।
प्रश्न: मैट्रिक्स जेल के अलावा ऑर्गेनोइड्स के संवर्धन के लिए और क्या उपयोग किया जा सकता है?
मैट्रिक्स जेल के अलावा, ऑर्गेनोइड्स को संवर्धित करने के विकल्पों में शामिल हैं (1) डीसेल्युलराइज्ड एक्स्ट्रासेलुलर मैट्रिक्स और अन्य व्युत्पन्न प्रोटीन, (2) सिंथेटिक हाइड्रोजेल, और (3) इंजीनियर्ड रीकॉम्बीनेंट प्रोटीन जैल।
प्रश्न: ऑर्गेनोइड्स का निर्देशित विभेदन कैसे प्राप्त किया जा सकता है?
ऑर्गेनोइड्स में स्टेम सेल-प्रेरित विभेदन के प्रारंभिक विकास को कई सिग्नलिंग मार्गों द्वारा संयुक्त रूप से विनियमित किया जाता है। इन विट्रो खेती के लिए इन सिग्नलिंग मार्गों की गतिविधि को अनुकरण करने के लिए वृद्धि कारकों को जोड़ने की आवश्यकता होती है, जो कोशिकाओं को विशिष्ट दिशाओं में विभेदित करने के लिए मार्गदर्शन करते हैं। उदाहरण के लिए, Y27632 और एक्टिविन ए के साथ प्रेरण भ्रूण स्टेम कोशिकाओं (ESCs) या प्रेरित प्लुरिपोटेंट स्टेम कोशिकाओं (iPSCs) को भ्रूण निकायों (EBs) में विभेदित कर सकता है। इसके बाद, सिग्नलिंग मार्ग को Wnt3a, FGF-4 और नोगिन जैसे कारकों द्वारा विनियमित किया जाता है ताकि विशिष्ट दिशाओं में स्टेम सेल विभेदन को प्रेरित किया जा सके।
प्रश्न: क्लिनिकल नमूने प्राप्त करते समय संदूषण से कैसे बचा जा सकता है?
(1) जितना संभव हो सके उतना सड़न रोकनेवाला नमूना सुनिश्चित करें। (2) निष्कर्षण से पहले, कई मिनटों के लिए एंटीबायोटिक युक्त पीबीएस में डुबोएं: बाहरी वातावरण के साथ संभावित संपर्क वाले क्षेत्रों जैसे कि पेट, आंतों और मूत्राशय में स्थित ट्यूमर के लिए, 5-10 मिनट के लिए 3% -5% एंटीबायोटिक युक्त पीबीएस में डुबोने की सिफारिश की जाती है; अन्य सामान्य ट्यूमर के लिए, लगभग 5 मिनट के लिए 1% -2% एंटीबायोटिक युक्त पीबीएस में डुबोएं। (3) सेल निष्कर्षण के दौरान उपयोग किए जाने वाले सभी अभिकर्मकों में 1% एंटीबायोटिक और प्राथमिक एंटीबायोटिक की उचित सांद्रता होनी चाहिए।
प्रश्न: ट्यूमर ऊतकों के संग्रह, संरक्षण और परिवहन के लिए क्या सावधानियां बरतनी चाहिए?
जितना संभव हो सके ट्यूमर कोशिकाओं की उच्च सामग्री वाले ट्यूमर ऊतकों को इकट्ठा करें, और संदूषण की संभावना को कम करने के लिए ऊतक के नमूनों को हवा के संपर्क में आने का समय कम से कम करें। एकत्रित ट्यूमर ऊतक के नमूनों को जल्द से जल्द विशेष नमूना संरक्षण समाधान युक्त बाँझ ट्यूबों में रखें और उन्हें कम तापमान (लगभग 4 डिग्री सेल्सियस) पर परीक्षण इकाई में तेजी से ले जाएँ (नमूना लेने के 2 से 4 घंटे के भीतर पहुँचाने का प्रयास करें)।
प्रश्न: क्या घावों से संवर्धित ऑर्गेनोइड्स और आस-पास के ऊतकों से संवर्धित ऑर्गेनोइड्स के बीच कोई अंतर है?
ट्यूमर ऊतकों के नमूने लेने वाली जगहों के लिए क्या ज़रूरतें हैं? हाँ, इसमें अंतर है। ट्यूमर खुद में विविधता दिखाते हैं, इसलिए अलग-अलग स्रोतों से प्राप्त ऑर्गेनोइड के बीच अंतर देखना आम बात है। रूपात्मक रूप से, प्राथमिक घावों से प्राप्त ऑर्गेनोइड में आस-पास के ऊतकों की तुलना में ज़्यादा आक्रामक संरचना होती है, जो आम तौर पर ज़्यादा अनियमित दिखाई देती है। मॉडलिंग या ड्रग स्क्रीनिंग में त्रुटियों को कम करने के लिए, अच्छी गतिविधि वाले क्षेत्रों से कई नमूने लिए जाने चाहिए।
प्रश्न: ट्यूमर ऑर्गेनोइड्स की दवा संवेदनशीलता परीक्षण के लिए किस प्रकार की दवाओं का उपयोग किया जा सकता है?
नैदानिक अभ्यास में मुख्य प्रकार की एंटी-ट्यूमर दवाओं को तीन श्रेणियों में वर्गीकृत किया जा सकता है: साइटोटॉक्सिक दवाएं (जैसे पैक्लिटैक्सेल, सिस्प्लैटिन/कार्बोप्लाटिन, 5-एफयू, आदि), लक्षित दवाएं (ईजीएफआर, एचईआर2, वीईजीएफआर, आदि को लक्षित करने वाली दवाएं), और प्रतिरक्षा जांच बिंदु अवरोधकों (पीडी-1 एंटीबॉडी, पीडी-एल1 एंटीबॉडी, आदि) द्वारा प्रदर्शित इम्यूनोथेरेपी दवाएं।
प्रश्न: पीडीओ खेती की सफलता दर क्या है?
पीडीओ खेती की सफलता दर स्रोत के आधार पर थोड़ी भिन्न होती है। अधिकांश पीडीओ की सफलता दर 63% से 70% के बीच होती है, या इससे भी अधिक, 90% तक, जो काफी हद तक ऊतक की गतिविधि से संबंधित होती है। इसके अतिरिक्त, नैदानिक उपचार सफलता दर को प्रभावित कर सकते हैं। ऊतक एक्स विवो और परिचालन चरणों के समय को कम करके सफलता दर में सुधार किया जा सकता है।
प्रश्न: क्या जमे हुए ऊतक का उपयोग ऑर्गेनोइड खेती के लिए किया जा सकता है?
आम तौर पर, व्यवहार्यता के महत्वपूर्ण नुकसान के कारण ऊतक क्रायोप्रिजर्वेशन की सिफारिश नहीं की जाती है। हालाँकि, यदि ऊतकों को -80 डिग्री सेल्सियस पर संग्रहीत किया जाता है, तो ऑर्गेनोइड खेती के लिए इष्टतम समय संरक्षण के बाद 6 सप्ताह के भीतर होता है। यदि ऊतकों को तरल नाइट्रोजन में संग्रहीत किया जाता है, तो संरक्षण समय लंबा हो सकता है लेकिन अधिमानतः छह महीने से अधिक नहीं होना चाहिए।
प्रश्न: प्राथमिक कोशिकाओं को निकालते समय, आमतौर पर फाइब्रोब्लास्ट्स भी इसमें शामिल होते हैं। इनसे कैसे निपटा जाना चाहिए?
(1) फाइब्रोब्लास्ट्स के खराब आसंजन के कारण, उन्हें बार-बार आसंजन द्वारा हटाया जा सकता है।(2) फाइब्रोब्लास्ट हटाने वाले अभिकर्मकों का उपयोग किया जा सकता है, लेकिन क्या वे ऑर्गेनोइड खेती को प्रभावित करते हैं, इसके लिए प्रयोगात्मक सत्यापन की आवश्यकता है।
प्रश्न: ट्यूमर ऑर्गेनोइड्स को कल्चर करने के लिए कितने मूल ट्यूमर ऊतक की आवश्यकता होती है? क्या बायोप्सी नमूना पर्याप्त है?
सामान्यतः, शल्य चिकित्सा के लिए ऊतक 2-3 सोयाबीन के आकार से बड़े होने चाहिए; यदि सुई बायोप्सी के माध्यम से प्राप्त किए जाते हैं, तो कम से कम 2-3 नमूनों की आवश्यकता होती है, जबकि एंडोस्कोपिक बायोप्सी के लिए कम से कम छह या अधिक ट्यूमर ऊतकों को क्लैंप करने की आवश्यकता होती है।
प्रश्न: यदि ट्यूमर ऊतक का नमूना बहुत छोटा है, और संवर्धित ऑर्गेनोइड की संख्या बाद के परीक्षण के लिए अपर्याप्त है, तो क्या किया जाना चाहिए?
चूंकि ट्यूमर स्रोतों से प्राप्त ऑर्गेनोइड्स पासिंग के बाद फेनोटाइपिक अंतर प्रदर्शित कर सकते हैं, इसलिए आमतौर पर पासिंग की सिफारिश नहीं की जाती है। साहित्य में ऑर्गेनोइड्स के पासिंग को 2-3 पीढ़ियों तक सीमित रखने की सिफारिश की गई है, अधिकतम 5 पीढ़ियों के साथ। यदि सेल संख्या बहुत छोटी है और 5 पीढ़ियों के बाद परीक्षण आवश्यकताओं को पूरा नहीं कर सकती है, तो परीक्षण विधि को बदलने पर विचार करें, जैसे कि एक छोटी 384-वेल प्लेट का उपयोग करना या परीक्षण के लिए माइक्रोफ्लुइडिक चिप्स आज़माना।
प्रश्न: क्या ट्यूमर के ऊतकों में सामान्य कोशिकाएँ होंगी? इन सामान्य कोशिकाओं को कैसे हटाया जाए?
सामान्य कोशिकाओं की संख्या कम हो सकती है। सबसे पहले, संग्रह के दौरान सामान्य ऊतकों के नमूने लेने से बचने की कोशिश करें। दूसरे, प्राथमिक कोशिकाओं को निकालने के बाद, आगे के ऑर्गेनोइड कल्चर के लिए चुंबकीय मनका छंटाई या प्रवाह साइटोमेट्री का उपयोग किया जा सकता है। जब बहुत कम संख्या में सामान्य कोशिकाएँ मौजूद होती हैं, तो यह बाद के ऑर्गेनोइड मॉडलिंग और कल्चर को महत्वपूर्ण रूप से प्रभावित नहीं करती हैं, इसलिए निष्कासन आवश्यक नहीं हो सकता है।
प्रश्न: ट्यूमर ऊतकों से प्राथमिक कोशिकाओं को निकालते समय कोशिकाएं लाल क्यों दिखाई देती हैं?
ऊतकों में रक्त की आपूर्ति प्रचुर मात्रा में होती है, इसलिए बहुत सारी लाल रक्त कोशिकाएँ होती हैं। ज़्यादातर मामलों में, इसके लिए प्रसंस्करण की ज़रूरत नहीं होती और इससे ऑर्गेनोइड की खेती पर कोई असर नहीं पड़ता। अगर बहुत ज़्यादा लाल रक्त कोशिकाएँ हैं, तो खेती से पहले उन्हें लिसिस बफर से उचित तरीके से उपचारित किया जा सकता है।
प्रश्न: ऑर्गेनोइड खेती के दौरान काले कण पाए जाते हैं। उन्हें कैसे हटाया जाए?
काले कण संभवतः अशुद्धियाँ या कोशिका मलबा हैं। इन्हें दो तरीकों से हटाया जा सकता है:
ऑर्गेनोइड्स को पचाएं और अशुद्धियों को पतला करने के लिए उन्हें बार-बार माध्यम से धोएं।
ऑर्गेनोइड्स को आधे में काटने के लिए एक जीवाणुरहित सर्जिकल चाकू का उपयोग करें, फिर ऑर्गेनोइड्स से अशुद्धियों को धीरे से बाहर निकालने के लिए माध्यम से भरी 1 मिलीलीटर सिरिंज का उपयोग करें।
प्रश्न: क्या ऑर्गेनोइड संवर्धन के लिए मार्गों की संख्या की कोई सीमा है, और कितने मार्ग संचालित किए जा सकते हैं?
मार्ग की संख्या आम तौर पर स्रोत कोशिकाओं के गुणों पर निर्भर करती है। अधिकांश ऑर्गेनोइड्स को इन विट्रो में 10 बार (>6 महीने) तक पारित किया जा सकता है। संस्कृति की स्थितियों का चुनाव भी कुछ प्रभाव डाल सकता है, जिसमें वातानुकूलित माध्यम आम तौर पर सिंथेटिक कारक माध्यम से बेहतर होता है।
प्रश्न: क्या ट्यूमर कोशिका रेखाओं (जैसे हेपजी2 कोशिका रेखा) को पीडीओ में संवर्धित किया जा सकता है?
पी.डी.ओ. जटिल स्व-संयोजित संरचनाएं हैं। एकल कोशिका रेखाओं द्वारा निर्मित 3डी संस्कृति प्रणालियों को पी.डी.ओ. नहीं कहा जा सकता; उन्हें केवल 3डी गोलाकार अवस्थाओं के रूप में संदर्भित किया जाता है।
प्रश्न: ऑर्गेनोइड्स को पास करने के मानदंड क्या हैं?
ऑर्गेनोइड्स की विकासात्मक स्थिति के आधार पर, समय भिन्न होता है, आमतौर पर 5-10 दिनों के बीच, लगभग 100-200μm व्यास के साथ। कुछ धीरे-धीरे विकसित होने वाले ऑर्गेनोइड्स को उपयुक्त पासिंग अवस्था तक पहुंचने में कई सप्ताह लग सकते हैं।
प्रश्न: व्यवहार्य ऑर्गेनोइड्स की संख्या की गणना कैसे करें?
प्रयोग के दौरान, पहले से तैयार कैल्सीन-एएम स्टोरेज घोल को बाहर निकालें और कैल्सीन-एएम घोल को माध्यम में 0.2μmol/L की अंतिम सांद्रता तक मिलाएँ। 37°C पर 60 मिनट तक इनक्यूबेट करें। समय बीत जाने के बाद, कैल्सीन-एएम युक्त माध्यम को धीरे-धीरे PBS से धोएँ और ताज़ा माध्यम डालें। ऑर्गेनोइड्स का निरीक्षण करने और उनकी तस्वीर लेने के लिए 490 एनएम की उत्तेजना तरंगदैर्ध्य और 515 एनएम की उत्सर्जन तरंगदैर्ध्य वाले फ्लोरोसेंस माइक्रोस्कोप का उपयोग करें। जीवित ऑर्गेनोइड्स हरे दिखाई देंगे और उनके किनारे साफ़ होंगे। 20μm से ज़्यादा व्यास वाले ऑर्गेनोइड्स की गिनती करें।
प्रश्न: ऑर्गेनोइड्स की व्यवहार्यता की गणना कैसे करें?
ऑर्गेनोइड्स की व्यवहार्यता की गणना सूत्र के अनुसार की जाती है: X=(Nlive/Ntotal)×100%, जहां: X ऑर्गेनोइड्स की व्यवहार्यता का प्रतिनिधित्व करता है; Nlive जीवित ऑर्गेनोइड्स की संख्या का प्रतिनिधित्व करता है; Ntotal ऑर्गेनोइड्स की कुल संख्या का प्रतिनिधित्व करता है।
प्रश्न: ऑर्गेनोइड्स की पहचान करने के तरीके क्या हैं?
सबसे बुनियादी विधि माइक्रोस्कोप के माध्यम से ऑर्गेनोइड्स की आकृति विज्ञान का निरीक्षण करना और एच एंड ई धुंधला करना है। अन्य विधियों में वेस्टर्न ब्लॉट, क्यूआरटी-पीसीआर, इम्यूनोफ्लोरेसेंस, फ्लो साइटोमेट्री शामिल हैं ताकि पता लगाया जा सके कि ऑर्गेनोइड्स संबंधित बायोमार्कर व्यक्त करते हैं या नहीं। आनुवंशिक अनुक्रमण सुसंस्कृत ऑर्गेनोइड्स और स्रोत ऊतक के बीच आनुवंशिक मिलान की पहचान कर सकता है। कुछ ऑर्गेनोइड्स के लिए, यह देखने के लिए कार्यात्मक परीक्षण किए जा सकते हैं कि क्या उनके पास विशिष्ट कार्य हैं। उदाहरण के लिए, अध्ययनों से पता चला है कि गैस्ट्रिक ऑर्गेनोइड्स गैस्ट्रिक एसिड का स्राव कर सकते हैं, और कार्डियक ऑर्गेनोइड्स स्वायत्त रूप से धड़क सकते हैं।
प्रश्न: क्या सामान्य कोशिकाएँ भी ऑर्गेनोइड में विकसित हो सकती हैं? ट्यूमर ऑर्गेनोइड खेती के दौरान सामान्य ऑर्गेनोइड को कैसे हटाया जाए?
सामान्य कोशिकाएँ भी ऑर्गेनोइड में विकसित हो सकती हैं। सामान्य ऑर्गेनोइड को हटाने के तरीकों में शामिल हैं: (1) माइक्रोस्कोप के तहत HE धुंधला परिणामों के आधार पर मैन्युअल चयन; (2) संस्कृति माध्यम की संरचना (जैसे विकास कारक / छोटे अणु अवरोधक) को समायोजित करके PDOs का शुद्धिकरण; (3) प्रवाह साइटोमेट्री या चुंबकीय मनका छंटाई के लिए एकल कोशिकाओं में PDOs को फैलाना।
प्रश्न: दवा संवेदनशीलता प्रयोगों के दौरान, क्या पीडीओ को मैट्रिक्स जेल से पचाया जाना चाहिए?
नहीं, PDO को इन विवो स्थितियों का अनुकरण करने के लिए त्रि-आयामी संरचना की आवश्यकता होती है। यदि मैट्रिक्स जेल से कोई समर्थन नहीं है, तो दवा संवेदनशीलता प्रयोगों की सटीकता प्रभावित होगी। आम तौर पर, घुलनशील दवाएं ऑर्गेनोइड्स पर कार्य करने के लिए मैट्रिक्स जेल में प्रवेश कर सकती हैं, लेकिन इम्यूनोसाइटोकेमिकल प्रयोगों का संचालन करते समय, मैट्रिक्स जेल को निकालना आवश्यक है।
प्रश्न: क्या पीडीओ प्रयोग पशु मॉडल (पीडीएक्स) को पूरी तरह से प्रतिस्थापित कर सकते हैं?
पीडीओ आंशिक रूप से पीडीएक्स की जगह ले सकते हैं, लेकिन पूरी तरह से नहीं।
प्रश्न: खेती के दौरान पी.डी.ओ. की असामान्य वृद्धि के क्या कारण हो सकते हैं, जो पिछली स्थितियों की तुलना में छोटे विकास चक्र और तेजी से प्रसार द्वारा चिह्नित हैं?
बाह्य कारक: (1) यह असामान्यता कुछ संदूषक कोशिकाओं, जैसे कि फाइब्रोब्लास्ट्स की व्यापक वृद्धि के कारण हो सकती है। ऐसे मामलों में, इन संदूषित कोशिकाओं की उपस्थिति की पुष्टि करने के लिए सेक्शन स्टेनिंग और अवलोकन करने की सिफारिश की जाती है और फिर उन्हें हटाने के लिए आगे बढ़ना चाहिए। (2) कुछ कारकों या छोटे अणुओं को जोड़ने सहित संस्कृति की स्थितियों में परिवर्तन, पीडीओ के प्रसार मार्गों को और अधिक सक्रिय कर सकते हैं।
आंतरिक फ़ैक्टर्स: संभावित आनुवंशिक उत्परिवर्तन। इसे सत्यापित करने के लिए, अनुक्रमण की सिफारिश की जाती है, और परिणामों की तुलना प्राथमिक PDOs के साथ की जानी चाहिए ताकि यह निर्धारित किया जा सके कि कोई आनुवंशिक उत्परिवर्तन है या नहीं।
प्रश्न: दवाओं के प्रति पीडीओ की संवेदनशीलता का परीक्षण कैसे किया जा सकता है?
PDOs को CCK8 परख, ATP सेल व्यवहार्यता परख, और जीवित/मृत धुंधलापन जैसी विधियों का उपयोग करके दवा संवेदनशीलता के लिए परीक्षण किया जा सकता है। ट्यूमर ऑर्गेनोइड्स की ATP गतिविधि का आकलन करना सबसे आम तरीका है। ATP कोशिकाओं में सबसे महत्वपूर्ण ऊर्जा अणु है और इसका उपयोग सेलुलर चयापचय स्तरों को मापने के लिए किया जा सकता है, जो व्यवहार्य कोशिकाओं की संख्या को दर्शाता है। सेलुलर एटीपी सामग्री पर दवा प्रशासन के प्रभाव के आधार पर, प्रत्येक दवा आहार के लिए IC50 मूल्य (परीक्षण की गई दवा की आधी-अधिकतम निरोधात्मक सांद्रता) की गणना ट्यूमर अवरोध के लिए सबसे प्रभावी दवाओं का चयन करने के लिए विश्लेषण सॉफ़्टवेयर का उपयोग करके की जा सकती है।
प्रश्न: क्या पी.डी.ओ. की दवा संवेदनशीलता प्रयोगों के लिए सांद्रता सीमा प्राथमिक ट्यूमर कोशिकाओं के समान है?
नहीं, वे समान नहीं हैं। आम तौर पर, PDOs के लिए दवा की सांद्रता प्राथमिक कोशिकाओं की तुलना में अधिक होनी चाहिए। औपचारिक दवा संवेदनशीलता प्रयोगों के लिए इष्टतम सांद्रता का विश्लेषण करने के लिए प्रारंभिक प्रयोग किए जा सकते हैं।
प्रश्न: विकास के किस चरण में ऑर्गेनोइड्स का उपयोग दवा परीक्षण के लिए किया जाना चाहिए?
आमतौर पर दवा परीक्षण के लिए 5 मार्गों के भीतर ऑर्गेनोइड का उपयोग करने की सिफारिश की जाती है। इस स्तर पर, ऑर्गेनोइड सबसे अच्छी स्थिरता और गतिविधि प्रदर्शित करते हैं।
प्रश्न: ऑर्गेनोइड स्थापना की सफलता निर्धारित करने के मानदंड क्या हैं?
(1) प्रारंभिक प्रारंभिक मूल्यांकन: ऑर्गेनॉइड आकारिकी सेलुलर अवस्था से रिक्तिका, नवोदित, कॉम्पैक्ट या ढीले जैसे रूपों में बदल जाती है। (2) विशिष्ट बायोमार्कर अभिव्यक्ति की पहचान, जो ऊतक स्लाइस में वितरण के समान होनी चाहिए। अधिक विस्तृत तुलना के लिए आगे अनुक्रम विश्लेषण किया जा सकता है।
प्रश्न: ऑर्गेनोइड संवर्धन नियमित कोशिका संवर्धन से किस प्रकार भिन्न है?
(1) विभिन्न सेल कल्चर विधियाँ: ऑर्गेनॉइड को अपनी त्रि-आयामी संरचना को बनाए रखने के लिए सब्सट्रेट या स्थानिक संरचनाओं के समर्थन की आवश्यकता होती है, जबकि नियमित सेल कल्चर के लिए इसकी आवश्यकता नहीं होती है। (2) ऑर्गेनॉइड कल्चर के लिए एक्स विवो भेदभाव और स्व-संयोजन प्राप्त करना आवश्यक है, इस प्रकार प्रेरण के लिए विभिन्न साइटोकिन्स के संयोजनों के उपयोग की आवश्यकता होती है, जिसके परिणामस्वरूप अपेक्षाकृत जटिल कल्चर माध्यम घटक बनते हैं। नियमित सेल कल्चर में आमतौर पर केवल एक ही प्रकार की कोशिका शामिल होती है, इसलिए कल्चर माध्यम घटक अपेक्षाकृत सरल होते हैं।(3) विभिन्न कोशिका स्रोत: ऑर्गेनोइड्स बहुशक्तिशाली उपकला कोशिकाओं से प्राप्त होते हैं, जबकि नियमित कोशिका संवर्धन विभिन्न प्रकार की चयनित कोशिकाओं की खेती के लिए उपयुक्त है।
प्रश्न: मैं कैसे निर्धारित कर सकता हूँ कि मेरे द्वारा संवर्धित 3D गोले ऑर्गेनोइड हैं और क्या वे लक्ष्य ऊतक के अनुरूप हैं?
ऑर्गेनोइड्स की पहचान करने के तरीकों में एच एंड ई स्टेनिंग, इम्यूनोहिस्टोकेमिस्ट्री (आईएचसी), सिंगल-सेल सीक्वेंसिंग और अन्य शामिल हैं। यह निर्धारित करने के लिए कि क्या वे लक्ष्य अंग या ऊतक के अनुरूप हैं, मॉर्फोलॉजिकल, हिस्टोपैथोलॉजिकल और आणविक आनुवंशिक दृष्टिकोण से बहुआयामी निर्णय लेना आवश्यक है। ट्यूमर ऑर्गेनोइड्स के लिए, पुष्टि के लिए विशिष्ट बायोमार्कर का पता लगाने का उपयोग किया जा सकता है।
प्रश्न: यदि खेती के दौरान देखी गई ऑर्गेनोइड्स की आकृति विज्ञान साहित्य में बताई गई आकृति विज्ञान से भिन्न है, तो इसका क्या कारण हो सकता है?
सबसे पहले, नमूना स्रोतों और उपप्रकारों में व्यक्तिगत अंतर और विविधता मौजूद हो सकती है। दूसरे, चयनित साइटोकाइन्स और प्रेरण के लिए उपयोग किए जाने वाले कुछ छोटे अणु अवरोधकों की गुणवत्ता में अंतर से विभिन्न ऑर्गेनोइड्स के विभेदन आकारिकी में भिन्नता हो सकती है। केवल साहित्य विवरण पर निर्भर रहने के बजाय, HE धुंधलापन, IHC और आनुवंशिक अनुक्रमण जैसे तरीकों के माध्यम से ऑर्गेनोइड आकृति विज्ञान और स्रोत ऊतक के बीच स्थिरता की पुष्टि करने का सुझाव दिया जाता है।
प्रश्न: ऑर्गेनोइड्स के साथ दवा संवेदनशीलता प्रयोग करते समय, क्या दवाओं के लिए विलायक के रूप में उपयोग किए जाने वाले डीएमएसओ की मात्रा को नियंत्रित करना आवश्यक है?
हां, आमतौर पर दवा संवेदनशीलता प्रयोगों के लिए डीएमएसओ का आयतन प्रतिशत 0.5% से कम होना आवश्यक है।
प्रश्न: मैट्रिक्स जेल से ऑर्गेनोइड्स को कैसे पुनर्प्राप्त किया जा सकता है?
निम्नलिखित विधियों की सिफारिश की जाती है: (1) व्यावसायिक रूप से उपलब्ध ऑर्गेनोइड रिकवरी समाधान (CAT#41421ES) का उपयोग कोशिकाओं या कोशिका सतह प्रोटीन को नुकसान पहुँचाए बिना धीरे-धीरे और प्रभावी ढंग से सेल निलंबन प्राप्त करने के लिए किया जा सकता है। (2) मैट्रिक्स जेल को नरम करने और ऑर्गेनोइड को मुक्त करने के लिए इसे कम तापमान पर पिघलाया जा सकता है।
प्रश्न: रिकवरी के दौरान कई ऑर्गेनोइड सेंट्रीफ्यूज ट्यूब की दीवारों से चिपक जाते हैं। रिकवरी दर को कैसे बेहतर बनाया जा सकता है?
संग्रह के बाद अपकेंद्रित्र करते समय, क्षैतिज रोटर अपकेंद्रित्र का उपयोग करें और अपकेंद्रित्र गति को उचित रूप से बढ़ाएँ। आम तौर पर, लगभग 300g का केन्द्रापसारक बल और लगभग 1000-1200rpm की गति उपयुक्त होती है।
| पीउत्पाद एनए एम इ | बिल्ली | आकार |
| मानव Wnt-3a | 92276ES10 | 10μजी |
| 92278ES20 | 20μजी | |
| 92701ES10 | 10μजी | |
| मानव सिर | 92528ES10 | 10μजी |
| 91330ईएस10 | 10μजी | |
| 91306ईएस10 | 10μजी | |
| 91502ईएस10 | 10μजी | |
| 91701ES08 | 10μजी | |
| 92602ES60 | 100μजी | |
| 91204ES10 | 10μजी | |
| 90601ईएस10 | 10μजी | |
| 91113ES10 | 10μजी | |
| 92279ES10 | 10μजी | |
| 92055ईएस10 | 10μजी | |
| 92053ES10 | 10μजी | |
| 92129ES08 | 5μजी | |
| 91304ES10 | 10μजी | |
| 91702ईएस10 | 10μजी | |
| 92252ES60 | 100μजी | |
| 90103ईएस10 | 10μजी | |
| 90104ES10 | 10μजी | |
| 90197ES10 | 10μजी | |
| 90144ES08 | 10μजी | |
| 90196ES10 | 10μजी | |
| 90194ES10 | 10μजी | |
| 90111ES10 | 10μजी | |
| 90120ईएस10 | 10μजी | |
| 90198ES10 | 10μजी | |
| 91605ईएस10 | 10μजी | |
| 92251ES10 | 10μजी | |
| 92566ES08 | 5μजी | |
| 92102ईएस10 | 10μजी | |
| 91103ES10 | 10μजी | |
| 92711ES10 | 10μजी | |
| 92122ES60 | 100μजी | |
| 92201ES60 | 100μजी | |
| 92275ES20 | 20μजी | |
| मानव बीएमपी-2 | 92051ES10 | 10μजी |
संबंधित पठन:
संदर्भ
