Công nghệ "phát hiện" hình ảnh trong cơ thể sống khiến các tế bào "ẩn" không có nơi nào để ẩn náu
Bạn muốn kiểm soát sự phát triển khối u ở chuột nude theo thời gian thực? Bạn có muốn biết vị trí của quá trình xâm chiếm tế bào ở chuột không? Bạn muốn biết tác dụng của điều trị bằng thuốc đối với khối u trong cơ thể sống? Bạn có thể thực hiện điều này bằng cách cài đặt một thiết bị theo dõi trên ô, cho phép bạn kiểm soát vị trí và số lượng ô bất cứ lúc nào. Công nghệ này là công nghệ "phát hiện" hình ảnh in vivo. Vậy công nghệ hình ảnh in vivo là gì?
1. Công nghệ hình ảnh in vivo là gì?
2. Đặc điểm của hình ảnh luciferase
3. Hướng ứng dụng của hình ảnh luciferase
4. Chia sẻ ví dụ thực nghiệm
5. Câu hỏi thường gặp
6. Thông tin sản phẩm
7. Về việc đọc
1. Công nghệ hình ảnh in vivo là gì?
Ngay từ năm 1999, Tiến sĩ Weissleder của Đại học Harvard tại Hoa Kỳ đã đề xuất khái niệm hình ảnh phân tử, tức là sử dụng các phương pháp hình ảnh để tiến hành nghiên cứu định tính và định lượng về các quá trình sinh học trong cơ thể sống ở cấp độ tế bào và phân tử. Hình ảnh trong cơ thể sống dựa trên hình ảnh phân tử. Thông qua hệ thống hình ảnh này, các quá trình sinh học như sự phát triển và di căn của khối u, sự phát triển của các bệnh truyền nhiễm và biểu hiện của các gen cụ thể có thể được quan sát ở động vật sống.
In vivo, hình ảnh quang học của động vật sống chủ yếu áp dụng hai công nghệ: phát quang sinh học và huỳnh quang. Phát quang sinh học là gen luciferase để đánh dấu tế bào hoặc DNA, trong khi công nghệ huỳnh quang sử dụng gen báo cáo huỳnh quang như protein huỳnh quang xanh và protein huỳnh quang đỏ và huỳnh quang như FITC, Cy5 và Cy7. Các nguyên tố và chấm lượng tử (QD) để dán nhãn. Phát quang sinh học ở động vật có vú thường tích hợp gen luciferase của đom đóm (gồm 554 nucleotide, khoảng 50KD), tức là gen luciferase, vào DNA nhiễm sắc thể của tế bào quan sát dự kiến để biểu hiện luciferase. Sau đó, nuôi cấy một dòng tế bào có thể biểu hiện luciferase ổn định và khi các tế bào phân chia, biệt hóa và chuyển giao, luciferase cũng sẽ tiếp tục biểu hiện ổn định. Gen, tế bào và động vật sống đều có thể được gắn thẻ bằng gen luciferase. Luciferase là một loại enzyme có thể xúc tác các chất nền để tạo ra phát quang sinh học. Luciferase từ các nguồn khác nhau có đặc điểm riêng và có thể xúc tác các chất nền để phát ra các màu ánh sáng khác nhau. Trong số đó, luciferase đom đóm có độ nhạy cao và phạm vi tuyến tính rộng từ 7~8 bậc độ lớn. Nó đã trở thành gen báo cáo tế bào động vật có vú được sử dụng phổ biến nhất. Plasmid báo cáo luciferase được chuyển vào các tế bào và chất nền luciferin của nó được thêm vào để ủ các tế bào. Với sự hiện diện của ATP, O2và ion magiê, luciferase có thể oxy hóa chất nền luciferin để tạo ra phản ứng ánh sáng khả kiến. Thực hiện "cài đặt 'theo dõi' một lần, theo dõi và phát hiện bất cứ lúc nào". Ngoài luciferase đom đóm, đôi khi người ta còn sử dụng renilla luciferase. Chất nền của hai chất này khác nhau, chất nền của chất trước là D-luciferin, và chất nền của chất sau là coelenterazine. Bước sóng phát sáng của hai chất này khác nhau, phạm vi bước sóng ánh sáng phát ra của chất trước là 540-600nm, và phạm vi bước sóng ánh sáng phát ra của chất sau là 460-540nm. Ánh sáng phát ra của chất trước dễ đi qua mô hơn, trong khi chất sau được chuyển hóa nhanh hơn trong cơ thể và tính đặc hiệu của nó không tốt bằng chất trước. Do đó, không phải hầu hết các thí nghiệm in vivo đều sử dụng luciferase đom đóm làm gen báo cáo.
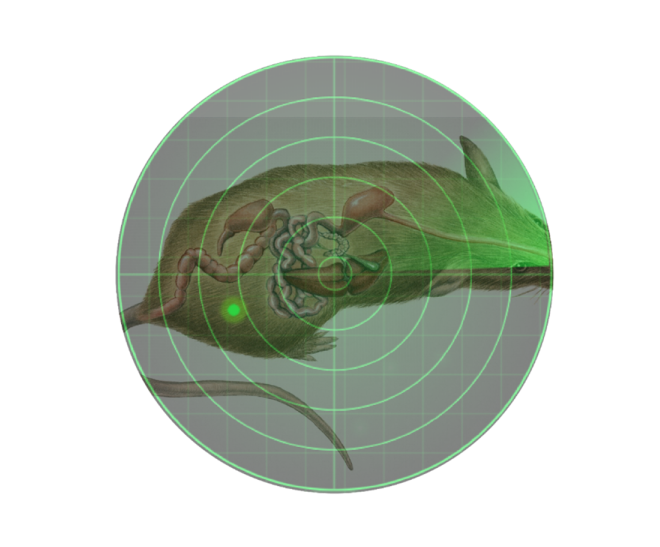
Hình 1.Vị trí của các tế bào được gắn nhãn luciferase
Nguyên lý quang học của phát quang sinh học: ánh sáng sẽ bị tán xạ và hấp thụ khi truyền trong các mô của động vật có vú, và các photon sẽ bị khúc xạ khi gặp màng tế bào và tế bào chất, và các loại tế bào và mô khác nhau có các đặc điểm hấp thụ photon khác nhau. Hemoglobin là nguyên nhân chính gây ra sự hấp thụ ánh sáng khả kiến trong cơ thể và có thể hấp thụ hầu hết dải ánh sáng khả kiến màu xanh lam-xanh lục. Nhưng trong dải ánh sáng khả kiến màu đỏ lớn hơn 600nm, sự hấp thụ của hemoglobin rất nhỏ. Do đó, một lượng lớn ánh sáng có thể đi qua mô và da để được phát hiện trong vùng màu đỏ. Có thể phát hiện ít nhất vài trăm tế bào dưới da bằng công nghệ hình ảnh phát quang sinh học ở động vật sống. Tuy nhiên, tùy thuộc vào độ sâu của nguồn sáng trong chuột, số lượng tế bào tối thiểu có thể nhìn thấy sẽ khác nhau. Nói chung, cứ tăng 1cm, cường độ sáng sẽ giảm đi 10 lần và sự suy giảm nhiều hơn đối với các mô và cơ quan giàu máu, và sự suy giảm ít hơn đối với các mô và cơ quan liền kề với xương. Trong trường hợp cùng độ sâu, cường độ sáng được phát hiện có mối quan hệ tuyến tính đáng kể với số lượng tế bào và cường độ sáng được phát hiện có thể được định lượng bằng thiết bị để phản ánh số lượng tế bào.
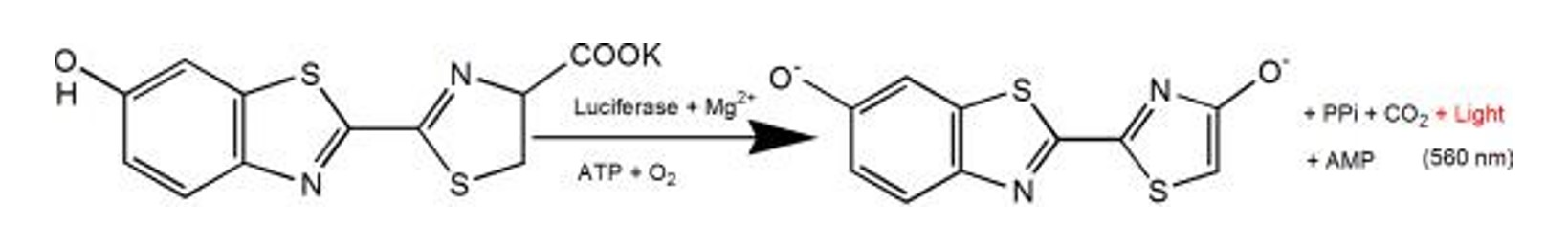
Hình 2. Nguyên lý phát quang của phản ứng muối kali luciferase và luciferin
Khác với phát quang sinh học, công nghệ huỳnh quang sử dụng gen báo cáo huỳnh quang hoặc thuốc nhuộm huỳnh quang (bao gồm các vật liệu nano-labeling mới như chấm lượng tử huỳnh quang) để gắn nhãn. Sử dụng huỳnh quang từ gen báo cáo, protein huỳnh quang hoặc thuốc nhuộm, có thể tạo ra nguồn sáng sinh học trong cơ thể sống. Phát quang sinh học là tự huỳnh quang ở động vật không có nguồn sáng kích thích, trong khi huỳnh quang đòi hỏi phải kích thích bằng nguồn sáng kích thích bên ngoài trước khi có thể được hệ thống hình ảnh phát hiện. Nhãn huỳnh quang được sử dụng rộng rãi, bao gồm động vật, tế bào, vi sinh vật, kháng thể, thuốc, vật liệu nano, v.v.
2. Đặc điểm của hình ảnh luciferase
◎ không có bức xạ, hầu như vô hại với sinh vật.
◎ Phát quang sinh học không cần nguồn sáng kích thích.
◎ Độ nhạy cao, có thể phát hiện hàng trăm tế bào.
◎ Khả năng xuyên thấu tốt, vẫn có thể phát hiện được độ sâu mô 3-4cm.
◎ Tỷ lệ tín hiệu trên nhiễu cao, tín hiệu huỳnh quang mạnh và khả năng chống nhiễu tốt.
3. Hướng ứng dụng của hình ảnh luciferase
3.1 Sự phát triển của khối u
Trong thí nghiệm phát sinh khối u ở chuột trụi lông, sự phát triển của khối u được quan sát theo thời gian thực mà không có sự xâm lấn và không cần phải cắt bỏ khối u để đo lường.
3.2 Thuốc ung thư
Ảnh hưởng của việc dùng thuốc lên sự phát triển hoặc di căn của khối u đã được phát hiện và chất nền fluorescein có thể bị loại bỏ trong vòng 3 giờ mà không ảnh hưởng đến thử nghiệm thuốc.
3.3 Vị trí tế bào
Đã phát hiện được vị trí và sự phân bố của tế bào lạ ở động vật.
3.4 Điều hòa biểu hiện gen
Gen mục tiêu hoặc vùng khởi động của gen mục tiêu được hợp nhất với gen luciferase để phát hiện những thay đổi biểu hiện gen trong quá trình điều trị bằng thuốc hoặc quá trình diễn biến của bệnh.
3.5 Nghiên cứu tế bào gốc
Theo dõi quá trình cấy ghép, sự sống sót và sự tăng sinh của tế bào gốc; Theo dõi sự phân bố và di chuyển của tế bào gốc trong cơ thể sống.
4. Thí nghiệm ví dụ chia sẻ

Hình 3. trong cơ thể sống phát hiện hình ảnh tác dụng điều trị của CAR-MUC1 T/CAR-MUC1-IL22 Tế bào T trên sự hình thành khối u bằng cách tiêm dưới da tế bào HN4 chuột[1].
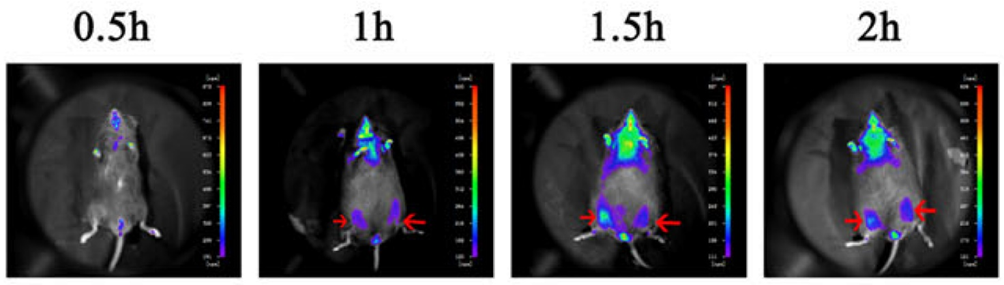
Hình 4. Sau khi các tế bào HUC-MSC được tiêm vào cơ xương chuột, vị trí của các tế bào được phát hiện bằng trong cơ thể sống hình ảnh (được đánh dấu bằng mũi tên màu đỏ)[2].
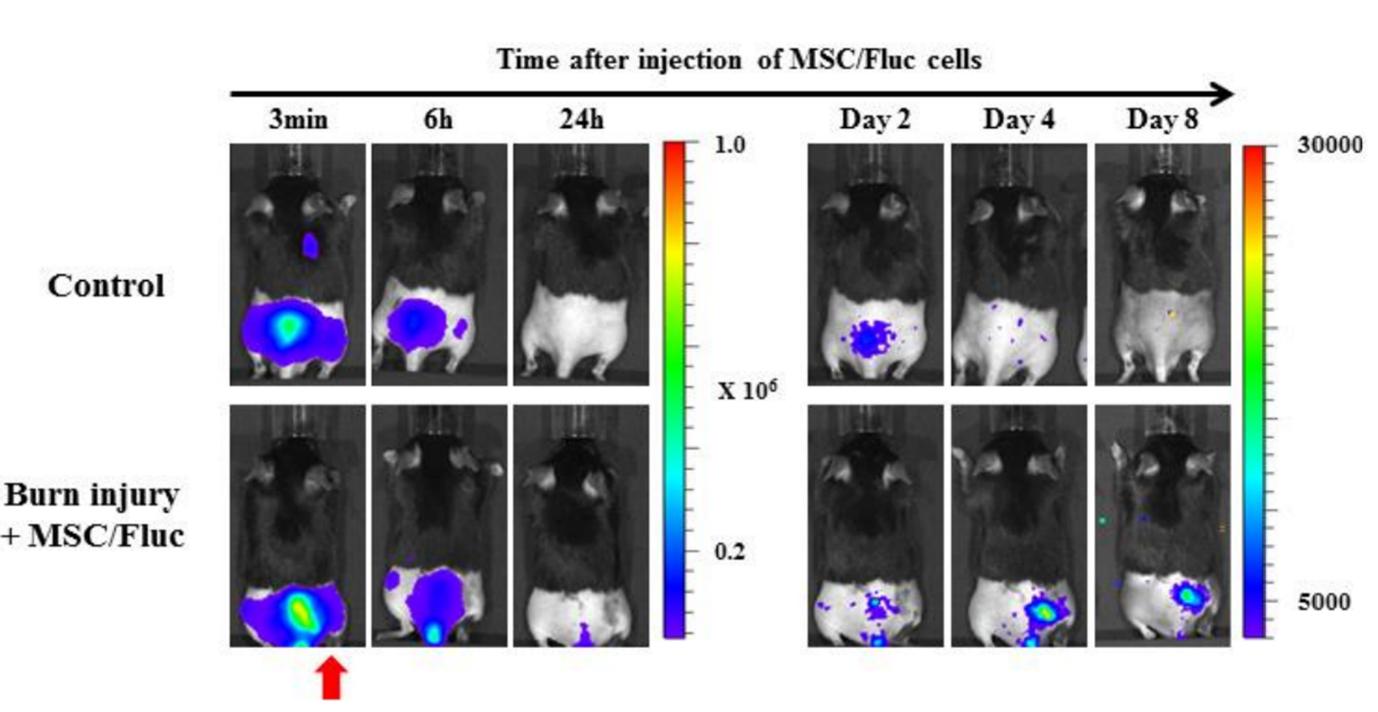
Hình 5. Khả năng của trong cơ thể sống chụp ảnh để phát hiện sự di chuyển của tế bào gốc trung mô (MSC) đến các vị trí bỏng. Tế bào gốc trung mô (MSC/FLuc) được tiêm tĩnh mạch vào mô hình bỏng lưng ở chuột. Bốn ngày sau khi tiêm, các tín hiệu phát quang sinh học xuất hiện tại vị trí bị thương của vết bỏng, sau đó giảm dần (mũi tên màu đỏ chỉ vị trí bỏng)[3].
5. Câu hỏi thường gặp
Câu hỏi 1: So với công nghệ truyền thống, công nghệ hình ảnh phát quang sinh học có ưu điểm gì?
So với công nghệ truyền thống, công nghệ này nhạy hơn các phương pháp truyền thống trong nghiên cứu di căn khối u, liệu pháp gen, dịch tễ học, theo dõi tế bào gốc, bệnh bạch cầu và các nghiên cứu liên quan khác. Nó cũng có thể nhanh chóng và trực quan nghiên cứu cơ chế bệnh sinh và sàng lọc thuốc của các bệnh liên quan thông qua một loạt các mô hình bệnh động vật chuyển gen.
Câu hỏi 2: Làm thế nào để gắn nhãn tế bào gốc bằng gen luciferase?
Các gen được biểu hiện liên tục có thể được dán nhãn để tạo ra chuột chuyển gen và các tế bào gốc được dán nhãn. Các tế bào gốc tạo máu được lấy từ tủy xương của chuột và cấy ghép vào tủy xương của một con chuột khác. Công nghệ này có thể được sử dụng để theo dõi sự tăng sinh, biệt hóa và di chuyển của các tế bào gốc tạo máu trong cơ thể. Một phương pháp khác là dán nhãn các tế bào gốc bằng lentivirus.
Câu hỏi 3: Sau khi tiêm fluorescein, thời gian thử nghiệm thích hợp là bao lâu và độ phát quang có thể kéo dài bao lâu?
Nhìn chung, tín hiệu huỳnh quang đạt đến giai đoạn ổn định mạnh nhất sau khi tiêm phúc mạc trong 10-15 phút và bắt đầu suy giảm sau 20-30 phút. Sau 3 giờ, fluorescein bị loại bỏ và hiện tượng phát quang biến mất hoàn toàn.
Câu hỏi 4: Làm thế nào để tiêm fluorescein vào chuột? Sự khác biệt giữa các phương pháp tiêm là gì?
Fluorescein có thể được tiêm vào chuột bằng cách tiêm phúc mạc hoặc tiêm tĩnh mạch đuôi. Nó có thể lan ra toàn bộ cơ thể chuột trong khoảng 1 phút. Trong hầu hết các trường hợp, nồng độ fluorescein là 150 mg/kg. Đối với chuột 20 g, có thể sử dụng khoảng 3 mg fluorescein. Đối với tiêm phúc mạc, sự khuếch tán chậm, phát quang ban đầu chậm và thời gian phát quang liên tục dài. Đối với tiêm tĩnh mạch đuôi fluorescein, nó khuếch tán nhanh và bắt đầu phát sáng nhanh, nhưng thời gian phát quang ngắn.
6.Thông tin sản phẩm
Bảng 1. Thông tin sản phẩm
| Thông tin sản phẩm | Mã sản phẩm | Thông số kỹ thuật |
| D-Luciferin, Muối Natri | 40901ES01/02/03/08/10 | 0,1/0,5/1/5/10g |
| D-Luciferin, Muối Kali | 40902ES01/02/03/08 | 0,1/0,5/1/5g |
| D-Luciferin Firefly, Axit Tự Do (Hỏi thăm) | 40903ES01/02/03 | 0,1/0,5/1 |
| Coelenterazine h (Hỏi thăm) | 40906ES02/03/08 | 0,5/1/5mg |
| Sẵn sàng sử dụng Coelenterazine h (Hỏi thăm) | 40907ES10 | 10 lọ |
| Bộ xét nghiệm gen báo cáo Luciferase kép (Hỏi thăm) | 11402ES60/80 | 100/1000T |
| Bộ xét nghiệm gen báo cáo Luciferase (Hỏi thăm) | 11401ES60/76/80 | 100/500/1000T |
| Plasmid báo cáo Luciferase VDR (Vitamin D Receptor)Hỏi thăm) | 11502ES03 | 1μg |
| Plasmid báo cáo gen luciferase STAT1 (Hỏi thăm) | 11504ES03 | 1μg |
7. Về việc đọc
Một thế hệ mới của hệ thống phát hiện gen báo cáo luciferase——Dễ dàng hơn, nhạy hơn, chính xác hơn
