Übersicht über T4 DNA Ligase
Welche Enzyme verwenden Wissenschaftler, um ein neues Gen zu binden? Natürlich gehört dazu auch DNA-Ligase. Warum ist DNA-Ligase also bei rekombinanter DNA so wichtig? Weil DNA-Ligase für die Ligation des Zielfragments an den Vektor verantwortlich ist, was eines der Schlüsselelemente ist, die den Erfolg des Experiments bestimmen. Welche Rolle spielt T4-DNA-Ligase als eine Art DNA-Ligase bei molekularen Klonexperimenten? Wie funktioniert sie? Die T4-DNA-Ligase wird als Nächstes ausführlich vorgestellt.
1. Was ist T4-DNA-Ligase?
2. Was ist die Funktion der T4-DNA-Ligase?
3.
4. Eine Auswahlhilfe für
1. Was ist T4-DNA-Ligase?
T4-DNA-Ligase ist eine ATP-abhängige Ligase, die die Ligationsreaktion zwischen DNA-Molekülen katalysiert. Sie bildet hauptsächlich Phosphodiester, indem sie die 3'-Hydroxyl- und 5'-Phosphatenden verbindet. DNA-Ligasen sind an DNA-Replikations- und Reparaturprozessen in allen Organismen beteiligt. Die phagenkodierte T4-DNA-Ligase wird während einer Infektion von E. coli mit dem Phagen T4 produziert.
Die in der Gentechnik verwendeten Ligasen sind hauptsächlich E. coli-DNA-Ligase und T4-DNA-Ligase, wobei letztere derzeit weiter verbreitet ist. T4-DNA-Ligase kann einzelsträngige Bruchstellen an doppelsträngiger DNA, doppelsträngiger RNA oder DNA/RNA-Hybridsträngen reparieren, um zwei benachbarte Nukleotide zu verbinden, und spielt eine wichtige Rolle bei der DNA-Reparatur und -Rekombination.
Im rekombinanten Plasmidkonstruktionsprozess kann T4-DNA-Ligase zusammen mit Restriktionsenzymen verwendet werden, um das Experiment zur rekombinanten Plasmidkonstruktion abzuschließen. Es kann die Bildung einer Phosphodiesterbindung zwischen dem 5'-P-Ende und dem 3'-OH-Ende doppelsträngiger DNA katalysieren und weist eine gute Verbindungseffizienz für klebrige Endverbindungen und stumpfe Endverbindungen auf.
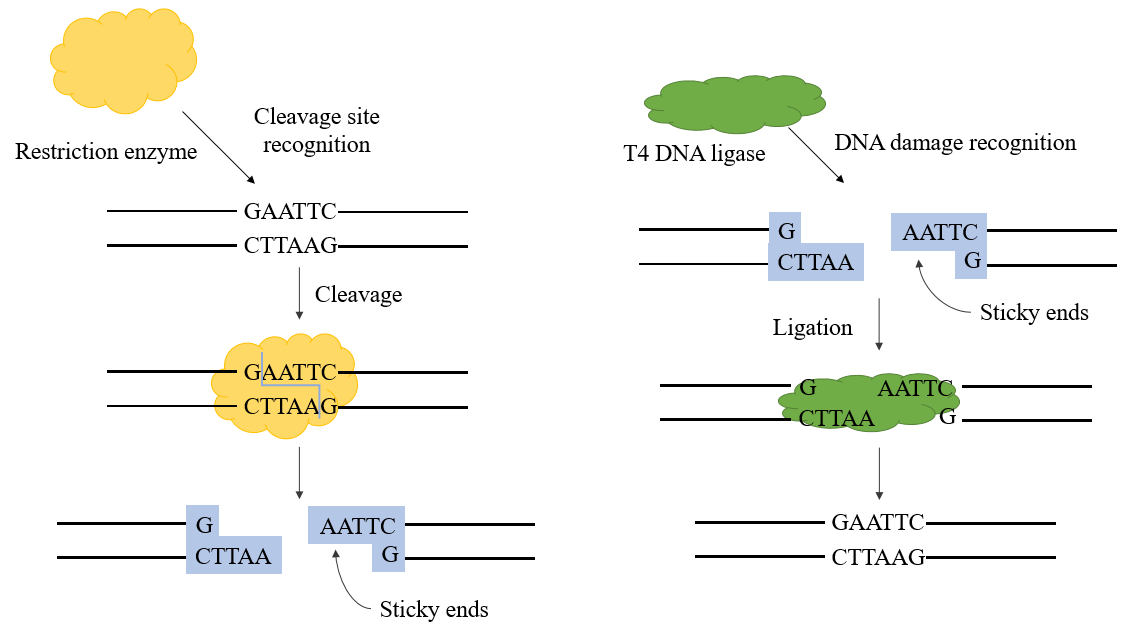
Abbildung 1. T4-DNA-Ligase-Mechanismus
2. Was ist die Funktion der T4-DNA-Ligase?
2.1 Vektorkonstruktion
Bei Experimenten zur Vektorkonstruktion können verschiedene Restriktionsenzyme unterschiedliche Endentypen erzeugen. Für unterschiedliche Enden verfügt die T4-DNA-Ligase über unterschiedliche Ligationsstrategien.
2.1.1 Klonierung mit Restriktionsenzymen, klebrige Enden entstehen durch Einzelverdau
Wenn während der Konstruktion des Vektors dieselbe Restriktionsendonuklease zum Schneiden des DNA-Fragments des Zielgens verwendet wird und das Vektormolekül dasselbe klebrige Ende erzeugen kann, kann die T4-DNA-Ligase die Rekombinationsverbindung direkt durchführen. Da die klebrigen Enden jedoch gleich sind, kann das Zielgen in Vorwärts- oder Rückwärtsrichtung in den Vektor eingefügt werden, was den Arbeitsaufwand beim Screening nach korrekten rekombinanten Klonen leicht erhöht. Erwägen Sie die Verwendung der Doppelenzymverdauungsmethode für die Vektorkonstruktion.
Darüber hinaus können die kohäsiven Enden des durch Einzelenzymverdauung hergestellten Vektors auch gepaart werden, und dann werden unter der Einwirkung von T4-DNA-Ligase Phosphodiesterbindungen zwischen Nukleotiden gebildet, was zur Selbstligation des Vektors führt. Die Behandlung des verdauten Vektors mit alkalischer Phosphatase kann die Phosphatgruppe am 5'-Ende des Vektors entfernen, sodass der Vektor die Selbstligation nicht abschließen kann. Somit werden unter der Einwirkung von T4-DNA-Ligase der Vektor und das Zielfragment verbunden, um die Konstruktion des rekombinanten Vektors abzuschließen.
2.1.2 Klonierung mit Restriktionsenzymen, klebrige Enden entstehen durch Doppelverdau
Wenn beim Vektoraufbau zwei Restriktionsenzyme mit unterschiedlichen klebrigen Enden verwendet werden, um das Zielfragment bzw. den Vektor zu verdauen, können zwei verschiedene klebrige Enden erzeugt werden. An diesem Punkt kann die T4-DNA-Ligase selektiv dieselben klebrigen Enden ligieren, um sicherzustellen, dass das Zielfragment in der richtigen Richtung in den Vektor eingefügt wird. Wenn das Zielfragment und der Vektor in Abbildung 2 gleichzeitig mit EcoR I und BamH I verdaut werden, können dieselben klebrigen Enden verbunden werden. Es gibt nur eine Ligationsrichtung zwischen dem Zielfragment und dem Vektor.

Abbildung 2. Durch Doppelenzymverdauung erzeugte klebrige Endligation[1]
2.1.3 Klonierung von Restriktionsfragmenten, blunt end
Einige Restriktionsendonukleasen, wie Sma I und andere, können bei enzymatischen Spaltungen auch stumpfe Enden erzeugen. T4-DNA-Ligase kann direkt eine Phosphodiesterbindung zwischen Vektor und Insert bilden, und es ist keine Paarung zwischen den Basen erforderlich. Diese Methode weist jedoch eine geringe Ligationseffizienz auf und ist anfällig für die Selbstligation des Vektors. Im Allgemeinen können die stumpfen Enden in klebrige Enden umgewandelt und dann ligiert werden. Beispielsweise verbessert das Hinzufügen komplementärer Poly-A- und Poly-T-Basen an den Enden des Zielfragments und des Vektors sowie künstlich klebriger komplementärer Enden die Verbindungseffizienz durch terminale Desoxynukleotidyltransferase.
2.1.4 TA-Klonen
Der beim TA-Klonen verwendete T-Vektor hat am 3'-Ende einen T-Überhang. Wenn die DNA-Sequenz des Zielfragments unklar ist, kann das Zielgenfragment durch TA-Klonen mit dem T-Vektor verbunden werden und das Zielgen kann durch Sequenzierung bestimmt werden. Die bei der PCR verwendete Taq-DNA-Polymerase hat eine terminale Transferaseaktivität und kann ein Nukleotid „A“ an das 3'-Ende des DNA-Fragments anfügen. T4-DNA-Ligase kann das durch Taq-DNA-Polymerase amplifizierte Produkt direkt mit dem T-Vektor verbinden und das durch PCR amplifizierte Produkt kann den Zweck eines effizienten Klonens ohne Hinzufügen künstlicher Adapter erfüllen.
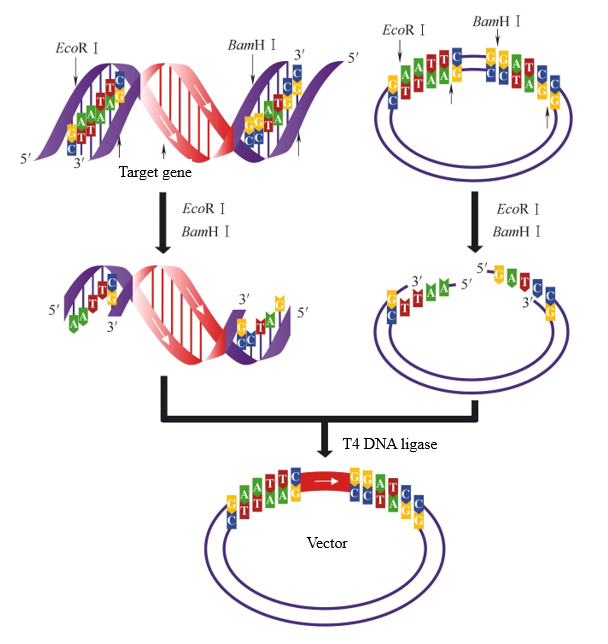
Abbildung 3. Der Workflow des TA-Klonens[2]
2.2 NGS-Adapterligatur
Während der Konstruktion der Sequenzierungsbibliothek der nächsten Generation muss der künstliche Adapter mit dem PCR-Produkt verbunden werden, bevor er an der Durchflusszelle auf dem Sequenzierungschip befestigt werden kann, um die Sequenzierung abzuschließen. Der Aufbau einer TA-Klonierungs-Ligationslinker-Bibliothek ist ein sehr verbreitetes technisches Mittel und sein Prinzip ähnelt dem oben erwähnten TA-Klonieren. Nachdem das zu sequenzierende DNA-Fragment am 5'-Ende phosphoryliert und am 3'-Ende ein „A“ hinzugefügt wurde, ist es komplementär und wird mit dem Adapter mit dem klebrigen „T“-Ende gepaart. Der vollständige Doppelstrang wird dann von der Maschine gebildet und sequenziert.
Während der TA-Ligation wirken sich unterschiedliche Probentypen oder die Komplexität der Nukleinsäurefragmentstruktur auf die Effizienz der Ligation aus, sodass sich auch die Adapter verschiedener Plattformen auf das endgültige Bibliotheksergebnis auswirken.
Beispielsweise verfügt der Bubble-Adapter der MGI-Plattform über eine spezielle Sekundärstruktur und erfordert eine sehr hohe Ligationseffizienz für T4-DNA-Ligase, und die Verringerung der Ligationseffizienz wirkt sich direkt auf die Ausgabe der Bibliothek aus.
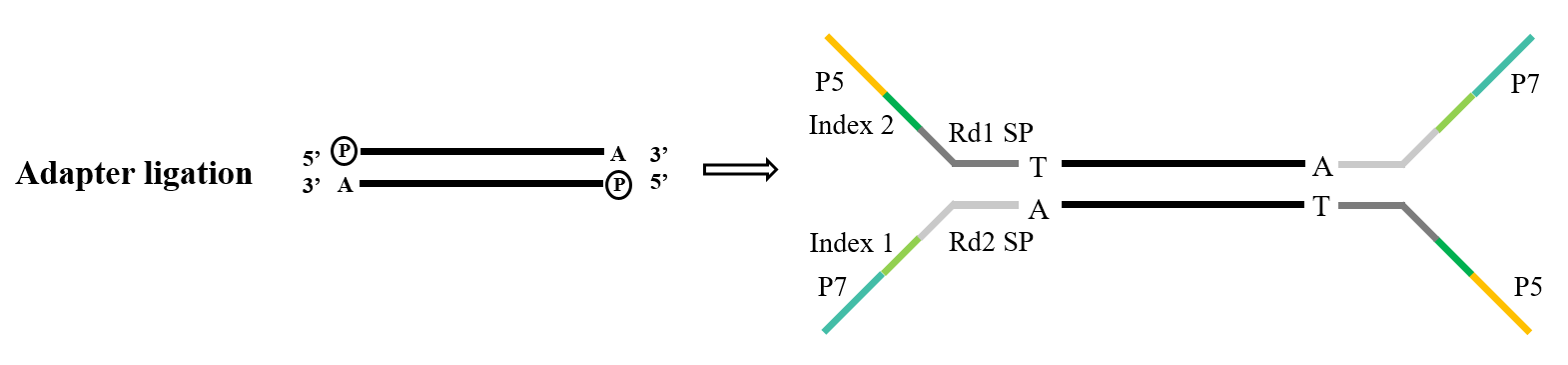
Abbildung 4. Allgemeiner Adapterligaturprozess
3.Yeasen Biotech T4 DNA Ligase kann für die NGS-Adapterligation verwendet werden
3.1 Yeasen Biotech Fast T4 DNA Ligase mit ultrahoher Ligationseffizienz
Verwenden Sie
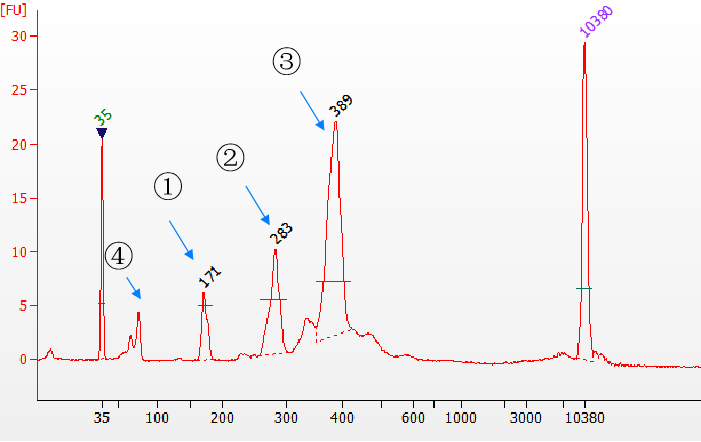
Abbildung 5. Verschiedene Arten von Ligationsprodukten, die vom Agilent 2100 erkannt werden
3.2 Yeasen Biotech Fast T4 DNA Ligase mit hervorragender Bibliotheksausbeute
Bei Verwendung von Fast T4 DNA Ligase für verschiedene Arten der Bibliothekskonstruktion sind die Bibliothekserträge im Vergleich zu anderen T4 DNA Ligasen besser.
Tabelle 1. Bibliotheksertrag verschiedener Arten von Proben
| Arten von Proben | gDNA der Darmmikrobiota | DNA-Extrakt | FFPE HD200 gDNA | |||
| T4 DNA-Ligase (dieselbe Einheit) | | N* | | N* | | N* |
| Eingegebene DNA (ng) | 10 | 10 | 50 | |||
| Anzahl der Amplifikationszyklen | 10 | 10 | 8 | |||
| Durchschnittliche Ausbeute (μg) Illumina-Plattform | 3.3 | 2.8 | 2.7 | 2.2 | 3 | 2.5 |
| Durchschnittliche Ausbeute (μg) MGI-Plattform | 2.7 | 0,9 | 2.0 | 0,7 | 2.3 | 0,8 |
4. Eine Auswahlhilfe für Yeasen Biotech T4 DNA Ligase
Tabelle 2: Verwandte Produkte
| Produktpositionierung | Produktname | Katze# | Anwendung |
| Universal | Hieff™ Gold T4 DNA Ligase (Erkundigen) | 10300ES | Molekulares Klonen. |
| Universal | 10301ES | Aufbau der NGS-Bibliothek. | |
| Hohe Ligationseffizienz und geringe Wirts-E. coli Rückstände | 10299ES | Aufbau einer NGS-Bibliothek, besonders geeignet für die Erkennung von Krankheitserregern, NIPT-Erkennung usw. | |
| Hohe Empfindlichkeit | 10298ES | Aufbau einer NGS-Bibliothek, besonders geeignet für den Aufbau einer Bibliothek von cfDNA-Proben. |
Verweise
[1] W. Yuan. Gentechnik[M]. Chemical Industry Press, 2019.
[2] Clark DP, Pazdernik NJ, Mcgehee M R. Klonen von Genen für die synthetische Biologie - ScienceDirect[J]. Molecular Biology (Dritte Ausgabe), 2019:199-239.
[3] Tomkinson AE, Vijayakumar S, Pascal JM, et al. DNA-Ligasen: Struktur, Reaktionsmechanismus und Funktion[J]. Chemical Reviews, 2006, 106(2):687-699.
[4] Shuman S. DNA-Ligasen: Fortschritt und Perspektiven[J]. Journal of Biological Chemistry, 2009, 284(26):17365-17369.
