HCD/HCP

生物学的製品の品質管理のための高感度、FGグレードの残留DNA検出キット
概要
宿主細胞の残留 DNA は、生物製剤の製造にかかわるプロセス関連の不純物であり、生物製剤の有効性を低下させるだけでなく、感染性や腫瘍形成性などの安全性上の懸念を引き起こす可能性があります。そのため、各国の規制当局は、生物製剤中の残留 DNA の量に制限を設けています。
現在の WH...
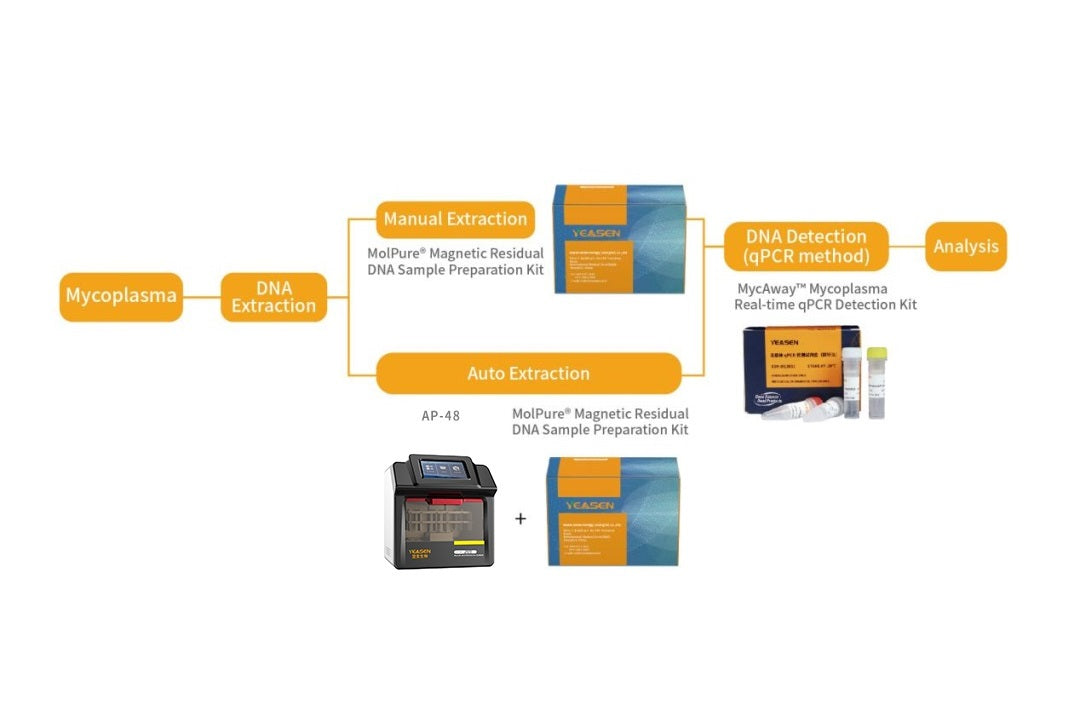
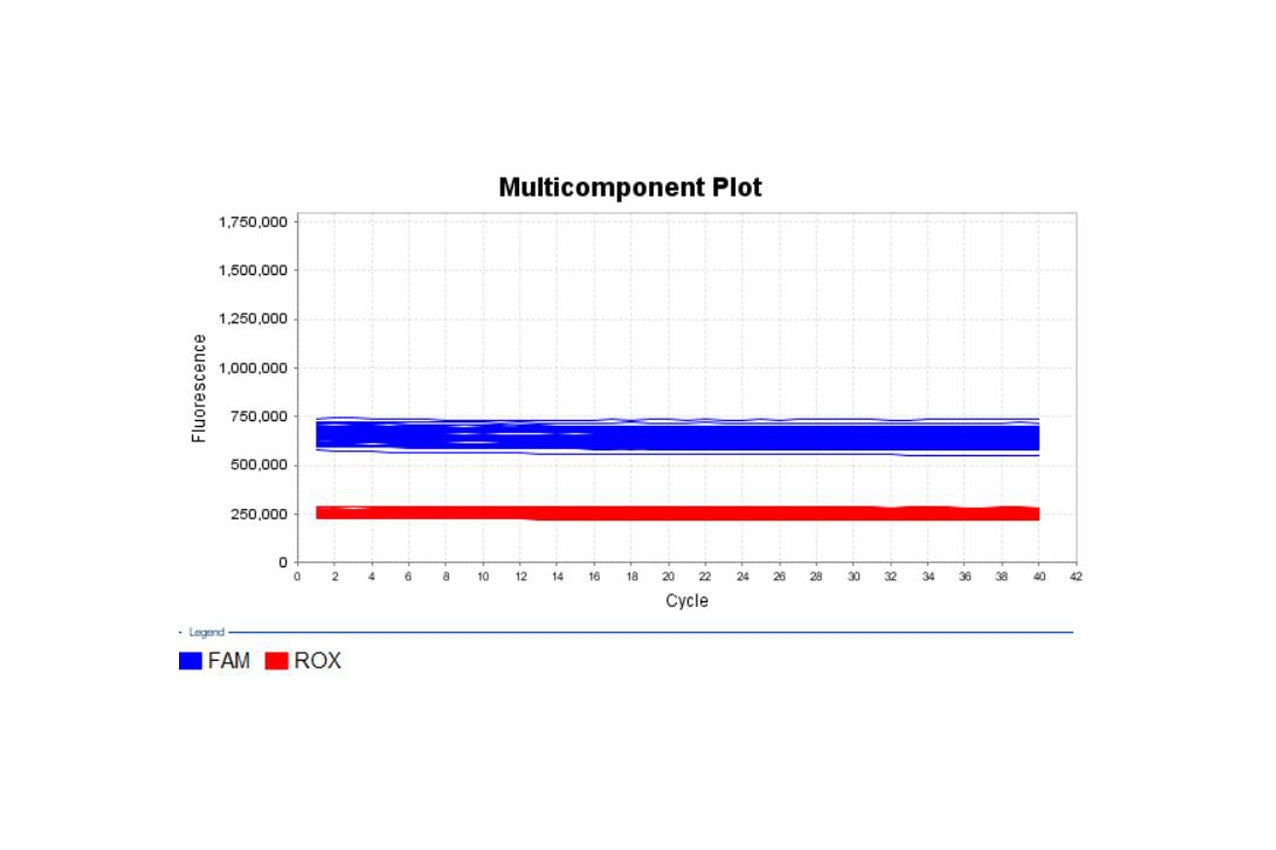
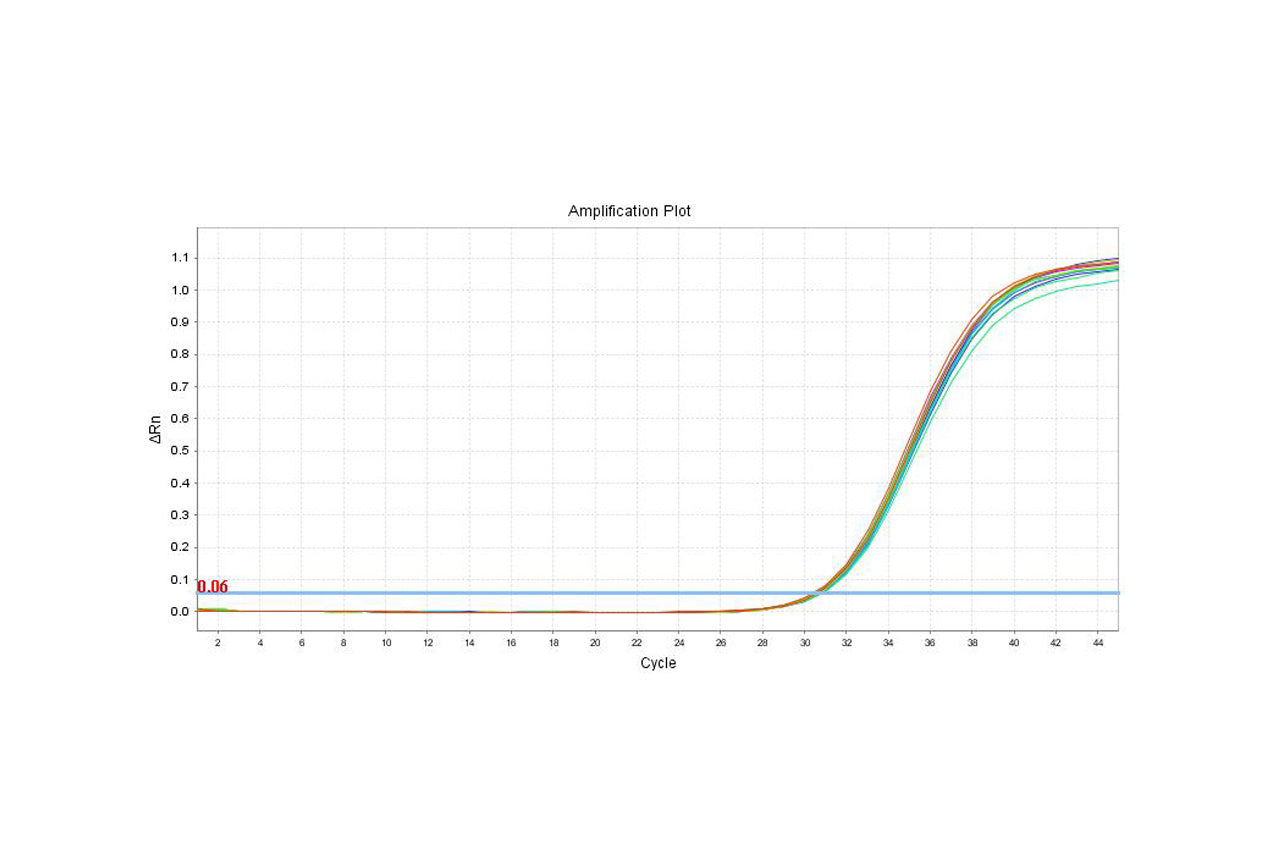
MycAway マイコプラズマ リアルタイム qPCR 検出キット (2G) 検証レポート
背景
このレポートにまとめられたデータは、MycAway TMマイコプラズマ リアルタイム qPCR 検出キット (2G) 製品について Yeasen Biotechnology (Shanghai) Co., Ltd. によって実行されたものです。
概要データはユー...
CHO 宿主細胞 DNA 残留物検出キット (3G) 検証レポート
CHO宿主細胞 DNA 残留物検出キット(3 G )
資格概要(カタログ番号: 41332 ES60)
背景
このレポートにまとめられたデータは、CHO 宿主細胞 DNA 残留物検出キット (3G) 製品について Yeasen Biotechnology が実施したも...
HEK293 宿主細胞 DNA 残留物検出キット (3G) 検証レポート
HEK293宿主細胞 DNA 残留物検出キット(3 G )
資格概要(カタログ番号:4 1331 ES60)
背景
このレポートにまとめられたデータは、Yeasen Biotechnology が「HEK293 宿主細胞 DNA 残留物検出キット (3G)」製品用に実...
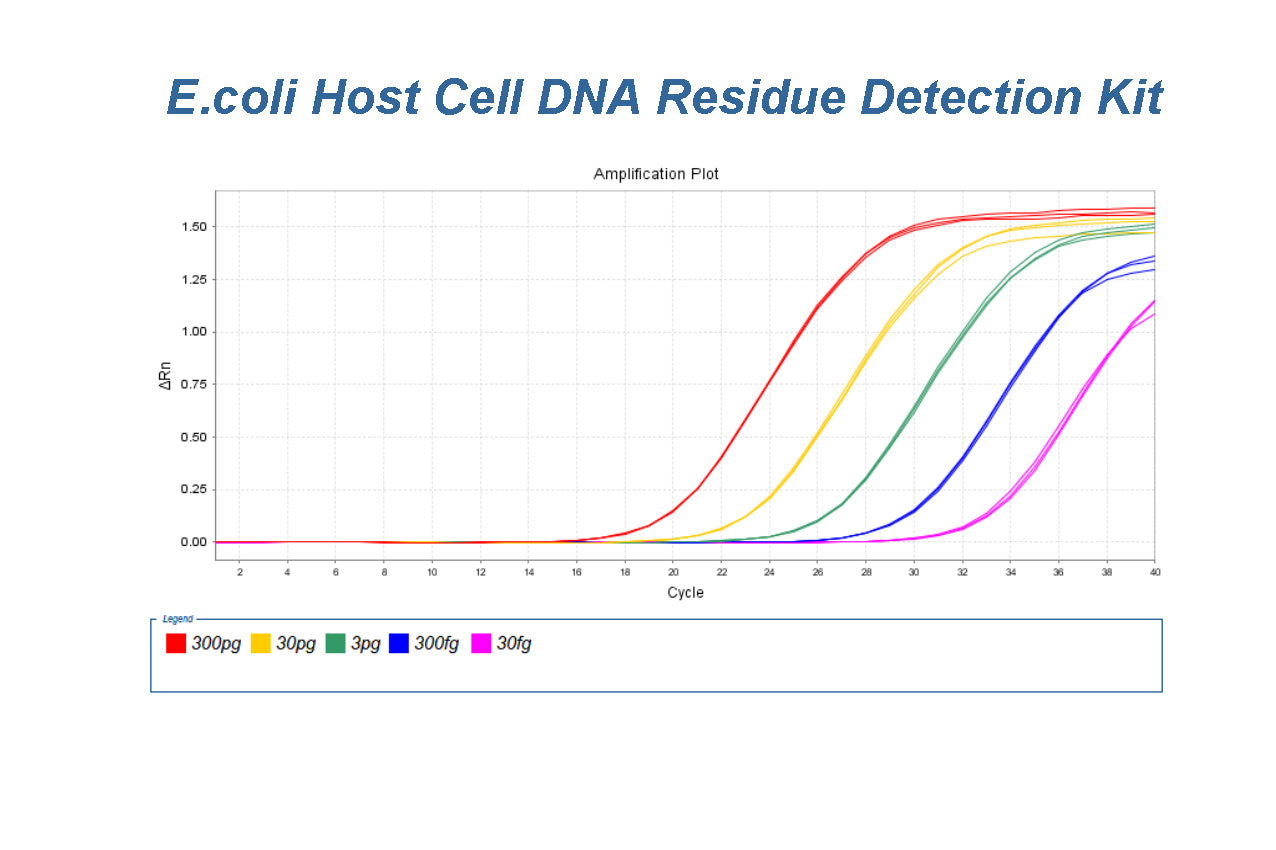
大腸菌宿主細胞DNA残留物検出キット(2G)検証レポート
大腸菌宿主細胞DNA残留物検出キット( 2G )
資格概要(カタログ番号:4 1308 ES60)
背景
このレポートにまとめられたデータは、Yeasen Biotechnology が「E.coli 宿主細胞 DNA 残留物検出キット (2G)」製品用に実施したもの...

マイコプラズマqPCR検出と方法の検証は、細胞および遺伝子治療技術開発の進歩に貢献します。
近年、バイオメディカルの急速な発展、COVID-19パンデミック下での細胞・遺伝子治療の出現、mRNAワクチンの登場により、生物学的製品の安全性と信頼性の確保は、世界中の政府や規制機関の焦点となっています。マイコプラズマ汚染は一般的ですが、除去するのが難しいタイプの汚染です。規制要件では、細...

宿主細胞残留DNA検出キットは生物製剤の研究開発と製造を促進
宿主細胞の残留 DNA は、生物製剤の製造にかかわるプロセス関連の不純物であり、生物製剤の有効性を低下させるだけでなく、感染性や腫瘍形成性などの安全性上の懸念を引き起こす可能性があります。そのため、各国の規制当局は、生物製剤中の残留 DNA の量に制限を設けています。
WHO と米国 FDA...

