Celtherapie verwijst naar het gebruik van biotechnologische methoden om cellen met specifieke functies te verkrijgen, die vervolgens worden verbeterd door processen zoals ex vivo-expansie en gespecialiseerde cultivatie. Deze cellen zijn begiftigd met verbeterde immuunreacties, pathogene en tumorceldodende capaciteiten en andere functies om de therapeutische doelen voor bepaalde ziekten te bereiken. Gentherapie verwijst naar de therapeutische benadering van het wijzigen van individuele genexpressie of het repareren van defecte genen door methoden zoals genadditie, genmodificatie en gen-silencing. Het uiteindelijke doel is om ziekten te genezen door abnormale genen te corrigeren.
| Product Typen | Beschrijving | Nummer van Goedgekeurd Medicijnen Wereldwijd |
| Gen Therapie Vector Producten | Deze producten gebruik maken van gen therapie vectoren naar leveren therapeutisch genen naar specifiek cellen in de patiënt weefsels, richten voor de uitdrukking of verordening van therapeutisch eiwitten. Dit categorie vertrouwt op op de levering van gen therapie vectoren. | 2 |
| Cellulair Producten | Gebruik makend van integreren viraal vectoren (zo een als lentiviraal vectoren), genen Zijn geïntroduceerd naar binnen voorloper cellen of stang cel genomen onder ex levend voorwaarden. Als cellen verdeling, de genen Zijn voorbij naar afstammeling cellen. De gewijzigd cellen Zijn Dan doordrenkt rug naar binnen de geduldig. Cellulair producten voornamelijk erbij betrekken categorieën zo een als T cellen, NK cellen, En stang cellen. | 8 |
| Oncolytisch Virus Producten | Afgeleid van van gewijzigd oncolytisch virussen met tumor-dodend mogelijkheden, deze producten werk op de beginsel van gebruik makend van de virus specifiek herkenning van tumor cellen En de immuun activering geactiveerd bij infecteren tumor cellen. Dit leidt naar gericht doden van tumor cellen. | 1 |
Oplossing voor virale vectorproductie en -expressie
De kern van de productie van geneesmiddelen voor cel- en gentherapie (CGT) ligt in de expressie van virale vectoren, een proces dat doorgaans zowel upstream-vectorexpressie als downstream-zuivering omvat. Vectorproductie omvat zeer complexe processen, brengt aanzienlijke uitdagingen met zich mee en heeft vaak lange voorbereidingscycli. Bijgevolg nadert de wereldwijde GMP-productiecapaciteit voor virale vectoren een knelpunt, wat een groot obstakel vormt voor de ontwikkeling van de gehele gentherapie-industrie. De ontwikkeling, opschaling en GMP-productie van gentherapievectoren omvatten ingewikkelde productiesystemen en strenge kwaliteitscontrolesystemen. Deze omvatten processen zoals het opzetten van stammen-, cel- en virusbanken, grootschalige E.coli-fermentatie, celkweekprocessen, virusoogst- en zuiveringsprocessen, aseptische verwerking en formulerings- en afvulprocessen.
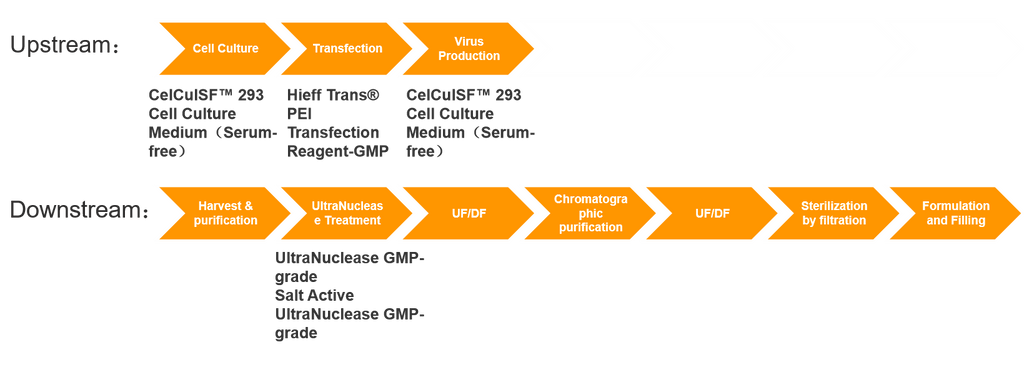
 AAV-productiekosten
AAV-productiekosten
Naast investeringen in vaste activa (zoals apparatuur, cleanrooms, etc.) en arbeidskosten, komen de belangrijkste kosten voort uit materiaalverbruik in de upstream- en downstreamprocessen. Upstreamkosten omvatten voornamelijk grondstoffen zoals plasmiden, kweekmedia, transfectiereagentia en nucleasen; downstreamkosten omvatten voornamelijk chromatografieharsen, kwaliteitscontrolekosten en meer.
Kationische polymeerdrager
Kationische polymeren (polymeren) omvatten polyethyleenimine (PEI), poly(beta-amino-ester) (PBAE), chitosan, polyacrylamide (PAH), diethylaminoethyldextran (DEAE-dextran), poly(amidoamine) dendrimeren (PAMAM) en andere. Het algemene principe van kationische polymeertransfectie omvat het complexeren van DNA onder fysiologische pH-omstandigheden om afbraak door DNase te voorkomen. Vervolgens hechten deze complexen zich aan het celmembraan en worden ze opgenomen door endocytose, gevolgd door breuk en vrijlating van DNA in het cytoplasma om hun beoogde functies uit te oefenen. Het primaire onderscheid tussen kationische polymeren en kationische lipiden ligt in de afwezigheid van hydrofobe delen in kationische polymeren, waardoor ze volledig in water oplosbaar zijn en gemakkelijke chemische modificaties mogelijk zijn.
Hieff Trans® PEI-transfectiereagentia

| Test Item | Standaard | Onderzoek en ontwikkeling Cijfer (40820) | GMP Cijfer (40821) |
| Averschijning | Compleet, nauwkeurig informatie, Nee schade, enz | √ | √ |
| Transfectie enefficiëntie | > 70% Transfectie efficiëntie> 80% Cel levensvatbaarheid | √ | √ |
| Ikndotoxine | < 0,5 EU/ml | √ | √ |
| Steriliteit | Aseptisch groei | √ | √ |
| Mycoplasma Residu | Negatief | √ | √ |
| pH | < 7.0 | √ | |
| Osmotisch PRessure | ≤ 30 mOsm/kg | √ | |
| Onzuiverheid Roverblijfsel | Methanol(≤ 0.3%) Ethyl ether(≤ 0,5%) Methylbenzeen(≤ 0,002%) | √ | |
| Zwaar Menz. Roverblijfsel | ≤ 10 p.p.m. |
| √ |
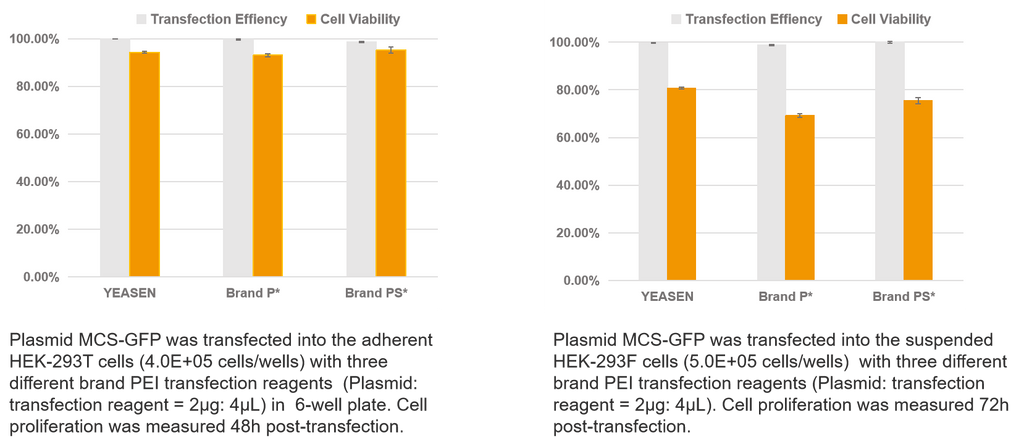
Transfectie van een enkel plasmide
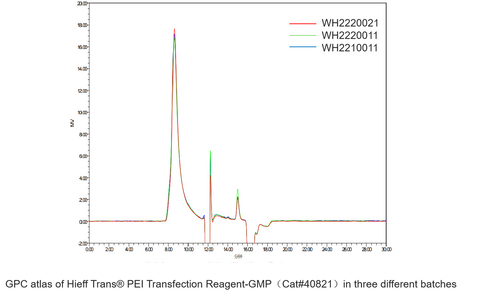
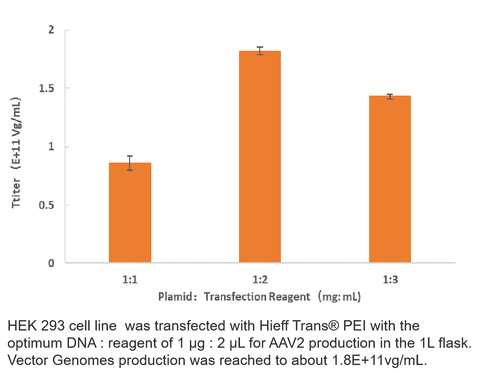
Virustitergegevens
1. LV-productie

2. AAV2-productie
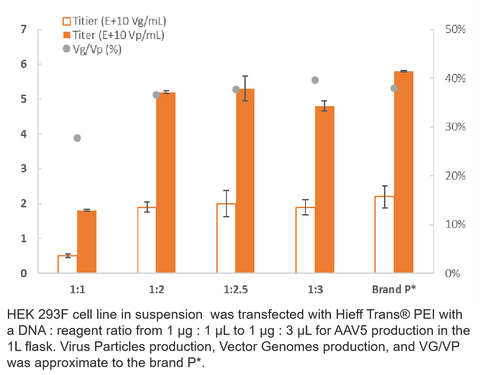
3. AAV5-productie
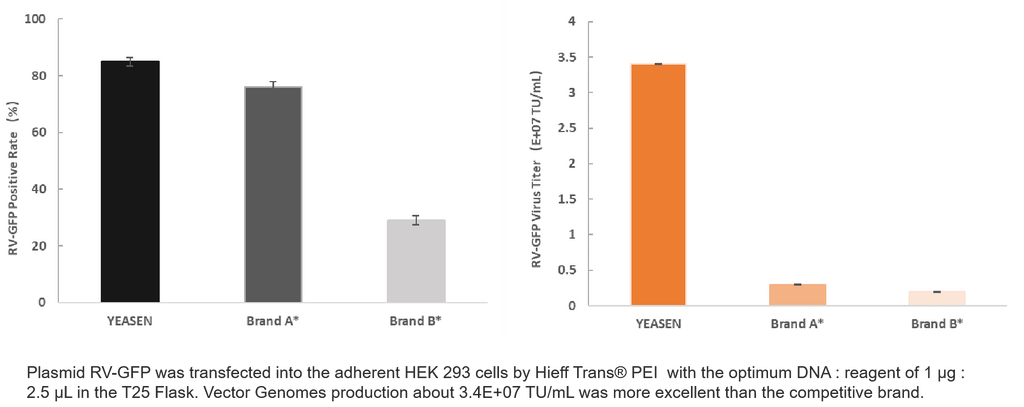
4. RV-productie
Productinformatie
| Productnaam | Cat.nr. |
| Hieff Trans® PEI Transfectie Reagens-GMP | 40821ES |
| E.coli gastheercel DNA residu detectie kit | 41308ES |
| E.coli Host Cell RNA Residu Detectie Kit | 41318ES |
| E.coli HCP ELISA-kit | 36712ES |
| HEK293 HCP ELISA-kit | 36713ES |
| HEK293 Host Cell DNA Residu Detectie Kit | 41302ES |
| HEK293 Host Cell Residue DNA-grootteanalysekit | 41316ES |
| MycAway™ Mycoplasma Real-time qPCR Detectiekit (2G) | 40619ES |
| UCF.ME® UltraNuclease GMP-klasse | 20157ES |
| Zout Actieve UltraNuclease GMP-kwaliteit | 20159ES |
| UltraNuclease ELISA-kit | 36701ES |
| Zout Actieve UltraNuclease ELISA Kit | 36703ES |
| RCA (E1A) Kopie-aantaldetectiekit | 41321ES |
| Replicatie-competente Lentivirus (RCL) Detectiekit | 41311ES |
| MolPure™ Magnetische Rest-DNA Monstervoorbereidingskit | 18461ES |
