Клеточная терапия относится к использованию методов биотехнологии для получения клеток с определенными функциями, которые затем улучшаются с помощью таких процессов, как ex vivo расширение и специализированное культивирование. Эти клетки наделены усиленными иммунными реакциями, возможностями уничтожения патогенных и опухолевых клеток и другими функциями для достижения терапевтических целей при определенных заболеваниях. Генная терапия относится к терапевтическому подходу изменения экспрессии отдельных генов или исправления дефектных генов с помощью таких методов, как добавление генов, модификация генов и подавление генов. Конечная цель — излечение болезней путем исправления аномальных генов.
| Продукт Типы | Описание | Число из Одобренный Наркотики Во всем мире |
| Ген Терапия Вектор Продукция | Эти продукты использовать ген терапия векторы к доставлять терапевтический гены к специфический клетки в пациента ткани, прицеливание для выражение или регулирование из терапевтический белки. Этот категория полагается на доставка из ген терапия векторы. | 2 |
| Сотовый Продукция | С использованием интегрирующий популярный векторы (такой как лентивирусный векторы), гены являются введен в предшественник клетки или корень клетка геномы под бывший виво условия. Как клетки разделять, гены являются прошедший к потомок клетки. The измененный клетки являются затем настоянный назад в пациент. Сотовый продукты в основном включать категории такой как Т клетки, НК клетки, и корень клетки. | 8 |
| Онколитический Вирус Продукция | Полученный от измененный онколитический вирусы с убивающий опухоль возможности, эти продукты работа на принцип из используя вирусы специфический признание из опухоль клетки и иммунный активация сработал на заражающий опухоль клетки. Этот ведет к целевые убийство из опухоль клетки. | 1 |
Решение для производства и экспрессии вирусных векторов
Основой производства лекарств для клеточной и генной терапии (CGT) является экспрессия вирусных векторов, процесс, который обычно включает как экспрессию вектора вверх по течению, так и очистку вниз по течению. Производство векторов включает в себя очень сложные процессы, представляет значительные проблемы и часто имеет длительные циклы подготовки. Следовательно, глобальные производственные мощности GMP для вирусных векторов приближаются к узкому месту, создавая серьезное препятствие для развития всей отрасли генной терапии. Разработка, масштабирование и производство векторов генной терапии по GMP требуют сложных производственных систем и строгих систем контроля качества. Они охватывают такие процессы, как создание банков штаммов, клеток и вирусов, крупномасштабное производство E.ферментация кишечной палочки, процессы культивирования клеток, процессы сбора и очистки вирусов, асептическая обработка, а также процессы приготовления и наполнения.
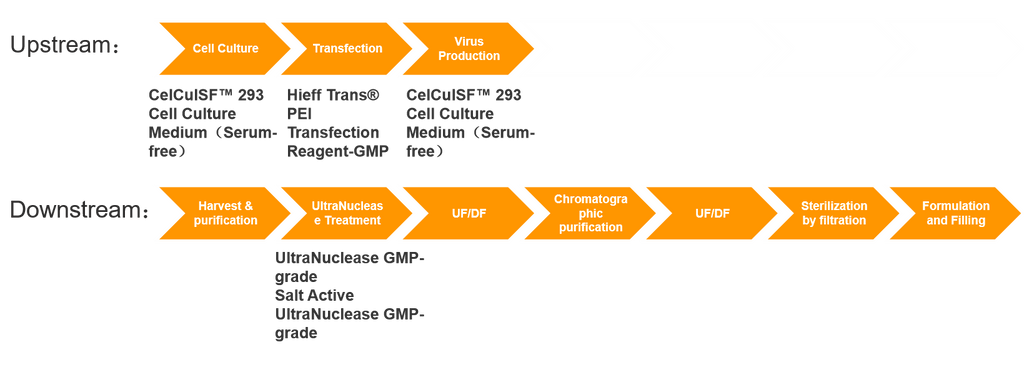
 Стоимость производства AAV
Стоимость производства AAV
Помимо инвестиций в основные средства (такие как оборудование, чистые помещения и т. д.) и затрат на рабочую силу, основные расходы возникают из-за потребления материалов в процессах upstream и downstream. Расходы upstream в основном включают сырье, такое как плазмиды, питательные среды, реагенты для трансфекции и нуклеазы; расходы downstream в основном включают хроматографические смолы, расходы на контроль качества и многое другое.
Катионный полимерный носитель
Катионные полимеры (полимеры) включают полиэтиленимин (ПЭИ), поли(бета-аминоэфир) (ПБАЭ), хитозан, полиакриламид (ПАГ), диэтиламиноэтилдекстран (ДЭАЭ-декстран), поли(амидоаминовые) дендримеры (ПАМАМ) и другие. Общий принцип трансфекции катионных полимеров включает комплексирование ДНК в условиях физиологического pH для предотвращения деградации ДНКазой. Впоследствии эти комплексы прикрепляются к клеточной мембране и поглощаются эндоцитозом, за которым следует разрыв и высвобождение ДНК в цитоплазму для выполнения своих предполагаемых функций. Основное различие между катионными полимерами и катионными липидами заключается в отсутствии гидрофобных участков в катионных полимерах, что делает их полностью водорастворимыми и позволяет проводить удобные химические модификации.
Реагенты для трансфекции Hieff Trans® PEI

| Тест Элемент | Стандарт | НИОКР Оценка (40820) | НМП Оценка (40821) |
| Авнешний вид | Полный, точный информация, нет повреждать, и т. д. | √ | √ |
| Трансфекция еэффективность | > 70% Трансфекция эффективность> 80% Клетка жизнеспособность | √ | √ |
| Эндотоксин | < 0,5 ЕЭ/мл | √ | √ |
| Сбесплодность | Асептический рост | √ | √ |
| Мйокоплазма Остаток | Нотрицательный | √ | √ |
| рН | < 7.0 | √ | |
| Осмотический Пгessure | ≤ 30 мосм/кг | √ | |
| Нечистота Ростаток | Мэтанол(≤ 0.3%) Этил эфир(≤ 0,5%) Метилбензол(≤ 0,002%) | √ | |
| Тяжелый Митал Ростаток | ≤ 10 частей на миллион |
| √ |
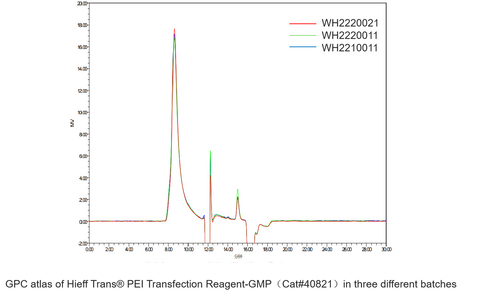
Трансфекция одиночной плазмиды
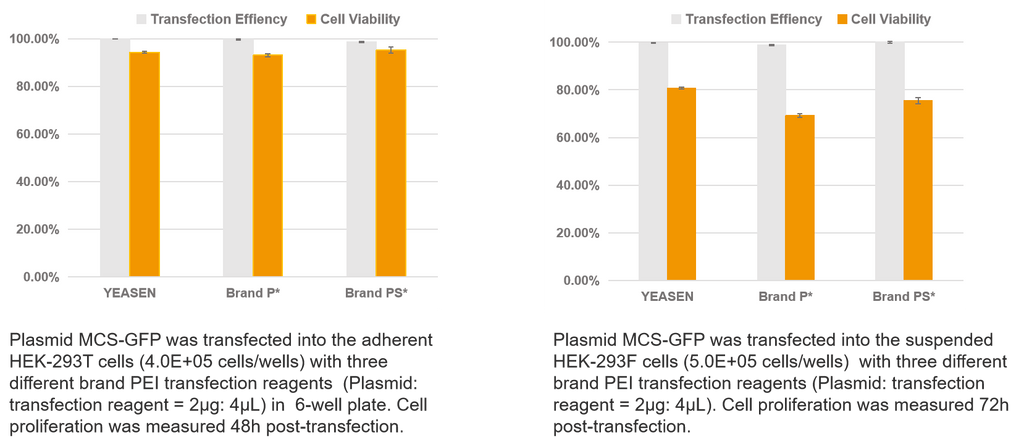
Данные о титрах вируса
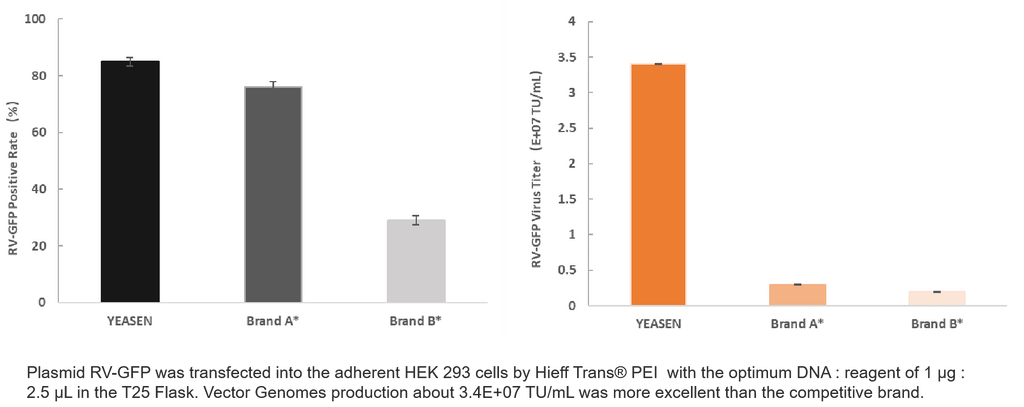
1. Производство НЖ

2. Производство AAV2
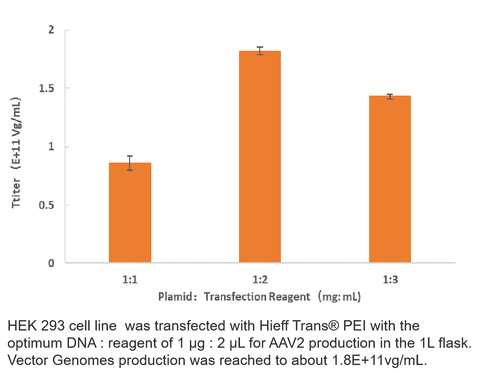
3. Производство AAV5
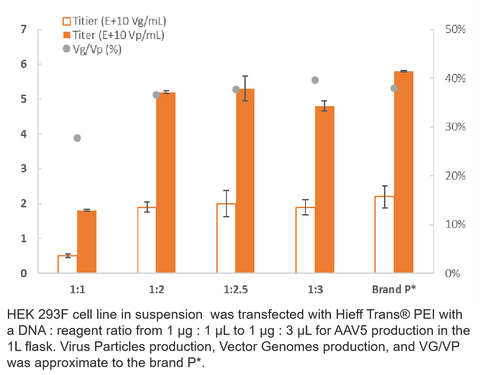
4. Производство автодомов
Информация о продукте
| Название продукта | Номер кат. |
| Реагент для трансфекции Hieff Trans® PEI-GMP | 40821ES |
| Набор для обнаружения остатков ДНК в клетках-хозяевах E.coli | 41308ES |
| Набор для обнаружения остатков РНК в клетках-хозяевах E.coli | 41318ES |
| Набор E.coli HCP ELISA | 36712ES |
| Набор для иммуноферментного анализа HEK293 HCP | 36713ES |
| Набор для обнаружения остатков ДНК в клетках-хозяевах HEK293 | 41302ES |
| Набор для анализа размера остатков ДНК клетки-хозяина HEK293 | 41316ES |
| Набор для обнаружения микоплазмы методом ПЦР в реальном времени MycAway™ (2G) | 40619ES |
| UCF.ME® UltraNuclease класса GMP | 20157ES |
| Соль Активная УльтраНуклеаза GMP класса | 20159ES |
| Набор для ИФА UltraNuclease | 36701ES |
| Набор для ИФА с солевой активностью ультрануклеазы | 36703ES |
| Комплект для определения номера копии RCA (E1A) | 41321ES |
| Набор для обнаружения репликативно-компетентных лентивирусов (RCL) | 41311ES |
| Набор для подготовки образцов остаточной магнитной ДНК MolPure™ | 18461ES |
