Hướng dẫn lựa chọn sản phẩm thuốc thử chuyển gen tế bào trong ống nghiệm
Thuốc thử chuyển gen tế bào đã trở thành thuốc thử thường quy để nghiên cứu và kiểm soát chức năng gen trong tế bào nhân chuẩn. Thuốc thử chuyển gen được sử dụng rộng rãi trong nghiên cứu chức năng gen, điều hòa biểu hiện gen và phân tích đột biến, cũng như liệu pháp gen, liệu pháp tế bào, sản xuất protein và sản xuất vắc-xin. Vậy chuyển gen là gì? Và làm thế nào để chọn loại thuốc thử chuyển gen dựa trên các thí nghiệm của bạn?
Có những loại chuyển gen nào?
Các tính năng của thuốc thử chuyển gen từ
Làm thế nào để chọn loại thuốc thử chuyển gen dựa trên thí nghiệm của bạn?
Trường hợp ứng dụng
Tài liệu tham khảo về điều kiện chuyển gen
Câu hỏi thường gặp
Xem xét Đọc
Có những loại chuyển gen nào?
Theo axit nucleic có tích hợp vào nhiễm sắc thể tế bào chủ sau khi chuyển gen hay không, nó được chia thành "tạm thời" (chuyển gen tạm thời) và "ổn định" (chuyển gen ổn định). Hiệu quả chuyển gen, độc tính tế bào, tác động đến sinh lý bình thường và mức độ biểu hiện gen của các phương pháp chuyển gen khác nhau là khác nhau. Các nguyên tắc, ứng dụng và đặc điểm được so sánh trong bảng sau:
Bảng 1 So sánh các phương pháp chuyển gen khác nhau
| Công nghệ | Nguyên tắc | Thuận lợi | Nhược điểm |
| Phương pháp chuyển gen hóa học | |||
| Liposome cationic | Liposome tích điện dương tạo thành phức hợp với nhóm phosphat tích điện âm của axit nucleic và được tế bào nội bào hóa. |
|
|
| Đồng kết tủa canxi phosphat | Các phức hợp DNA canxi phosphat hấp thụ vào màng tế bào và được tế bào nội bào hóa |
|
|
| Dextran | Phức hợp được hình thành bởi sự tương tác giữa DEAE-dextran tích điện dương và chuỗi phosphate tích điện âm của axit nucleic được tế bào nội bào hóa. |
|
|
| Các polyme cation khác | Polyme tích điện dương tạo thành phức hợp tích điện dương với nhóm phosphate tích điện âm của axit nucleic, sau đó tương tác với proteoglycan tích điện âm trên bề mặt tế bào và đi vào tế bào thông qua quá trình nội bào. |
|
|
| Phương pháp chuyển gen sinh học | |||
| Chuyển gen virus | Bản năng lây nhiễm tế bào và cung cấp vật liệu di truyền |
|
|
| Phương pháp chuyển gen vật lý | |||
| Chuyển điện | Điện áp xung cao làm gián đoạn điện thế màng tế bào và DNA được đưa vào qua các lỗ hình thành trên màng. |
|
|
| Truyền dẫn sinh học Phân phối hạt (Bắn phá hạt) | DNA được kết tủa bằng các hạt kim loại nặng cực nhỏ, sau đó các hạt phủ này được chiếu vào tế bào bằng thiết bị đạn đạo, DNA sẽ dần được giải phóng và biểu hiện trong tế bào. |
|
|
| tiêm vi mô | Kỹ thuật vi thao tác được sử dụng để tiêm DNA trực tiếp vào nhân của tế bào đích. |
|
|
Các tính năng của thuốc thử chuyển gen từ Yeasen
Đối với thuốc thử chuyển gen DNA và thuốc thử chuyển gen RNA,
| Thuốc thử chuyển gen Liposomal không chứa tế bào Hieff Trans™ Suspension | |
| 40802ES | 40805ES |
| Hieff Trans™ trong ống nghiệm Thuốc thử chuyển gen siRNA/miRNA | |
| 40806ES | 40816ES |
- Hiệu quả cao: phù hợp cho quá trình chuyển gen tạm thời hoặc chuyển gen ổn định cho các dòng tế bào.
- Độc tính thấp: Các tế bào được chuyển gen vẫn có khả năng sống tốt.
- Khả năng thích ứng rộng: bao phủ toàn diện các tế bào phổ biến và các tế bào sơ cấp khó chuyển gen.
- Dễ vận hành: phù hợp với môi trường có huyết thanh, không cần thay đổi môi trường trước và sau khi chuyển gen.
- Tiết kiệm chi phí: kinh tế và thiết thực, hiệu quả chuyển gen cao, giá thành thấp.
Làm thế nào để chọn loại thuốc thử chuyển gen dựa trên thí nghiệm của bạn?
Việc lựa chọn thuốc thử chuyển gen cần được thực hiện theo các mục đích thử nghiệm và nội dung thử nghiệm khác nhau, chẳng hạn như các chất được chuyển gen, tế bào cụ thể, sự tiện lợi khi vận hành và các yếu tố khác.
| Sản phẩm | Thuốc thử chuyển gen Liposomal không chứa tế bào Hieff Trans™ Suspension | Hieff Trans™ trong ống nghiệm Thuốc thử chuyển gen siRNA/miRNA | ||
| Loại tế bào | tế bào thông thường | tế bào thông thường | tế bào thông thường | tế bào thông thường |
| / | / | tế bào khó chuyển gen | tế bào khó chuyển gen | |
| Loại axit nucleic | ADN | ADN | / | ADN |
| siRNA | siRNA | siRNA | / | |
| / | / | miRNA | / | |
| / | / | bắt chước miRNA | / | |
| / | / | kháng miRNA | / | |
| Đồng chuyển gen DNA/siRNA | Đồng chuyển gen DNA/siRNA | / | / | |
| đóng gói virus | đóng gói virus | / | đóng gói virus |
Trường hợp ứng dụng
Thuốc thử chuyển gen Liposomal Hieff Trans™
Hieff Trans™ được cung cấp dưới dạng chất lỏng vô trùng. Nói chung, đối với quá trình chuyển gen trên đĩa 24 giếng, khoảng 1,5 μL mỗi lần, 1 mL Hieff Trans™ có thể thực hiện khoảng 660 lần chuyển gen; đối với đĩa 6 giếng, khoảng 6 μL mỗi lần, 1 mL Hieff Trans™ có thể thực hiện khoảng 660 lần chuyển gen. 160 lần chuyển gen;
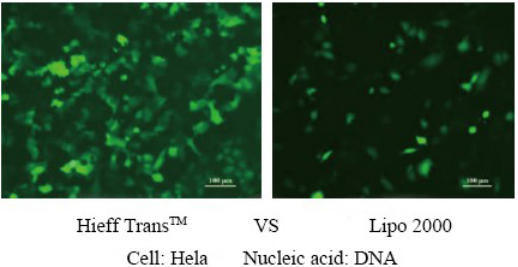
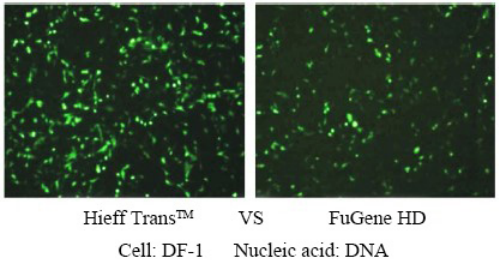
Để biết thêm chi tiết, vui lòng xem Sự tự tin trong quá trình chuyển gen với Thuốc thử Lipofectamine Hieff Trans™
Polyethylenimine tuyến tính (PEI) MW40000 (phân hủy nhanh)
PEI 40000 là một loại polymer cation tích điện cao với trọng lượng phân tử là 40.000 liên kết với các phân tử axit nucleic tích điện âm rất dễ dàng, tạo thành phức hợp và cho phép phức hợp này xâm nhập vào tế bào. PEI 40000 là thuốc thử chuyển gen tạm thời có độc tính tế bào thấp, hiệu quả chuyển gen cao và hiệu quả biểu hiện gen cao trong các tế bào như HEK293 và CHO. Thuốc thử chuyển gen PEI tuyến tính đã được xác nhận cho nhiều dòng tế bào bao gồm tế bào HEK-293, HEK293T, CHO-K1, COS-1, COS-7, NIH/3T3, Sf9, HepG2 và Hela. Hiệu quả chuyển gen cao tới 80%~90%.
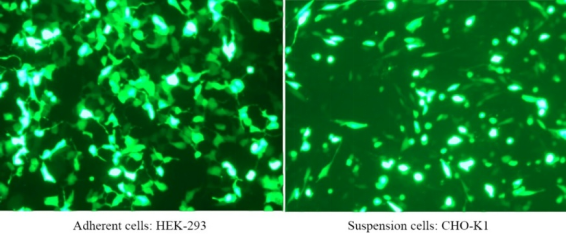
Để biết thêm chi tiết, vui lòng xem Sản phẩm ưa thích mới cho quá trình chuyển gen —— Linear PEI MW 40000, thuốc thử chuyển gen hiệu quả hơn
Hieff Trans™ trong ống nghiệm Thuốc thử chuyển gen siRNA/miRNA
Sản phẩm này có thể đạt hiệu quả biểu hiện trên 90% của 1 nM siRNA trong nhiều dòng tế bào, tránh các tác dụng ngoài mục tiêu. Thích hợp để chuyển gen nhiều loại tế bào, bao gồm Hela, MCF-7, HepG2, CHO và các tế bào bám dính khác; và các dòng tế bào huyền phù khó chuyển gen, chẳng hạn như tế bào K562 hoặc THP-1, có thể đạt hiệu quả im lặng 80%; Bao gồm một số tế bào chính, nguyên bào sợi người chính và tế bào gan người chính, v.v., có thể đạt hiệu quả im lặng 80%.
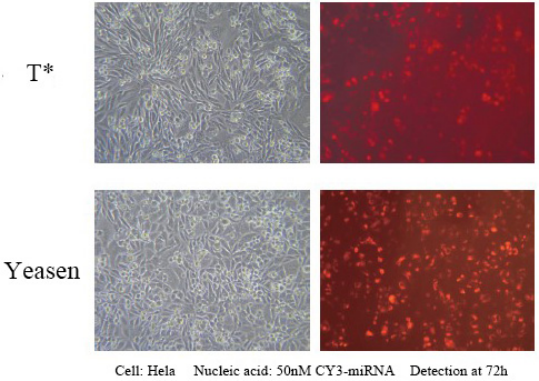
Tài liệu tham khảo về điều kiện chuyển gen
Ngoài hướng dẫn sử dụng của từng sản phẩm, khách hàng vận hành theo nội dung thử nghiệm cụ thể của mình, lượng sử dụng sẽ có sự khác biệt khác nhau. Theo điều kiện chuyển gen tế bào trong ống nghiệm do khách hàng báo cáo sau khi sử dụng sản phẩm, chúng tôi đã sắp xếp để bạn tham khảo.
| Tên sản phẩm/Số mặt hàng | |||||
| Tế bào | Bình nuôi cấy | Mật độ mạ tế bào | ADN | Hieff dịch | Hiệu quả chuyển gen |
| A549 | 6 giếng | 90% | 0,7 μg | 1,15 μL | +++ |
| BV 2 | 24 giếng | 95% | 0,2 μg | 0,2 μL | ++ |
| C2C12 | 24 giếng | 80% - 90% | 1 μg | 5 μL | ++ |
| DF 1 | 24 giếng | 80% - 90% | 0,5 μg | 0,5 μL | +++ |
| H520 | 6 giếng | 80% | 1.2μg | 6 μL | ++ |
| HaCaT | 96 giếng | 70% | 100 ng | 1 μL | ++ |
| HCT116 | 6 giếng | 90% | 4 μg | 10 μL | ++ |
| HEK293 | 6 giếng | 95% | 2 μg | 10 μL | 80 - 90% |
| HEK 293FT | 24 giếng | 85% | 1 μg | 4 μL | 90% |
| HEK293T | 12 giếng | 1×105 | 1 μg | 2 μL | +++ |
| HEK 293T(hệ thống treo) | 30ml | 80% | 30 μg | 60 μL | ++ |
| Hela | 12 giếng | 90% | 0,2μg | 0,6 μL | 90% |
| Hela | 12 giếng | 80% | 1 μg | 3 μL | +++ |
| HepG2 | 12 giếng | 80% | 1 μg | 3 μL | ++ |
| HUVEC | 24 giếng | 80% | 1 μg | 2 μL | ++ |
| MCF10A | Đĩa 10 cm | 60% | 5 μg | 15 μL | ++ |
| N2A | 24 giếng | 70% - 80% | 300 ng | 900 μL | + |
| NCI H1975 | 6 giếng | 80% | 4 μg | 10 μL | +++ |
| Viện Y tế Quốc gia 3T3 | 6 giếng | 90% | 4 μg | 10 μL | +++ |
| Nguyên bản 264.7 | Đĩa 35 mm | 80% | 1 μg | 2 μL | 90% |
| Vero | 6 giếng | 80% | 3 μg | 9 μL | +++ |
| Tế bào | Bình nuôi cấy | Mật độ mạ tế bào | siRNA | Hieff dịch | Hiệu quả chuyển gen |
| HK2 | 6 giếng | 65% | 100 giờ chiều | 6 μL | +++ |
Câu hỏi thường gặp
1 Thuốc thử chuyển gen Liposomal Hieff Trans™
1.1 Hỏi: Có thể sử dụng huyết thanh khi chuẩn bị phức hợp thuốc thử chuyển gen axit nucleic không?
A: Sự có mặt của huyết thanh sẽ ảnh hưởng đến sự hình thành liposome. Nên sử dụng môi trường không có huyết thanh (thường là môi trường MEM) khi chuẩn bị phức hợp thuốc thử chuyển gen axit nucleic.
1.2 Hỏi: Tôi cần lưu ý điều gì khi sử dụng Thuốc thử chuyển gen axit nucleic liposome Hieff Trans™?
MỘT:
1) Khi chuyển gen tế bào, mật độ tế bào tốt nhất là 80%-95% và mật độ mạ cụ thể được xác định theo tình trạng của tế bào;
2) Sử dụng DNA có độ tinh khiết cao giúp đạt hiệu quả chuyển gen cao hơn;
3) Các thuốc thử chuyển gen và DNA cần được pha loãng với môi trường không có huyết thanh khi chuẩn bị phức hợp chuyển gen;
4) Không được thêm kháng sinh vào môi trường trong quá trình chuyển gen;
5) Thuốc thử phải được bảo quản ở nhiệt độ 2-8°C, lưu ý tránh mở nắp nhiều lần trong thời gian dài;
6) Nồng độ DNA và số lượng thuốc thử liposome cation nên được tối ưu hóa cho lần sử dụng đầu tiên để đạt được hiệu quả chuyển gen tối đa. Tỷ lệ DNA so với thuốc thử chuyển gen thường được khuyến nghị là 1:2-1:3.
1.3 Hỏi: Có cần phải chấm dứt sau khi chuyển gen không?
A: Không cần. Phức hợp liposome ổn định trong 6 giờ. Nếu môi trường tế bào không thay đổi trước khi chuyển gen, để đảm bảo các chất dinh dưỡng cần thiết cho sự phát triển bình thường của tế bào, cần phải thay đổi môi trường mới sau 4-6 giờ. Tuy nhiên, nếu môi trường đã thay đổi trước khi chuyển gen, không cần phải thay đổi môi trường sau khi chuyển gen liposome.
1.4 Hỏi: Có thể thực hiện đồng chuyển gen DNA và siRNA không? Hiệu quả như thế nào?
A: Có, khi DNA và siRNA được đồng chuyển gen, hiệu quả chuyển gen siRNA sẽ kém hơn một chút.
1.5 Hỏi: Thuốc thử chuyển gen có thể được sử dụng để chuyển gen bao bì lentivirus không?
A: Có thể đóng gói bằng lentivirus.
1.6 Hỏi: Có thể chuyển gen tế bào huyền phù bằng Thuốc thử chuyển gen axit nucleic liposome Hieff Trans™ không?
A: Thuốc thử chuyển gen axit nucleic Liposome Hieff Trans™ có thể được sử dụng để chuyển gen tế bào treo, xem Giao thức để biết chi tiết. Ngoài ra, chúng tôi cũng giới thiệu một thuốc thử chuyển gen dành riêng cho tế bào treo (Mã số Cat.40805, Thuốc thử chuyển gen Liposomal không chứa tế bào Hieff Trans™ Suspension)
2 Hieff Trans™ trong ống nghiệm Thuốc thử chuyển gen siRNA/miRNA
2.1 Hỏi: Thuốc thử chuyển gen có cần phải thay đổi sau khi chuyển gen không?
A: Vấn đề này có thể chia thành hai trường hợp: 1. Nếu không thay đổi môi trường trước khi chuyển gen, môi trường nên được thay đổi khoảng 6 giờ sau khi chuyển gen để đảm bảo các chất dinh dưỡng cần thiết cho sự phát triển của tế bào; 2. Nếu có thay đổi môi trường trước khi chuyển gen, có thể vận hành theo hoạt động bình thường của tế bào nuôi cấy không? ? Sau khi thay đổi chất lỏng?
2.2 Hỏi: Thuốc thử chuyển gen có thể được đông lạnh không?
A: Không thể đông lạnh, vì thuốc thử chuyển gen là thuốc thử chuyển gen cation PEI. Đông lạnh ở nhiệt độ thấp sẽ phá hủy hoạt động của thuốc thử chuyển gen PEI. Do đó, tốt nhất là bảo quản ở nhiệt độ 2-8 °C để duy trì hiệu quả chuyển gen tốt nhất.
Thông tin sản phẩm
| Tên sản phẩm | Mã sản phẩm | Thông số kỹ thuật |
| Thuốc thử chuyển gen Liposomal Hieff Trans™ | 40802ES02 | 0,5ml |
| 40802ES03 | 1,0mL | |
| 40802ES08 | 5×1mL | |
| Thuốc thử chuyển gen Liposomal không chứa tế bào Hieff Trans™ Suspension (Yêu cầu) | 40805ES02 | 0,5ml |
| 40805ES03 | 1,0mL | |
| 40805ES08 | 5×1 mL | |
| Hieff Trans™ trong ống nghiệm Thuốc thử chuyển gen siRNA/miRNA (Hỏi) | 40806ES02 | 0,5ml |
| 40806ES03 | 1,0mL | |
| Polyethylenimine Linear (PEI) MW40000(phân hủy nhanh) | 40816ES02 | 100mg |
| 40816ES03 | 1g | |
| 40816ES08 | 5×1g |
Một số bài viết được xuất bản bằng sản phẩm của chúng tôi
[1] Liu R, Yang J, et al. Kiểm soát quang di truyền chức năng và chuyển hóa RNA bằng cách sử dụng các protein liên kết RNA có thể chuyển đổi ánh sáng được thiết kế. Nat Biotechnol. 2022 ngày 3 tháng 1. (IF:55)
[2] Luo J, Yang Q, et al. TFPI là thụ thể hốc ruột kết cho TcdB từ nhánh siêu độc lực 2 C. difficile. Tế bào. 2022 ngày 17 tháng 3.(IF:41.582)
[3] Zhou J, Chen P, et al. Các biến thể Cas12a được thiết kế để giảm tác động ngoài mục tiêu trên toàn bộ hệ gen thông qua nhận dạng PAM nghiêm ngặt. Mol Ther. 2022 5 tháng 1.(IF:11.454)
[4] Chen S, Cao X, et al. circVAMP3 thúc đẩy quá trình tách pha CAPRIN1 và ức chế ung thư biểu mô tế bào gan bằng cách ức chế quá trình dịch mã c-Myc. Adv Sci (Weinh). 24 tháng 1 năm 2022.(IF:16.808)
[5] Gu C, Wang Y, et al. AHSA1 là một mục tiêu điều trị đầy hứa hẹn cho sự tăng sinh tế bào và khả năng kháng thuốc ức chế proteasome ở bệnh đa u tủy. J Exp Clin Cancer Res. 2022 ngày 6 tháng 1.(IF:11.161)
[6] Zhang Y, Yu X, et al. Yếu tố ghép nối arginine/serine-rich 8 thúc đẩy bệnh ác tính đa u tủy và tổn thương xương thông qua ghép nối thay thế của CACYBP và giao tiếp tế bào dựa trên exosome. Clin Transl Med. 2022 tháng 2 (IF:11.492)
[7] Qin J, Cai Y, et al. Cơ chế phân tử của chủ vận và chủ vận ngược trong thụ thể ghrelin. Nat Commun. 2022 ngày 13 tháng 1.(IF:14.9)
[8] Tang X, Deng Z, và cộng sự.Một loại protein mới được mã hóa bởi circHNRNPU thúc đẩy sự tiến triển của bệnh đa u tủy bằng cách điều chỉnh vi môi trường tủy xương và ghép nối thay thế. J Exp Clin Cancer Res. 2022 ngày 8 tháng 3 (IF:11.161)
[9] Xie F, Su P, et al. Kỹ thuật các túi ngoại bào được làm giàu bằng ACE2 được palmitoylated như liệu pháp điều trị COVID-19. Adv Mater. 19 tháng 10 năm 2021. (IF:30.849)
[10] Liang Y, Lu Q, et al. Tái kích hoạt chất ức chế khối u trong ung thư vú bằng cách chuyển đổi tăng cường thông qua mạng NamiRNA. Nucleic Acids Res. 2021 ngày 7 tháng 9.(IF:16.9)
[11] Fan Y, Wang J, et al. CircNR3C2 thúc đẩy hiệu ứng ức chế khối u do HRD1 làm trung gian thông qua việc hấp thụ miR-513a-3p trong ung thư vú ba âm tính. Mol Cancer. 2021 tháng 2 ngày 2.(IF:27.403)
[12] Dai L, Dai Y, et al. Hiểu biết sâu sắc về cấu trúc vào quá trình tuyển dụng phức hợp BRCA1-BARD1 vào chromatin bị hư hỏng. Mol Cell. 2021 1 tháng 7.(IF:17.97)
[13] Zhang K, Wang A, et al. Trục UBQLN2-HSP70 làm giảm các tập hợp poly-Gly-Ala và làm giảm các khiếm khuyết về hành vi ở mô hình động vật C9ORF72. Neuron. 2021 ngày 16 tháng 6.(IF:17.17)
[14] Li T, Chen X, et al. Một thiết bị quang di truyền dựa trên BRET tổng hợp để biểu hiện gen chuyển mạch xung cho phép cân bằng glucose ở chuột. Nat Commun. 27 tháng 1 năm 2021.(IF:14.92)
[15] Yan F, Huang C, et al. Threonine ADP-Ribosylation của Ubiquitin bởi một họ tác nhân vi khuẩn ngăn chặn Ubiquitin hóa vật chủ. Mol Cell. 21 tháng 5 năm 2020.(IF:17.97)
[16] Sun X, Peng X, et al. ADNP thúc đẩy sự phân hóa thần kinh bằng cách điều chỉnh tín hiệu Wnt/β-catenin. Nat Commun. 2020 ngày 12 tháng 6.(IF:14.911)
[17] Yang X, Wang H, et al. Việc nối lại tín hiệu ERBB3 và ERK mang lại khả năng kháng ức chế FGFR1 ở ung thư đường tiêu hóa có đột biến ERBB3-E928G. Protein Cell. Tháng 12 năm 2020 (IF:14.872)
[18] Zou Y, Wang A, et al. Phân tích cảnh quan và động lực oxy hóa khử trong tế bào sống và trong cơ thể sống bằng cách sử dụng các cảm biến huỳnh quang được mã hóa di truyền. Nat Protoc. 2018 tháng 10 (IF:13.490)
[19] Hao H, Hu S, et al. Mất CXCR7 nội mô làm suy yếu cân bằng mạch máu và tái tạo tim sau nhồi máu cơ tim: Ý nghĩa đối với việc khám phá thuốc tim mạch. Tuần hoàn. 28 tháng 3 năm 2017.(IF:29,69)
