Cellterapi avser användning av biotekniska metoder för att erhålla celler med specifika funktioner, som sedan förstärks genom processer som ex vivo expansion och specialiserad odling. Dessa celler är utrustade med förstärkta immunsvar, patogen- och tumörcelldödande kapacitet och andra funktioner för att uppnå de terapeutiska målen för vissa sjukdomar. Genterapi hänvisar till det terapeutiska tillvägagångssättet att modifiera individuellt genuttryck eller reparera defekta gener genom metoder som gentillägg, genmodifiering och gentystnad. Det yttersta målet är att bota sjukdomar genom att rätta till onormala gener.
| Produkt Typer | Beskrivning | Antal av Godkänd Narkotika Över hela världen |
| Gen Terapi Vektor Produkter | Dessa produkter utnyttja gen terapi vektorer till leverera terapeutisk gener till specifik celler i de patientens vävnader, sikta för de uttryck eller reglering av terapeutisk proteiner. Detta kategori förlitar sig på de leverans av gen terapi vektorer. | 2 |
| Cellulär Produkter | Använder integrera viral vektorer (sådan som lentiviral vektorer), gener är infördes till föregångare celler eller stam cell genom under ex vivo villkor. Som celler dela, de gener är godkänd till ättling celler. De ändrad celler är sedan infunderas tillbaka till de patient. Cellulär produkter huvudsakligen omfatta kategorier sådan som T celler, NK celler, och stam celler. | 8 |
| Onkolytisk Virus Produkter | Härledd från ändrad onkolytisk virus med tumördödande förmågor, dessa produkter arbete på de princip av använda de virus specifik erkännande av tumör celler och de immun aktivering utlöstes på infekterar tumör celler. Detta leder till målinriktad dödande av tumör celler. | 1 |
Viral vektorproduktion och uttryckslösning
Kärnan i cell- och genterapiläkemedelsproduktionen (CGT) ligger i uttrycket av virala vektorer, en process som vanligtvis involverar både uppströms vektoruttryck och nedströmsrening. Vektorproduktion involverar mycket komplexa processer, innebär betydande utmaningar och har ofta långa förberedelsecykler. Följaktligen närmar sig den globala GMP-produktionskapaciteten för virala vektorer en flaskhals, vilket utgör ett stort hinder för hela genterapiindustrins utveckling. Utvecklingen, uppskalningen och GMP-produktionen av genterapivektorer involverar intrikata produktionssystem och stränga kvalitetskontrollsystem. Dessa omfattar processer som stam-, cell- och virusbanksetablering, storskalig E.coli-fermentering, cellodlingsprocesser, virusskörd och reningsprocesser, aseptisk bearbetning och formulerings- och fyllningsprocesser.
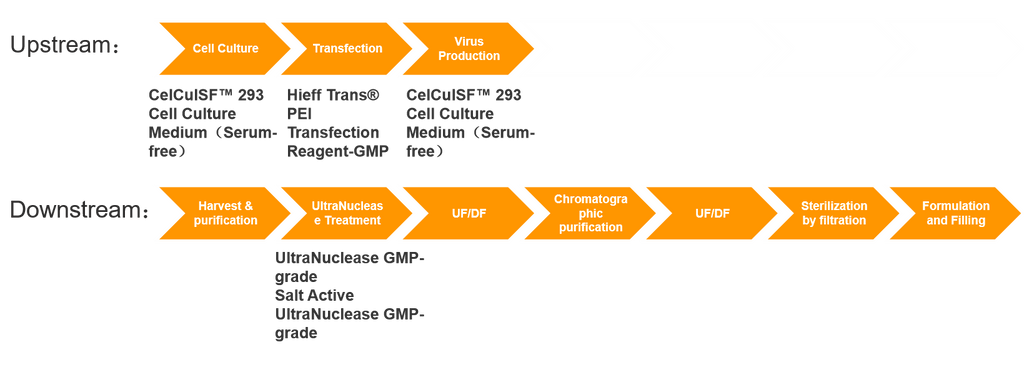
 AAV Produktionskostnader
AAV Produktionskostnader
Bortsett från investeringar i anläggningstillgångar (såsom utrustning, renrum etc.) och arbetskostnader härrör de huvudsakliga kostnaderna från materialförbrukning i uppströms- och nedströmsprocesserna. Uppströmskostnader omfattar huvudsakligen råmaterial som plasmider, odlingsmedier, transfektionsreagenser och nukleaser; Nedströmskostnader inkluderar huvudsakligen kromatografihartser, kostnader för kvalitetskontroll och mer.
Katjonisk polymerbärare
Katjoniska polymerer (polymerer) inkluderar polyetylenimin (PEI), poly(beta-aminoester) (PBAE), kitosan, polyakrylamid (PAH), dietylaminoetyldextran (DEAE-dextran), poly(amidoamin) dendrimerer (PAMAM) och andra. Den vanliga principen för katjonisk polymertransfektion involverar komplexbildning av DNA under fysiologiska pH-förhållanden för att förhindra nedbrytning av DNas. Därefter fäster dessa komplex till cellmembranet och tas upp av endocytos, följt av bristning och frisättning av DNA i cytoplasman för att utöva sina avsedda funktioner. Den primära skillnaden mellan katjoniska polymerer och katjoniska lipider ligger i frånvaron av hydrofoba delar i katjoniska polymerer, vilket gör dem helt vattenlösliga och möjliggör bekväma kemiska modifieringar.
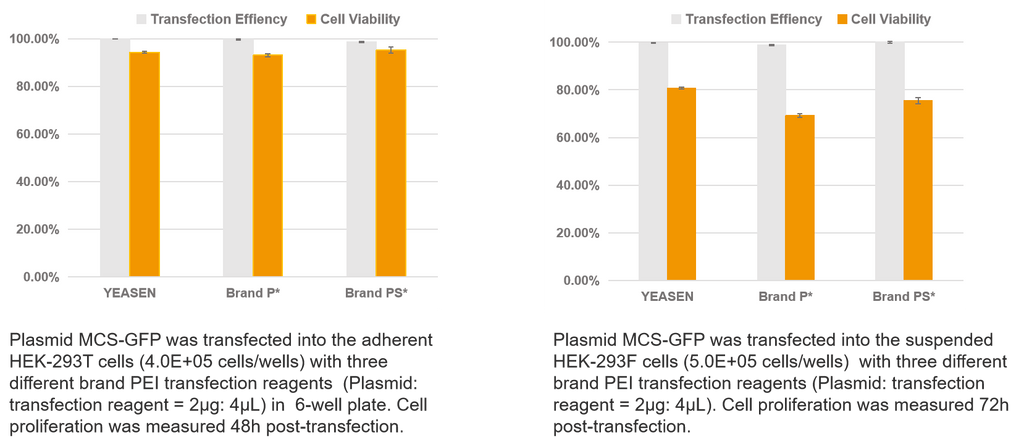
Hieff Trans® PEI-transfektionsreagenser

| Testa Punkt | Standard | FoU Kvalitet (40820) | GMP Kvalitet (40821) |
| Autseende | Komplett, exakt information, inga skada, etc | √ | √ |
| Transfektion eeffektivitet | > 70 % Transfektion effektivitet> 80 % Cell livskraft | √ | √ |
| Edotoxin | < 0,5 EU/ml | √ | √ |
| Sterilitet | Aseptisk tillväxt | √ | √ |
| Mykoplasma Återstod | Negativ | √ | √ |
| pH | < 7,0 | √ | |
| Osmotisk Pressure | ≤ 30 mOsm/kg | √ | |
| Förorening Råterstod | Metanol(≤ 0.3 %) Etyl eter(≤ 0,5 %) Metylbensen(≤ 0,002 %) | √ | |
| Tung Metal Råterstod | ≤ 10 ppm |
| √ |
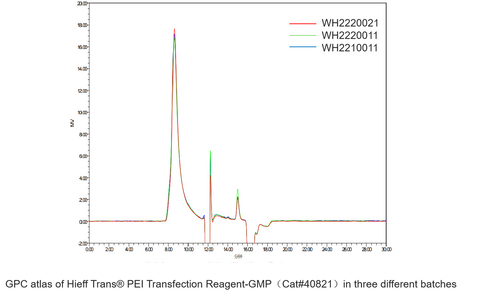
Transfektion av enkel plasmid
Virus Titer Data
1. LV Produktion

2. AAV2 produktion
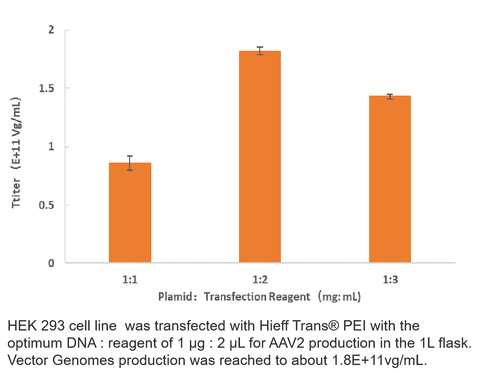
3. AAV5 produktion
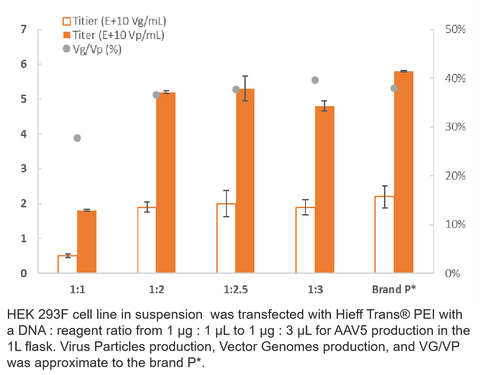
4. Husbilsproduktion
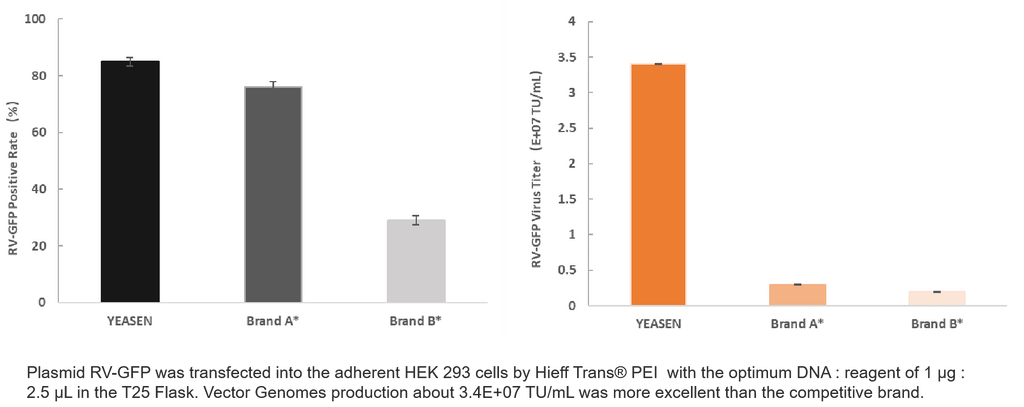
Produktinformation
| Produktnamn | Katt nr. |
| Hieff Trans® PEI Transfektionsreagens-GMP | 40821ES |
| E.coli värdcells-DNA-restdetektionskit | 41308ES |
| E.coli Host Cell RNA Residue Detection Kit | 41318ES |
| E.coli HCP ELISA-kit | 36712ES |
| HEK293 HCP ELISA kit | 36713ES |
| HEK293 värdcells-DNA-restdetektionskit | 41302ES |
| HEK293 värdcellsrester DNA-storleksanalyssats | 41316ES |
| MycAway™ Mycoplasma qPCR-detektionssats i realtid (2G) | 40619ES |
| UCF.ME® UltraNuclease GMP-kvalitet | 20157ES |
| Salt Active UltraNuclease GMP-grade | 20159ES |
| UltraNuclease ELISA Kit | 36701ES |
| Salt Active UltraNuclease ELISA Kit | 36703ES |
| RCA (E1A) Kopianummer Detektionskit | 41321ES |
| Replikationskompetent Lentivirus (RCL) Detection Kit | 41311ES |
| MolPure™ Magnetic Residual DNA Sample Preparation Kit | 18461ES |
