Celleterapi refererer til brugen af bioteknologiske metoder til at opnå celler med specifikke funktioner, som derefter forbedres gennem processer som ex vivo ekspansion og specialiseret dyrkning. Disse celler er udstyret med forstærkede immunresponser, patogen- og tumorcelledræbende evner og andre funktioner til at nå de terapeutiske mål for visse sygdomme. Genterapi refererer til den terapeutiske tilgang til at modificere individuel genekspression eller reparere defekte gener gennem metoder som genaddition, genmodifikation og gendæmpning. Det ultimative mål er at helbrede sygdomme ved at rette op på unormale gener.
| Produkt Typer | Beskrivelse | Antal af Godkendt Narkotika På verdensplan |
| Gene Terapi Vektor Produkter | Disse produkter udnytte gen terapi vektorer til levere terapeutisk gener til bestemt celler i de patientens væv, sigte for de udtryk eller regulering af terapeutisk proteiner. Denne kategori stoler på på de levering af gen terapi vektorer. | 2 |
| Cellulær Produkter | Bruger integrere viral vektorer (sådan som lentiviral vektorer), gener er indført til forløber celler eller stilk celle genomer under eks vivo forhold. Som celler dele, de gener er bestået til efterkommer celler. De modificeret celler er så infunderet tilbage til de patient. Cellulær produkter hovedsagelig omfatte kategorier sådan som T celler, NK celler, og stilk celler. | 8 |
| Onkolytisk Virus Produkter | Afledt fra modificeret onkolytisk vira med tumor-dræbende kapaciteter, disse produkter arbejde på de princip af udnytter de virus bestemt anerkendelse af svulst celler og de immun aktivering udløst på inficerer svulst celler. Denne fører til målrettet drab af svulst celler. | 1 |
Viral vektorproduktion og -ekspressionsløsning
Kernen i celle- og genterapi-lægemiddelproduktion (CGT) ligger i ekspressionen af virale vektorer, en proces, der typisk involverer både opstrøms vektorekspression og nedstrøms oprensning. Vektorproduktion involverer meget komplekse processer, giver betydelige udfordringer og har ofte lange forberedelsescyklusser. Følgelig nærmer den globale GMP-produktionskapacitet for virale vektorer sig en flaskehals, hvilket udgør en stor hindring for hele genterapiindustriens udvikling. Udvikling, opskalering og GMP-produktion af genterapivektorer involverer indviklede produktionssystemer og strenge kvalitetskontrolsystemer. Disse omfatter processer såsom etablering af stamme-, celle- og virusbanker, E.coli-fermentering, cellekulturprocesser, virushøst- og oprensningsprocesser, aseptisk behandling og formulerings- og påfyldningsprocesser.
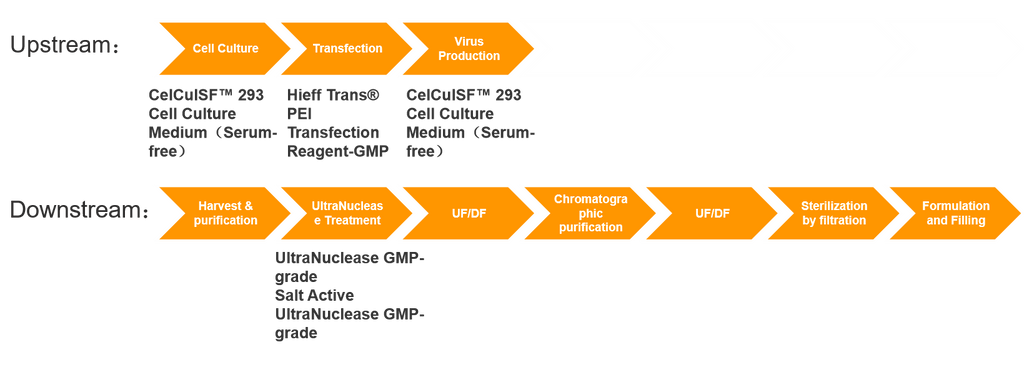
 AAV Produktionsomkostninger
AAV Produktionsomkostninger
Bortset fra investeringer i anlægsaktiver (såsom udstyr, renrum osv.) og lønomkostninger stammer hovedudgifterne fra materialeforbrug i upstream- og downstream-processerne. Opstrømsomkostninger involverer hovedsageligt råmaterialer som plasmider, kulturmedier, transfektionsreagenser og nukleaser; downstream-omkostninger omfatter hovedsageligt kromatografiharpikser, kvalitetskontroludgifter og mere.
Kationisk polymerbærer
Kationiske polymerer (polymerer) inkluderer polyethylenimin (PEI), poly(beta-aminoester) (PBAE), chitosan, polyacrylamid (PAH), diethylaminoethyldextran (DEAE-dextran), poly(amidoamin) dendrimerer (PAMAM) og andre. Det almindelige princip for kationisk polymertransfektion involverer kompleksdannelse af DNA under fysiologiske pH-betingelser for at forhindre nedbrydning af DNase. Efterfølgende binder disse komplekser sig til cellemembranen og optages ved endocytose, efterfulgt af brud og frigivelse af DNA til cytoplasmaet for at udøve deres tilsigtede funktioner. Den primære skelnen mellem kationiske polymerer og kationiske lipider ligger i fraværet af hydrofobe dele i kationiske polymerer, hvilket gør dem fuldstændigt vandopløselige og muliggør praktiske kemiske modifikationer.
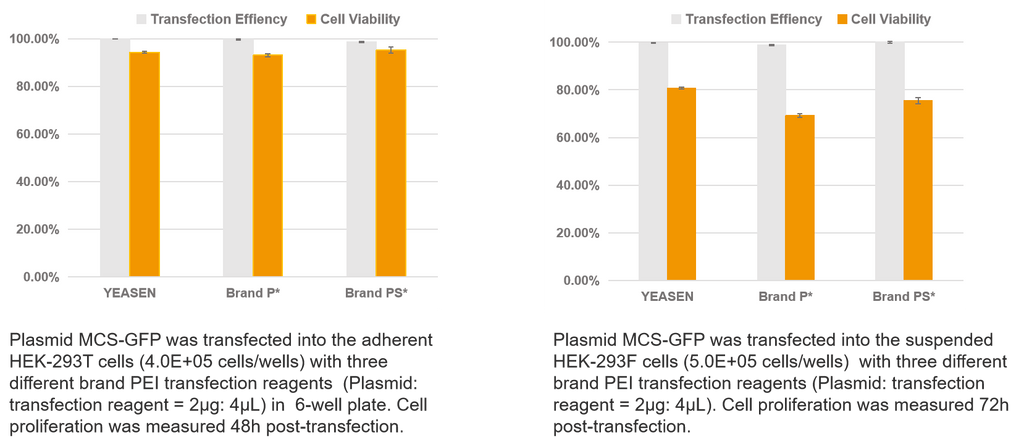
Hieff Trans® PEI-transfektionsreagenser

| Prøve Punkt | Standard | R&D Grad (40820) | GMP Grad (40821) |
| ENudseende | Komplet, nøjagtig information, ingen skade, osv | √ | √ |
| Transfektion eeffektivitet | > 70 % Transfektion effektivitet> 80 % Celle levedygtighed | √ | √ |
| Endotoksin | < 0,5 EU/ml | √ | √ |
| Sterilitet | Aseptisk vækst | √ | √ |
| Mycoplasma Rest | Negativ | √ | √ |
| pH | < 7,0 | √ | |
| Osmotisk Pressure | ≤ 30 mOsm/kg | √ | |
| Urenhed Rrest | Methanol (≤ 0.3 %) Ethyl æter (≤ 0,5 %) Methylbenzen (≤ 0,002 %) | √ | |
| Tung Metal Rrest | ≤ 10 ppm |
| √ |
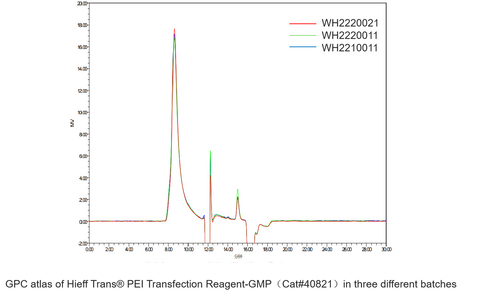
Transfektion af enkelt plasmid
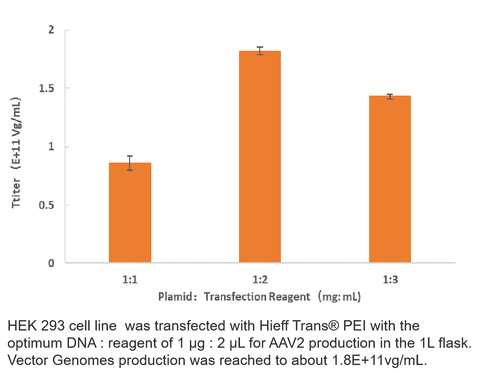
Virus Titer Data
1. LV Produktion

2. AAV2 produktion
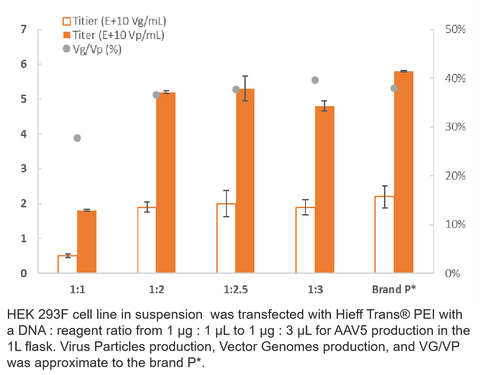
3. AAV5 produktion
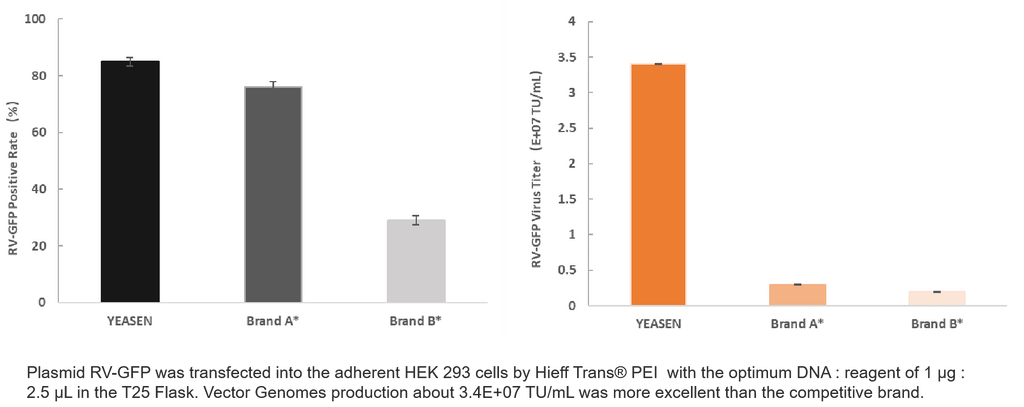
4. RV Produktion
Produktinformation
| Produktnavn | Kat nr. |
| Hieff Trans® PEI Transfektionsreagens-GMP | 40821ES |
| E.coli værtscelle DNA-restdetektionskit | 41308ES |
| E.coli værtscelle RNA-restdetektionskit | 41318ES |
| E.coli HCP ELISA kit | 36712ES |
| HEK293 HCP ELISA kit | 36713ES |
| HEK293 Værtscelle DNA-restdetektionskit | 41302ES |
| HEK293 Værtscellerest DNA-størrelsesanalysesæt | 41316ES |
| MycAway™ Mycoplasma qPCR-detektionssæt i realtid (2G) | 40619ES |
| UCF.ME® UltraNuclease GMP-kvalitet | 20157ES |
| Salt Active UltraNuclease GMP-kvalitet | 20159ES |
| UltraNuclease ELISA Kit | 36701ES |
| Salt Active UltraNuclease ELISA Kit | 36703ES |
| RCA (E1A) Kopinummer Detection Kit | 41321ES |
| Replikationskompetent Lentivirus (RCL) detektionskit | 41311ES |
| MolPure™ Magnetic Residual DNA Sample Preparation Kit | 18461ES |
