Les progrès rapides de la biotechnologie ont eu un impact considérable sur la lutte contre les maladies infectieuses comme la COVID-19 grâce à la création de vaccins à ARNm produits par une technologie de synthèse d’ARN in vitro. De nombreuses entreprises, dont Moderna aux États-Unis, CureVac en Allemagne et BioNTech en Allemagne, ont non seulement développé des vaccins thérapeutiques à ARNm, mais également des traitements contre des maladies telles que les tumeurs, les maladies infectieuses et les maladies chroniques.
La recherche et la formulation de vaccins à ARNm nécessitent une gamme variée de matières premières pour assurer leur développement réussi. En tant que pionnier dans l'industrie des enzymes moléculaires, Yeasen a réussi à créer divers enzymes et réactifs moléculaires grâce à la biotechnologie avancée des enzymes moléculaires et aux techniques de fermentation et de purification des protéines à grande échelle.
Pour garantir à la fois la qualité des produits et la capacité de production, Yeasen a établi une usine de production de niveau GMP à Wuhan, capable de satisfaire pleinement aux exigences de production à l'échelle industrielle avec une capacité annuelle supérieure à 5 milliards d'unités. De plus, Yeasen est la première entreprise chinoise à obtenir la certification ISO 13485 pour la recherche, le développement, la fabrication et la distribution d'enzymes moléculaires. Cette certification garantit la qualité, la cohérence et la traçabilité de tous leurs réactifs.
1. Avantage des BPF
2. Yeasen peut fournir des produits de qualité GMP
3. Yeasen a acquis des numéros DMF pour de nombreux produits
4. Scénarios d'application des produits Yeasen
5. Matières premières pour la préparation du vaccin à ARNm fournies par Yeasen
6. Informations de commande
1. Avantage des BPF
« Qualité GMP » est un terme de marque utilisé par Yeasen pour décrire les réactifs fabriqués dans des installations certifiées ISO 13485. Les réactifs de qualité GMP de Yeasen sont produits conformément aux normes du système de gestion de la qualité ISO 13485 et avec des contrôles de processus plus stricts et des dossiers de documentation complets. Yeasen peut non seulement proposer des réactifs de haute qualité, mais également fournir des documents, des audits de site et d'autres formes d'assistance à nos clients.
Tableau 1. Avantage des BPF
| Contrôles de qualité | Niveau de recherche | Qualité GMP |
| Sans animaux | Des matières d'origine animale peuvent être utilisées | Des certificats sans animaux peuvent être fournis si nécessaire |
| Caractérisation des banques cellulaires | Moins strict | Rigoureux (conforme aux réglementations GMP) |
| Informations de traçabilité des matières premières et du produit fini | Moins strict | Rigoureux (conforme aux réglementations GMP) |
| Contrôle du niveau d'endotoxines | / | Strict |
| Contrôle stérile | / | Strict |
| Dossiers de lots pour la fabrication et les tests | Moins strict | Rigoureux (des enregistrements de lots peuvent être fournis si nécessaire) |
| Rapport de validation du processus | / | Le rapport peut être fourni si nécessaire |
| Système de contrôle des changements | Auto-évaluation | Rigoureux (conforme aux réglementations GMP) |
| Système de gestion de la qualité | Auto-évaluation | Certification ISO 13485 |
| Numéro DMF | / | Oui (signalement) |
2. Yeasen peut fournir des produits de qualité GMP
S'appuyant sur une vaste expertise et une excellence technique dans le développement d'enzymes et la production à l'échelle industrielle, Yeasen a mis en place une installation de pointe connue sous le nom de « mRNAtools ». Cette installation, d'une superficie de 50 000 pieds carrés, adhère aux réglementations GMP et dispose de fonctionnalités de pointe, notamment 2 unités de fermentation automatisées de 1 500 L, des équipements de purification à grande échelle et des capacités de lyophilisation. mRNAtools se consacre à la fourniture de réactifs rigoureux qui s'alignent sur les exigences de production et de réglementation des clients.
L'usine de production d'enzymes moléculaires de Yeasen, spécialement conçue pour les produits de qualité GMP, garantit la qualité des produits au niveau matériel et logiciel. Elle comprend une équipe hautement qualifiée de 70 professionnels, chacun possédant une vaste expérience de la production GMP. Les opérations d'entreposage et de logistique sont modulaires, garantissant le stockage sûr et le transport efficace des produits. Un réseau de distribution multicentrique à l'échelle nationale garantit en outre un cycle d'approvisionnement fiable.
3. Yeasen a acquis des numéros DMF pour de nombreux produits
Les dossiers de médicaments (DMF) sont des documents confidentiels soumis volontairement à la Food & Drug Administration (FDA) des États-Unis. Ils contiennent des informations détaillées sur les installations, les processus ou les articles utilisés dans la production, le traitement, le conditionnement et le stockage des médicaments à usage humain.
La FDA examine le contenu technique d'un DMF lorsqu'un fabricant d'ingrédients pharmaceutiques actifs (API) y fait référence pour étayer sa demande de nouveau médicament expérimental (IND), sa demande de nouveau médicament (NDA), sa demande abrégée de nouveau médicament (ANDA) ou sa demande d'exportation. Les DMF jouent un rôle essentiel dans ces demandes.Lorsque les fabricants déposent des DMF pour des matériaux spécifiques, le processus d’approbation de la FDA peut être considérablement accéléré.
Yeasen possède des fichiers DMF qui peuvent simplifier les délais des projets. Si vous le souhaitez, vous pouvez demander une autorisation de référence à nos DMF pour appuyer votre demande auprès de la FDA. Pour lancer l'autorisation de référence de nos DMF, veuillez soumettre une demande de lettre d'autorisation à Yeasen, en nous demandant de fournir une lettre d'autorisation DMF spécifique au centre de la FDA.
4. Scénarios d'application des produits Yeasen
4.1 Génération de modèles
La linéarisation des plasmides est une étape indispensable lors de la génération de modèles lorsque des vecteurs plasmidiques sont utilisés comme modèles de transcription. Au fur et à mesure que la transcription se poursuit jusqu'à la fin des modèles d'ADN, la linéarisation des plasmides garantit la génération de transcrits d'ARN d'une longueur et d'une séquence définies. Yeasen propose diverses enzymes de restriction pour répondre à vos besoins. Nous vous recommandons de sélectionner des enzymes de restriction qui génèrent des extrémités franches ou des surplombs 5'.
4.2 In vitro Transcription (IVT)
La transcription in vitro est affectée par divers facteurs. Les enzymes, les tampons et les substrats modifiés ont tous un impact important sur l’efficacité de la transcription.
Sur la base de la plateforme ZymeEditor, YEASEN Biotech a développé de nouvelles ARN polymérases T7 qui réduisent considérablement la génération d'ARNdb au cours du processus de transcription in vitro (IVT) (ARN polymérase T7, faible ARN ds, 250 U/μL). Il réduit considérablement l'immunogénicité de l'ARNm et, dans une certaine mesure, améliore l'intégrité de l'ARNm. Ce développement devrait jouer un rôle crucial dans l'avancement du développement de vaccins à ARNm et de médicaments contre le cancer.

En optimisant le tampon et en ajustant le type de sel du substrat nucléotidique, nous avons considérablement amélioré l’efficacité de la transcription et réduit la production d’ARNdb.

Figure 2. Le Tris NTP peut grandement améliorer l'efficacité du lVT et réduire la production d'ARNdb
4.3 Coiffage de l'ARNm
Comme une structure de coiffe 5' réduit l'immunogénicité et est nécessaire à une traduction efficace des ARNm, l'ajout de structures de coiffe aux extrémités 5' de l'ARNm généré par la transcription est nécessaire.
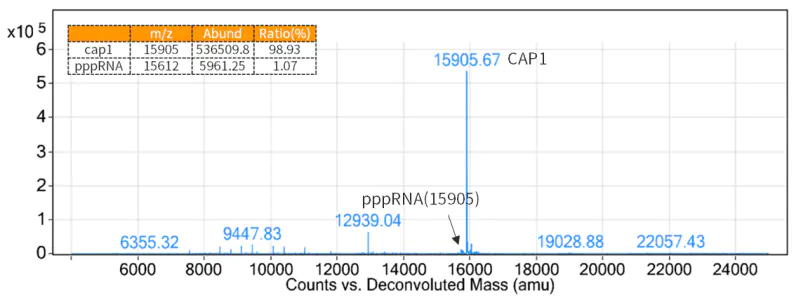
Figure 3. Résultats de la détection du taux de capsulage (détection LC-MS)
4.4 Purification de l'ARNm
La purification est une étape indispensable pour obtenir des ARNm de haute pureté.
5. Matières premières pour la préparation du vaccin à ARNm fournies par Yeasen
À l'heure actuelle, Yeasen peut fournir un ensemble complet de produits dans le processus de production de solutions mères d'ARNm. Les produits sont strictement contrôlés par la production GMP et répondent pleinement aux exigences de la production de vaccins à ARNm.
Tableau 2.Matières premières pour la préparation du vaccin à ARNm fournies par Yeasen
| Préparation du modèle | Transcription in vitro | ||
| 10164ES | 10623ES | ||
| 10122ES | 10625ES | ||
| 10922ES | 10672ES | ||
| 10300ES | 10621ES | ||
|
| 10611ES | ||
| 10661ES | 10133ES | ||
| ARNase R (20U/uL) | 14615ES | 10650ES | |
| Xba I | 10662ES | 10651ES | |
| Capsulage |
| Purification |
|
| 10614ES | 12602ES | ||
| 10612ES | Support de séparation magnétique | 80460ES | |
| 10619ES | 36717ES | ||
| 10681ES |
| ||
6. Informations de commande
Voici quelques exemples de produits proposés par Yeasen. D'autres tailles sont disponibles.Nos produits sont hautement optimisés pour fonctionner de concert, afin de garantir des performances et une reproductibilité supérieures. Nous pouvons également fournir des services personnalisés. Si vous êtes intéressé par un produit qui n'est pas présenté, contactez-nous et nous travaillerons avec vous pour répondre à vos besoins.
Tableau 3. Informations de commande
Concernant la lecture :
Réactifs de qualité GMP pour la synthèse in vitro d'ARNm
DNase I et leurs applications en biomédecine
Références:
[1] Chaudhary, N., Weissman, D., & Whitehead, KA (2021). Vaccins à ARNm contre les maladies infectieuses : principes, administration et traduction clinique. Revue de la nature. Découverte de médicaments, 20(11), 817–838.
[2] Vogel, AB et al. Les vaccins à ARN auto-amplifiants offrent une protection équivalente contre la grippe aux vaccins à ARNm, mais
à des doses beaucoup plus faibles. Thérapie moléculaire : le journal de l'American Society of Gene Therapy 26, 446-455,
[3] Fuchs, AL, Neu, A. & Sprangers, R. Une méthode générale pour une production à grande échelle rapide et rentable de 5'
ARN coiffé. ARN (New York, NY) 22, 1454-1466, doi:10.1261/rna.056614.116 (2016).
[4] Schmid, A.Considérations relatives à la production de vaccins à ARNm destinés aux essais cliniques. Méthodes en biologie moléculaire (Clifton, NJ) 1499, 237-251,
[5] Banerji, A. et al. Vaccins à ARNm pour prévenir la maladie COVID-19 et les réactions allergiques signalées : données actuelles et approche suggérée. Journal of Allergy and Clinical Immunology. En pratique 9, 1423-1437,
[6] Richner, JM et al. Les vaccins à ARNm modifiés protègent contre l'infection par le virus Zika. Cellule 168, 1114-1125.e1110,
[7] Corbett, KS et al. La conception d'un vaccin à ARNm contre le SRAS-CoV-2 a été rendue possible par la préparation du prototype d'agent pathogène. Nature 586,567-571,
[8] Corbett, KS et al. L'ARNm-1273 protège contre l'infection par le SARS-CoV-2 bêta chez les primates non humains. Nature immunology 22, 1306-1315,
[9] Keech, C. et al. Essai de phase 1-2 d'un vaccin à base de nanoparticules de protéine de pointe recombinante contre le SRAS-CoV-2. The New England journal of medicine 383, 2320-2332,
[10] Kramps, T. & Elbers, K. Introduction aux vaccins à ARN. Méthodes en biologie moléculaire (Clifton, NJ) 1499, 1-11,
[11] Linares-Fernández, S., Lacroix, C., Exposito, JY et Verrier, B. Adapter le vaccin à ARNm pour équilibrer la réponse immunitaire innée/adaptative. Tendances en médecine moléculaire 26, 311-323,
