Il rapido progresso della biotecnologia ha avuto un profondo impatto sulla lotta alle malattie infettive come il COVID-19 attraverso la creazione di vaccini mRNA prodotti tramite la tecnologia di sintesi dell'RNA in vitro. Numerose aziende, tra cui Moderna negli Stati Uniti, CureVac in Germania e BioNTech in Germania, hanno sviluppato non solo vaccini terapeutici mRNA, ma anche trattamenti per condizioni come tumori, malattie infettive e malattie croniche.
La ricerca e la formulazione di vaccini mRNA necessitano di una vasta gamma di materie prime per garantirne il successo nello sviluppo. In qualità di forza pionieristica nel settore degli enzimi molecolari, Yeasen ha ottenuto successo nella creazione di vari enzimi molecolari e reagenti attraverso la biotecnologia avanzata degli enzimi molecolari e tecniche di fermentazione e purificazione delle proteine su larga scala.
Per garantire sia la qualità del prodotto che la capacità produttiva, Yeasen ha istituito un impianto di produzione di livello GMP a Wuhan, in grado di soddisfare pienamente i requisiti di produzione su scala industriale con una capacità annuale superiore a 5 miliardi di unità. Inoltre, Yeasen è la prima azienda cinese ad aver ottenuto la certificazione ISO 13485 per la ricerca, lo sviluppo, la produzione e la distribuzione di enzimi molecolari. Questa certificazione assicura la qualità, la coerenza e la tracciabilità di tutti i suoi reagenti.
1. Vantaggio di GMP
2. Yeasen può fornire prodotti di grado GMP
3. Yeasen ha acquisito i numeri DMF per molti prodotti
4. Scenari applicativi dei prodotti Yeasen
5. Materie prime per la preparazione del vaccino mRNA fornite da Yeasen
6. Informazioni per l'ordinazione
1. Vantaggio di GMP
"GMP-grade" è un termine di branding che Yeasen usa per descrivere i reagenti prodotti in strutture certificate ISO 13485. I reagenti GMP-grade di Yeasen sono prodotti in conformità con gli standard del sistema di gestione della qualità ISO 13485 e con controlli di processo più rigorosi e registrazioni di documentazione complete. Yeasen non solo può offrire reagenti di alta qualità, ma può anche fornire documenti, audit in loco e altro supporto ai nostri clienti.
Tabella 1. Vantaggio di GMP
| Controlli di qualità | Livello di ricerca | Grado GMP |
| Senza animali | Può essere utilizzato materiale derivato da animali | Se richiesto, possono essere forniti certificati di esenzione dagli animali |
| Caratterizzazione della banca cellulare | Meno rigoroso | Rigoroso (conforme alle normative GMP) |
| Informazioni sulla tracciabilità delle materie prime e del prodotto finito | Meno rigoroso | Rigoroso (conforme alle normative GMP) |
| Controllo del livello di endotossina | / | rigoroso |
| Controllo sterile | / | rigoroso |
| Registrazioni di lotti per la produzione e il collaudo | Meno rigoroso | Rigoroso (se necessario, possono essere forniti record di batch) |
| Rapporto di convalida del processo | / | Il rapporto può essere fornito se richiesto |
| Cambia il sistema di controllo | Autovalutazione | Rigoroso (conforme alle normative GMP) |
| Sistema di gestione della qualità | Autovalutazione | Certificazione ISO 13485 |
| Numero DMF | / | Sì (segnalazione) |
2. Yeasen può fornire prodotti di grado GMP
Sfruttando una vasta competenza ed eccellenza tecnica nello sviluppo di enzimi e nella produzione su scala industriale, Yeasen ha creato una struttura all'avanguardia nota come "mRNAtools". Questa struttura, che si estende su 50.000 piedi quadrati, aderisce alle normative GMP e vanta caratteristiche all'avanguardia, tra cui unità di fermentazione automatizzate da 2×1500L, apparecchiature di purificazione su larga scala e capacità di liofilizzazione. mRNAtools è dedicata alla fornitura di reagenti rigorosi che si allineano ai requisiti normativi e di produzione del cliente.
L'impianto di produzione di enzimi molecolari di Yeasen, costruito appositamente per prodotti di grado GMP, salvaguarda la qualità del prodotto sia a livello hardware che software. È composto da un team altamente qualificato di 70 professionisti, ognuno dei quali possiede una vasta esperienza nella produzione GMP. Le operazioni di magazzinaggio e logistica sono modularizzate, garantendo lo stoccaggio sicuro e il trasporto efficiente dei prodotti. Una rete di distribuzione multi-centro a livello nazionale garantisce ulteriormente un ciclo di fornitura affidabile.
3. Yeasen ha acquisito i numeri DMF per molti prodotti
I Drug master file (DMF) sono documenti riservati inviati volontariamente alla Food & Drug Administration (FDA) degli Stati Uniti. Contengono informazioni dettagliate su strutture, processi o articoli utilizzati nella produzione, elaborazione, confezionamento e conservazione di prodotti farmaceutici per uso umano.
La FDA esamina attentamente il contenuto tecnico di un DMF quando un produttore di principi attivi farmaceutici (API) vi fa riferimento per supportare la propria Investigational New Drug Application (IND), New Drug Application (NDA), Abbreviated New Drug Application (ANDA) o Export Application. I DMF svolgono un ruolo fondamentale in queste applicazioni.Quando i produttori presentano DMF per materiali specifici, il processo di approvazione della FDA può essere notevolmente accelerato.
Yeasen possiede file DMF che possono semplificare le tempistiche del progetto. Se lo desideri, puoi richiedere l'autorizzazione di riferimento ai nostri DMF per supportare la tua richiesta FDA. Per avviare l'autorizzazione di riferimento dei nostri DMF, invia una richiesta di lettera di autorizzazione a Yeasen, richiedendoci di fornire una lettera di autorizzazione DMF specifica per il centro FDA.
4. Scenari applicativi dei prodotti Yeasen
4.1 Generazione del modello
La linearizzazione dei plasmidi è un passaggio indispensabile durante la generazione di template quando i vettori plasmidi vengono utilizzati come template di trascrizione. Man mano che la trascrizione procede fino alla fine dei template di DNA, la linearizzazione dei plasmidi assicura che vengano generati trascritti di RNA di una lunghezza e sequenza definite. Yeasen fornisce vari enzimi di restrizione per soddisfare le tue esigenze. Consigliamo di selezionare enzimi di restrizione che generino estremità smussate o sporgenze di 5'.
4.2 In vitro Trascrizione (IVT)
La trascrizione in vitro è influenzata da vari fattori. Enzimi, tamponi e substrati modificati hanno tutti un grande impatto sull'efficienza della trascrizione.
Sulla base della piattaforma ZymeEditor, YEASEN Biotech ha sviluppato nuove RNA polimerasi T7 che riducono significativamente la generazione di dsRNA durante il processo di trascrizione in vitro (IVT) (T7 RNA polimerasi, ds RNA basso, 250 U/μL). Riduce notevolmente l'immunogenicità dell'mRNA e, in una certa misura, ne migliora l'integrità. Si prevede che questo sviluppo svolgerà un ruolo cruciale nel far progredire lo sviluppo di vaccini a mRNA e farmaci contro il cancro.

Ottimizzando il tampone e regolando il tipo di sale del substrato nucleotidico, abbiamo notevolmente migliorato l'efficienza della trascrizione e ridotto la produzione di dsRNA.

Figura 2. Tris NTP può migliorare notevolmente l'efficienza lVT e ridurre la produzione di dsRNA
4.3 Capping dell'mRNA
Poiché una struttura a cappuccio 5' riduce l'immunogenicità ed è necessaria per una traduzione efficiente degli mRNA, è necessario aggiungere strutture a cappuccio alle estremità 5' dell'mRNA generato dalla trascrizione.
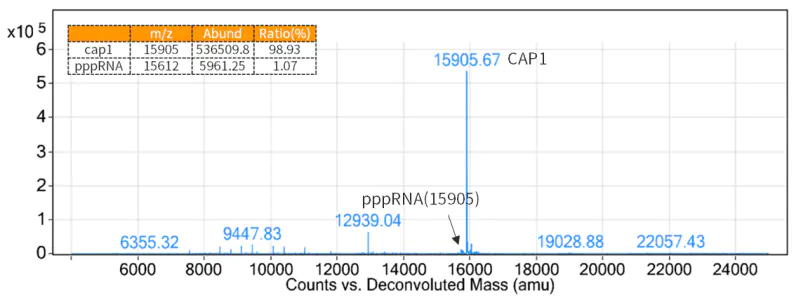
Figura 3. Risultati del rilevamento del tasso di capitalizzazione (rilevamento LC-MS)
4.4 Purificazione dell'mRNA
La purificazione è un passaggio indispensabile per ottenere mRNA ad elevata purezza.
5. Materie prime per la preparazione del vaccino mRNA fornite da Yeasen
Attualmente, Yeasen può fornire un set completo di prodotti nel processo di produzione della soluzione madre di mRNA. I prodotti sono rigorosamente controllati dalla produzione GMP e soddisfano pienamente i requisiti della produzione del vaccino mRNA.
Tabella 2.Materie prime per la preparazione del vaccino mRNA fornite da Yeasen
| Preparazione del modello | Trascrizione in vitro | ||
| 10164ES | 10623ES | ||
| 10122ES | 10625ES | ||
| 10922ES | 10672ES | ||
| 10300ES | 10621ES | ||
|
| 10611ES | ||
| 10661ES | 10133ES | ||
| RNAsi R (20U/uL) | 14615ES | 10650ES | |
| Xba io | 10662ES | 10651ES | |
| Tappatura |
| Purificazione |
|
| 10614ES | 12602ES | ||
| 10612ES | Rack di separazione magnetica | 80460ES | |
| 10619ES | 36717ES | ||
| 10681ES |
| ||
6. Informazioni per l'ordinazione
Di seguito sono riportati i prodotti rappresentativi offerti da Yeasen. Sono disponibili altre misure.I nostri prodotti sono altamente ottimizzati per lavorare in concerto, per aiutare a garantire prestazioni e riproducibilità superiori. Possiamo anche fornire servizi personalizzati. Se sei interessato a un prodotto che non è mostrato, contattaci e lavoreremo con te per soddisfare le tue esigenze.
Tabella 3. Informazioni per l'ordinazione
Per quanto riguarda la lettura:
Reagenti di grado GMP per la sintesi in vitro di mRNA
DNasi I e le loro applicazioni in biomedicina
Riferimenti:
[1] Chaudhary, N., Weissman, D., & Whitehead, KA (2021). Vaccini a mRNA per le malattie infettive: principi, somministrazione e traduzione clinica. Recensioni sulla natura. Scoperta di farmaci, Italiano: 20(11), 817–838.
[2] Vogel, AB et al. I vaccini a RNA autoamplificanti forniscono una protezione equivalente contro l'influenza ai vaccini a mRNA ma
a dosi molto più basse. Terapia molecolare: la rivista della American Society of Gene Therapy 26, 446-455,
[3] Fuchs, AL, Neu, A. & Sprangers, R. Un metodo generale per una produzione su larga scala rapida ed economica di 5'
RNA tappato. RNA (New York, NY) 22, 1454-1466, doi:10.1261/rna.056614.116 (2016).
[4] Giovanni,Considerazioni per la produzione di vaccini mRNA per sperimentazioni cliniche. Metodi in biologia molecolare (Clifton, NJ) 1499, 237-251,
[5] Banerji, A. et al. Vaccini mRNA per prevenire la malattia da COVID-19 e reazioni allergiche segnalate: prove attuali e approccio suggerito. The journal of allergy and clinical immunology. In pratica 9, 1423-1437,
[6] Richner, JM et al. I vaccini mRNA modificati proteggono dall'infezione da virus Zika. Cellula 168, 1114-1125.e1110,
[7] Corbett, KS et al. Progettazione del vaccino mRNA SARS-CoV-2 abilitata dalla preparazione del prototipo del patogeno. Nature 586,567-571,
[8] Corbett, KS et al. mRNA-1273 protegge dall'infezione da SARS-CoV-2 beta nei primati non umani. Nature immunology 22, 1306-1315,
[9] Keech, C. et al. Studio di fase 1-2 di un vaccino con nanoparticelle di proteine Spike ricombinanti SARS-CoV-2. The New England journal of medicine 383, 2320-2332,
[10] Kramps, T. & Elbers, K. Introduzione ai vaccini a RNA. Metodi in biologia molecolare (Clifton, NJ) 1499, 1-11,
[11] Linares-Fernández, S., Lacroix, C., Exposito, JY e Verrier, B. Adattamento del vaccino mRNA per bilanciare la risposta immunitaria innata/adattativa. Tendenze nella medicina molecolare 26, 311-323,
