Liệu pháp tế bào đề cập đến việc sử dụng các phương pháp công nghệ sinh học để thu được các tế bào có chức năng cụ thể, sau đó được tăng cường thông qua các quá trình như mở rộng ex vivo và nuôi cấy chuyên biệt. Các tế bào này được trang bị phản ứng miễn dịch tăng cường, khả năng tiêu diệt tế bào ung thư và mầm bệnh, cùng các chức năng khác để đạt được mục tiêu điều trị cho một số bệnh nhất định. Liệu pháp gen đề cập đến phương pháp điều trị bằng cách sửa đổi biểu hiện gen riêng lẻ hoặc sửa chữa các gen khiếm khuyết thông qua các phương pháp như bổ sung gen, sửa đổi gen và làm gen im lặng. Mục đích cuối cùng là chữa khỏi bệnh bằng cách chỉnh sửa các gen bất thường.
| Sản phẩm Các loại | Sự miêu tả | Con số của Tán thành Thuốc Trên toàn thế giới |
| Gen Liệu pháp Véc tơ Các sản phẩm | Những cái này các sản phẩm sử dụng gen liệu pháp các vectơ ĐẾN giao điều trị gen ĐẾN cụ thể tế bào TRONG cái bệnh nhân mô, nhắm tới vì cái sự biểu lộ hoặc quy định của điều trị protein. Cái này loại dựa vào TRÊN cái vận chuyển của gen liệu pháp vectơ. | 2 |
| Di động Các sản phẩm | Sử dụng tích hợp nổi tiếng các vectơ (như là BẰNG lentivirus vectơ), gen là giới thiệu vào trong tiền thân tế bào hoặc thân cây tế bào bộ gen dưới bán tại sống động điều kiện. BẰNG tế bào chia, cái gen là đi qua ĐẾN hậu duệ tế bào. Các đã sửa đổi tế bào là sau đó truyền vào mặt sau vào trong cái kiên nhẫn. Di động các sản phẩm chủ yếu bao gồm Thể loại như là BẰNG T tế bào, NK tế bào, Và thân cây tế bào. | 8 |
| Thuốc tiêu ung thư Vi-rút Các sản phẩm | Đã được phái sinh từ đã sửa đổi thuốc tiêu ung thư vi-rút với tiêu diệt khối u khả năng, những cái này các sản phẩm công việc TRÊN cái nguyên tắc của sử dụng cái vi-rút cụ thể sự công nhận của khối u tế bào Và cái miễn dịch kích hoạt được kích hoạt trên lây nhiễm khối u tế bào. Cái này dẫn ĐẾN được nhắm mục tiêu giết chết của khối u tế bào. | 1 |
Giải pháp sản xuất và biểu hiện vectơ virus
Cốt lõi của sản xuất thuốc Liệu pháp tế bào và gen (CGT) nằm ở việc biểu hiện các vectơ virus, một quá trình thường liên quan đến cả biểu hiện vectơ thượng nguồn và tinh chế hạ nguồn. Sản xuất vectơ liên quan đến các quá trình cực kỳ phức tạp, đặt ra những thách thức đáng kể và thường có chu kỳ chuẩn bị dài. Do đó, năng lực sản xuất GMP toàn cầu đối với các vectơ virus đang tiến gần đến điểm nghẽn, gây ra trở ngại lớn cho sự phát triển của toàn bộ ngành liệu pháp gen. Việc phát triển, mở rộng quy mô và sản xuất GMP các vectơ liệu pháp gen liên quan đến các hệ thống sản xuất phức tạp và hệ thống kiểm soát chất lượng nghiêm ngặt. Những điều này bao gồm các quy trình như thành lập ngân hàng chủng, tế bào và virus, E.quá trình lên men coli, quá trình nuôi cấy tế bào, quá trình thu hoạch và tinh chế vi-rút, quá trình chế biến vô trùng, quá trình pha chế và đóng gói.
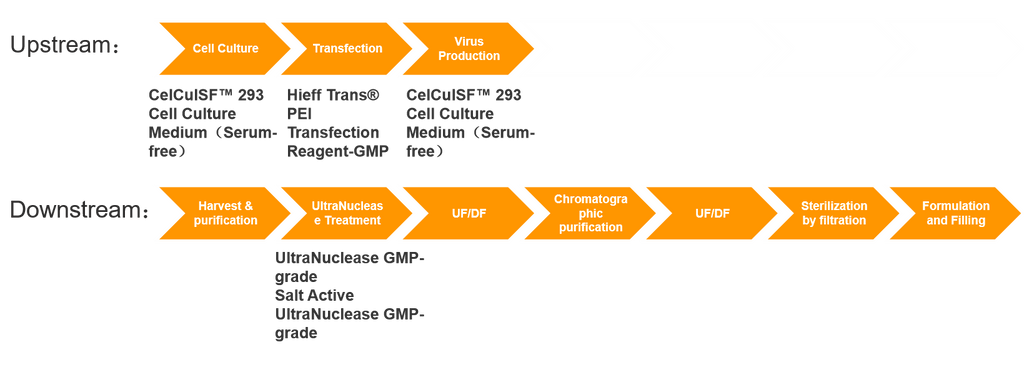
 Chi phí sản xuất AAV
Chi phí sản xuất AAV
Ngoài các khoản đầu tư tài sản cố định (như thiết bị, phòng sạch, v.v.) và chi phí nhân công, các chi phí chính phát sinh từ việc tiêu thụ vật liệu trong các quy trình thượng nguồn và hạ nguồn. Chi phí thượng nguồn chủ yếu liên quan đến nguyên liệu thô như plasmid, môi trường nuôi cấy, thuốc thử chuyển gen và nuclease; chi phí hạ nguồn chủ yếu bao gồm nhựa sắc ký, chi phí kiểm soát chất lượng, v.v.
Chất mang polymer cation
Các polyme cation (polyme) bao gồm polyethylenimine (PEI), poly(beta-amino ester) (PBAE), chitosan, polyacrylamide (PAH), diethylaminoethyl dextran (DEAE-dextran), poly(amidoamine) dendrimer (PAMAM) và các loại khác. Nguyên lý chung của quá trình chuyển gen polyme cation liên quan đến việc tạo phức hợp DNA trong điều kiện pH sinh lý để ngăn chặn sự phân hủy của DNase. Sau đó, các phức hợp này bám vào màng tế bào và được hấp thụ bằng quá trình nội bào, tiếp theo là sự đứt gãy và giải phóng DNA vào tế bào chất để thực hiện các chức năng mong muốn của chúng. Sự khác biệt chính giữa polyme cation và lipid cation nằm ở chỗ không có các phần kỵ nước trong polyme cation, khiến chúng hoàn toàn tan trong nước và cho phép thực hiện các sửa đổi hóa học thuận tiện.
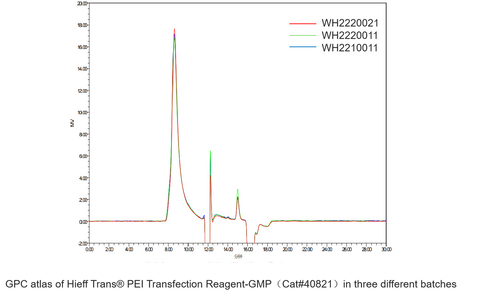
Thuốc thử chuyển gen Hieff Trans® PEI

| Bài kiểm tra Mục | Tiêu chuẩn | Nghiên cứu và phát triển Cấp (40820) | GMP Cấp (40821) |
| MỘTngoại hình | Hoàn thành, chính xác thông tin, KHÔNG hư hại, vân vân | √ | √ |
| Chuyển gen vàhiệu quả | > 70% Chuyển gen hiệu quả> 80% Tế bào khả năng sống | √ | √ |
| Eđộc tố | < 0,5 EU/mL | √ | √ |
| Ssự nguy hiểm | Vô trùng sự phát triển | √ | √ |
| Tôiycoplasma Dư lượng | Ntiêu cực | √ | √ |
| độ pH | < 7.0 | √ | |
| thẩm thấu Prđảm bảo | ≤ 30 mOsm/kg | √ | |
| tạp chất Rdư lượng | Tôietanol≤ 0.3%) Etyl ê-te≤ 0,5%) Metylbenzen≤ 0,002%) | √ | |
| Nặng Tôietal Rdư lượng | ≤ 10 phần triệu |
| √ |
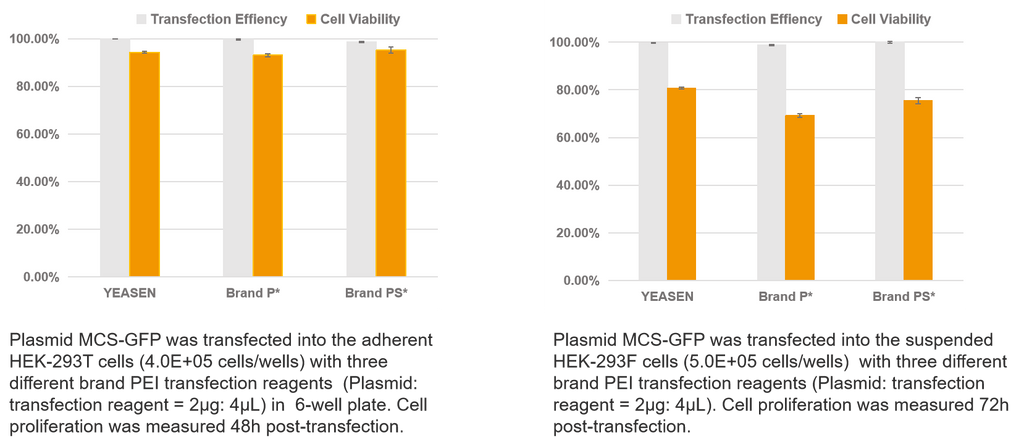
Chuyển gen Plasmid đơn
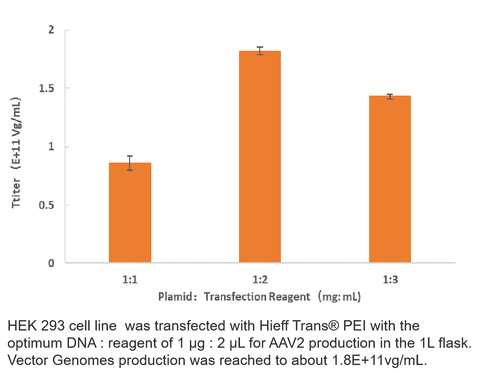
Dữ liệu Titer Virus
1. Sản xuất LV

2. Sản xuất AAV2
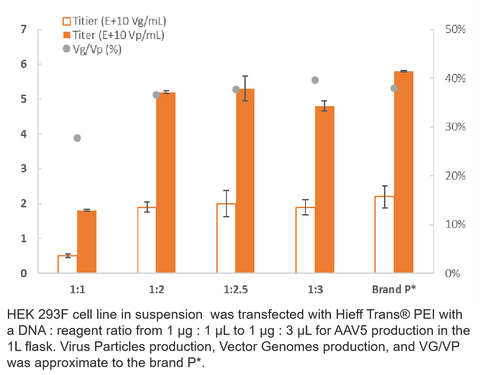
3. Sản xuất AAV5
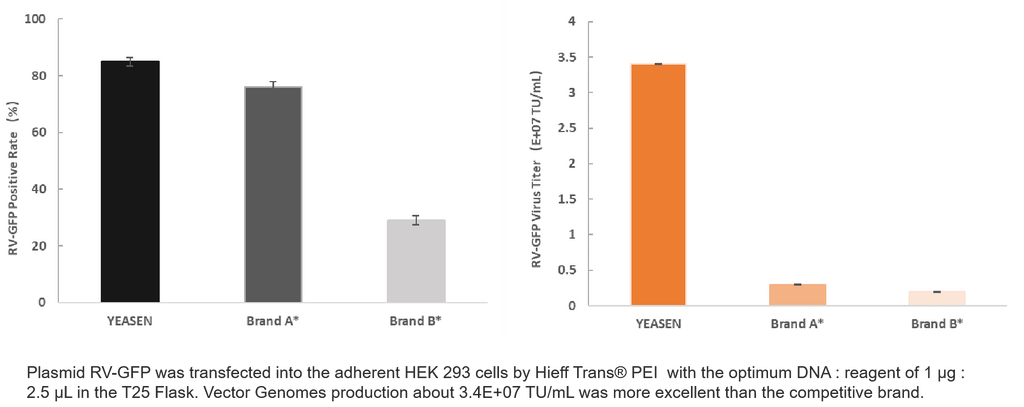
4. Sản xuất RV
Thông tin sản phẩm
| Tên sản phẩm | Số mèo |
| Thuốc thử chuyển gen Hieff Trans® PEI-GMP | 40821ES |
| Bộ dụng cụ phát hiện dư lượng DNA tế bào chủ E.coli | 41308ES |
| Bộ phát hiện dư lượng RNA tế bào chủ E.coli | 41318ES |
| Bộ xét nghiệm E.coli HCP ELISA | 36712ES |
| Bộ xét nghiệm ELISA HEK293 HCP | 36713ES |
| Bộ phát hiện dư lượng DNA tế bào chủ HEK293 | 41302ES |
| Bộ phân tích kích thước DNA dư lượng tế bào chủ HEK293 | 41316ES |
| Bộ phát hiện qPCR thời gian thực MycAway™ Mycoplasma (2G) | 40619ES |
| UCF.ME® UltraNuclease đạt chuẩn GMP | 20157ES |
| Muối hoạt tính UltraNuclease đạt chuẩn GMP | 20159ES |
| Bộ xét nghiệm ELISA UltraNuclease | 36701ES |
| Bộ ELISA Salt Active UltraNuclease | 36703ES |
| Bộ phát hiện số bản sao RCA (E1A) | 41321ES |
| Bộ phát hiện Lentivirus có khả năng sao chép (RCL) | 41311ES |
| Bộ dụng cụ chuẩn bị mẫu DNA dư từ MolPure™ | 18461ES |
